. Autorský rukopis; dostupné v PMC: 1. októbra 2010.
Abstrakt
Gén klotho kóduje jednopriechodový transmembránový proteín, ktorý tvorí komplex s viacerými receptormi fibroblastového rastového faktora (FGF) a funguje ako povinný koreceptor pre FGF23, hormón pochádzajúci z kostí, ktorý vyvoláva negatívnu fosfátovú rovnováhu. Defekty v expresii génov Klotho alebo Fgf23 spôsobujú nielen zadržiavanie fosfátov, ale aj syndróm predčasného starnutia u myší, čo odhaľuje potenciálne spojenie medzi metabolizmom fosfátov a starnutím. Okrem toho je extracelulárna doména proteínu Klotho odstrihnutá na bunkovom povrchu a vylučovaná do krvného obehu, pričom potenciálne funguje ako endokrinný faktor. Secernovaný Klotho proteín má predpokladanú sialidázovú aktivitu, ktorá modifikuje glykány na bunkovom povrchu, čo môže vysvetliť schopnosť secernovaného Klotho proteínu regulovať aktivitu viacerých iónových kanálov a rastových faktorov vrátane inzulínu, IGF-1 a Wnt. Vylučovaný proteín Klotho tiež chráni bunky a tkanivá pred oxidačným stresom prostredníctvom mechanizmu, ktorý ešte nebol identifikovaný. Transmembránové a sekretované formy proteínu Klotho teda majú odlišné funkcie, ktoré môžu spoločne ovplyvniť procesy starnutia u cicavcov.
1. Úvod
V gréckej mytológii tri bohyne určujú dĺžku života každého smrteľníka ovládaním vlákna života. Sú to Klotho, Lachesis a Atropos, ktoré pradú, merajú a pretínajú niť života, resp. Gén klotho , pomenovaný po spinnerovi, bol identifikovaný v roku 1997 ako gén zmutovaný v myši klotho , ktorá vykazuje extrémne skrátenú dĺžku života s viacerými poruchami pripomínajúcimi ľudské syndrómy predčasného starnutia [ 1 ]. Klotho myš bola náhodne vytvorená ako vedľajší produkt počas procesu výroby transgénnych myší konvenčnou pronukleárnou mikroinjekciou transgénu [ 2 ]. Pretože k integrácii transgénu dochádza náhodne v myšacom genóme, transgén môže náhodne narušiť endogénny myšací gén (gény) okolo integračného miesta (inzerčná mutácia), čo občas vedie k neočakávaným fenotypom. Klotho myš bola jednou z transgénnych myších línií, ktorá neexprimovala transgén, a preto sa predpokladalo, že nebude užitočná . Vykazoval však viaceré fenotypy podobné starnutiu, keď bol homozygotný pre transgén v dôsledku inzerčnej mutácie transgénu. Analýza genómu myši klotho odhalila, že ~10 kópií transgénu bolo integrovaných v tandeme na jedinom lokuse na chromozóme 5 a narušilo promótorovú oblasť neznámeho génu, ktorý bol neskôr identifikovaný ako gén klotho [ 1 ].
Gén klotho sa skladá z 5 exónov [ 3 , 4 ] a kóduje jednopriechodový transmembránový proteín typu I (dlhý 1 014 aminokyselín). Intracelulárna doména je krátka (dlhá 10 aminokyselín) a nemá žiadne známe funkčné domény. Extracelulárna doména sa skladá z dvoch domén so slabou homológiou, nazývaných KL1 a KL2. Každá doména má homológiu s glykozidázami rodiny 1, vrátane laktóza-florizín hydrolázy cicavcov a β-glukozidáz baktérií a rastlín [ 1 , 5 ]. Tieto enzýmy majú exoglykozidázovú aktivitu, ktorá hydrolyzuje β-glukozidovú väzbu v sacharidoch, glykoproteínoch a glykolipidoch. Rekombinantný proteín Klotho však nemal enzymatickú aktivitu podobnú β-glukozidáze, pravdepodobne preto, že kritické aminokyselinové zvyšky v domnelých aktívnych centrách proteínu Klotho sa líšia od tých, ktoré sú konzervované v celej skupine enzýmov β-glukozidázy [ 1 , 5 ].
Gén klotho je exprimovaný v obmedzených tkanivách a typoch buniek. Najvyššia expresia sa pozoruje v distálnych stočených tubuloch v obličkách a choroidálnom plexe v mozgu [ 1 ]. Nižšia expresia sa deteguje v hypofýze, mozgu, prištítnych telieskach [ 6 ], pankrease, vaječníkoch, semenníkoch, placente, kostrovom svale, močovom mechúre, hrubom čreve [ 1 ], vnútornom uchu [ 7 ] a epiteliálnych bunkách prsníka [ 8 ]. Expresia génu Klotho je u klotho myši silne potlačená v dôsledku inzerčnej mutácie v 5′ priľahlej oblasti génu klotho [ 1 ]. Klotho myš teda nie je nulový, ale závažný hypomorfný kmeň. Nulový kmeň pre gén klotho bol neskôr vytvorený konvenčným zacielením génu a vykazoval fenotypy podobné starnutiu identické s fenotypmi pozorovanými u pôvodnej myši klotho [ 9 ]. Preto sú myš Klotho -/- a pôvodná myš klotho v tomto prehľade súhrnne opísané ako myši s deficitom Klotho.
2. Klotho-deficientné myši
Klotho-deficitné myši sú takmer na nerozoznanie od svojich divokých a heterozygotných súrodencov z vrhu vzhľadom a rastom až do veku 3 týždňov. Potom prestanú rásť a takmer nepriberajú na váhe, až kým predčasne nezomrú okolo 8. – 9. týždňa veku. Hoci vykazujú viaceré patológie pripomínajúce ľudské starnutie, ako je opísané nižšie, konkrétna príčina smrti nie je jasná, pretože každá z týchto patológií sa sama o sebe nezdá byť smrteľná [ 1 ].
2.1. Hypogonadizmus
Klotho-deficientné myši majú atrofické vonkajšie a vnútorné pohlavné orgány u oboch pohlaví. Nikdy sa nestanú sexuálne dospelými a sú neplodné. Semenník je extrémne atrofický a neobsahuje žiadne zrelé spermie. Zrenie spermatocytov je zastavené v štádiu pachyténu. Ovarium obsahuje iba primárne alebo sekundárne folikuly a žiadne Graafove folikuly alebo žlté teliesko [ 1 ]. Hoci expresia Klotho je zistiteľná vo vaječníkoch, zhoršené dozrievanie folikulov u myší s deficitom Klotho nie je spôsobené defektom vaječníkov, ale je spôsobené poruchou funkcie hypofýzy a/alebo hypotalamu (hypogonadotropný hypogonadizmus), pretože 1) sérové LH a FSH hladiny u myší s deficitom Klotho sú nižšie ako u myší divokého typu, 2) dozrievanie folikulov a rast 3) vaječníky myší s deficitom Klotho fungujú normálne, keď sa transplantujú do samičiek myší divokého typu [ 10 ]. Tieto pozorovania naznačujú, že Klotho sa môže podieľať na regulácii produkcie/sekrécie hormónov uvoľňujúcich gonadotropín a gonadotropín v hypofýze a hypotalame.
2.2. Predčasná involúcia týmusu
Týmus myší s deficitom Klotho sa normálne vyvíja až do veku 3–4 týždňov a potom sa rýchlo zmenšuje, až kým sa vo veku 6–9 týždňov stane sotva detegovateľným [ 1 ]. Thymopoetická nedostatočnosť u myší s deficitom Klotho nie je spôsobená vnútorným defektom lymfohematopoetických progenitorov, pretože krvotvorné kmeňové bunky z myší s deficitom Klotho sa môžu po transplantácii do myší SCID diferencovať na normálne lymfoidné bunky [ 11 ]. Je to spôsobené defektom epitelových buniek týmusu, ktoré podporujú proliferáciu a prežitie tymocytov. Táto patofyziológia je podobná patofyziológii pozorovanej pri involúcii týmusu spojenej s normálnym procesom starnutia. Dôležité je, že injekcia KGF (keratinocytový rastový faktor, aka FGF7), ktorý indukuje proliferáciu buniek týmusového epitelu, zlepšuje tymopoézu a obnovuje degeneráciu týmusu nielen u myší s deficitom Klotho, ale aj u starých myší divokého typu [ 11 ].
2.3. Ektopická kalcifikácia
U myší s deficitom Klotho sa pozoruje rozsiahla ektopická kalcifikácia v rôznych mäkkých tkanivách. Najvýraznejšie sa vyskytuje v žalúdočnej sliznici, priedušnici, renálnych tubuloch a malých artériách v obličkách, ako aj väčších artériách vrátane renálnych artérií a aorty. Vaskulárna kalcifikácia sa vyskytuje v médiu bez súčasného zhrubnutia intimy alebo akumulácie penových buniek. Tieto vaskulárne zmeny teda nie sú typickou aterosklerózou, ale pripomínajú artériosklerózu Mönckebergovho typu často pozorovanú u starších ľudí, ako aj u pacientov s cukrovkou a chronickým ochorením obličiek u ľudí [ 1 ]. Ektopická kalcifikácia a vaskulárna kalcifikácia u myší s deficitom Klotho môže byť sekundárna v dôsledku zvýšených hladín vápnika, fosfátu a vitamínu D v krvi [ 9 , 12 ]. Mechanizmus, ktorým nedostatok Klotho spôsobuje zhoršený metabolizmus vápnika/fosfátu, je podrobne diskutovaný neskôr.
2.4. Zhoršená mineralizácia kostí
Klotho-deficientné myši majú osteopéniu [ 1 , 13 ]. Hrúbka kortikálnej kosti stehennej kosti, holennej kosti a stavcov je v porovnaní s myšami divokého typu znížená o 20–40 %. Histomorfometrická analýza kosti ukazuje, že osteopénia u myší s deficitom Klotho je sprevádzaná významným znížením tvorby aj resorpcie kosti. Zníženie tvorby kosti prevyšuje zníženie kostnej resorpcie, čo vedie k čistej strate kostnej hmoty s nízkym kostným obratom. Táto patofyziológia je podobná patofyziológii pozorovanej pri senilnej osteoporóze u starších ľudí, ale odlišuje sa od postmenopauzálnej osteoporózy u žien vyvolanej vysadením estrogénu, pretože postmenopauzálna osteoporóza je primárne spôsobená zvýšenou kostnou resorpciou v dôsledku zvýšeného počtu a funkcie osteoklastov, čo vedie k vysoký kostný obrat. Hoci sú kortikálne kosti u Klotho-deficientných myší redukované, paradoxne majú zväčšené trabekulárne kosti na stavcoch a metafýze holennej kosti a stehennej kosti [ 13 – 15 ]. Aj keď mechanizmus, ktorým nedostatok Klotho ovplyvňuje kortikálne a trabekulárne kosti iným spôsobom, je potrebné určiť, môže ísť o dysreguláciu signálnej dráhy Wnt, o ktorej sa bude hovoriť neskôr.
2.5. Atrofia kože
Koža myší s deficitom Klotho je tenká a atrofická. Histologické vyšetrenie ukazuje znížený počet vlasových folikulov a zníženú hrúbku dermálnych a epidermálnych vrstiev. Nie je pozorovaný žiadny podkožný tuk. Tieto nálezy sú podobné tým, ktoré sa pozorovali pri senilnej atrofodermii vo veku [ 1 ].
2.6. Emfyzém pľúc
Histológia pľúc myší s deficitom Klotho je nerozoznateľná od histológie pľúc súrodencov divokého typu vo veku do 2 týždňov, kedy sa pľúca stanú zrelými. Približne vo veku 4 týždňov pľúca myší s deficitom Klotho podliehajú progresívnym emfyzematóznym zmenám vrátane deštrukcie alveolárnych stien a zväčšenia vzduchových priestorov [ 1 ]. Okrem histologických zmien je respiračná funkcia Klotho-deficientných myší v súlade s pľúcnym emfyzémom charakterizovaným zvýšenou poddajnosťou a exspiračným časom [ 16 ]. Starnutie a fajčenie boli identifikované ako dva hlavné rizikové faktory pľúcneho emfyzému. Matematický model naznačuje, že model alveolárnej deštrukcie u myší s deficitom Klotho je v súlade s náhodnou deštrukciou spôsobenou systémovým faktorom (faktormi) a nie korelovanou deštrukciou spôsobenou lokálnym faktorom (faktormi), ako je fajčenie [ 17 ]. Pľúca myší s deficitom Klotho teda môžu predstavovať pľúcny emfyzém súvisiaci so starnutím.
2.7. Neurodegenerácia
Klotho-deficientné myši majú v porovnaní s myšami divokého typu zhoršenie kognitívnych funkcií meraných pomocou rozpoznávania nových objektov a testov podmieneného strachu [ 18 ]. Zhoršenie kognície u myší s deficitom Klotho je spojené so zvýšeným počtom apoptotických buniek a zvýšenými hladinami oxidovaných lipidov a DNA v hipokampe. Okrem toho liečba myší s deficitom Klotho antioxidačným a-tokoferolom zlepšuje kognitívne poškodenie a znižuje oxidačné poškodenie a apoptotické bunky v hipokampe, čo naznačuje, že Klotho môže fungovať ako neuroprotektívny faktor prostredníctvom zabránenia oxidačnému poškodeniu neurónov. Okrem toho myši s deficitom Klotho vykazovali degeneratívne zmeny buniek predného rohu (AHC) v mieche. Je to podobné ako nález pozorovaný u pacientov s amyotrofickou laterálnou sklerózou (ALS). AHC myší s deficitom Klotho vykazujú významný pokles cytoplazmatickej RNA, ribozómov a drsného endoplazmatického retikula a akumuláciu neurofilamentov ako u pacientov s ALS [ 19 ]. Nedávne štúdie ukázali, že zvýšený oxidačný stres môže byť spoločným mechanizmom mnohých neurodegeneratívnych porúch vrátane Alzheimerovej choroby, Parkinsonovej choroby a ALS [ 20 ]. Schopnosť proteínu Klotho zmierniť oxidačný stres (diskutované neskôr) môže prispieť k neuroprotektívnym vlastnostiam Klotho.
2.8. Strata sluchu
Gén klotho je exprimovaný v stria vascularis a špirálovom väzive vnútorného ucha. Hoci Klotho-deficientné myši nemajú žiadne morfologické abnormality vo vnútornom uchu, majú signifikantne vyšší prah pre sluchovú odpoveď mozgového kmeňa ako myši divokého typu, čo naznačuje existenciu poruchy sluchu [ 7 ]. Hoci funkcia Klotho vo vnútornom uchu nie je známa, je možné, že proteín Klotho sa môže podieľať na homeostáze elektrolytov endolymfy v kochleárnom kanáliku prostredníctvom svojej aktivity, ktorá reguluje iónové kanály.
2.9. Chémia krvi
Myši s deficitom Klotho majú vyššie hladiny sérového fosforu, vápnika a aktívneho vitamínu D (1,25-dihydroxyvitamín D 3 ) [ 9 ] a nižšie hladiny glukózy v sére [ 21 ] ako myši divokého typu. Dôležité je, že tieto abnormálne opatrenia sa pozorujú už vo veku 2 týždňov predtým, ako sa u myší s deficitom Klotho vyvinú viditeľné fenotypy podobné starnutiu. Mechanizmus abnormálnej chémie krvi je úzko spojený s funkciou proteínu Klotho a podrobne sa o ňom diskutuje neskôr.
2.10. Fenotypy neboli pozorované u myší s deficitom Klotho
Všetky tieto fenotypy sa vyskytujú u každej myši s deficitom Klotho so 100% penetráciou. Je pozoruhodné, že niekoľko fenotypov podobných starnutiu je pozorovaných v tkanivách, ktoré endogénne neexprimujú Klotho, čo naznačuje, že funkciu proteínu Klotho sprostredkúva humorálny faktor (faktory). Ako negatívne zistenia zatiaľ neexistuje žiadna správa, ktorá by naznačovala, že myši s deficitom Klotho majú zvýšený výskyt zhubných nádorov alebo zvýšené amyloidné plaky alebo neurofibrilárne spleti v mozgu, čo sú bežné znaky starnutia. Je možné, že uhynú príliš skoro (okolo 2 mesiacov veku), aby sa u nich rozvinuli tieto choroby. Hoci existujú rozdiely medzi patofyziológiou pozorovanou u myší s deficitom Klotho a pri prirodzenom starnutí, myši s deficitom Klotho sa použili ako jeden z najlepšie charakterizovaných cicavčích modelov syndrómov predčasného starnutia, ktoré sa prejavujú viacerými fenotypmi podobnými starnutiu u jedného jedinca.
3. Transgénne myši s nadmernou expresiou Klotho
Boli stanovené dve nezávislé línie transgénnych myší, ktoré nadmerne exprimovali transmembránovú formu proteínu Klotho pod kontrolou všadeprítomného promótora (promótor ľudského elongačného faktora-1α) [ 1 ]. Jedna z nich ( EFmKL46 ) exprimovala exogénne Klotho v každom doteraz skúmanom tkanive, zatiaľ čo druhá línia ( EFmKL48 ) exprimovala transgén len v niekoľkých tkanivách vrátane mozgu a semenníkov, ale nie v obličkách, pravdepodobne v dôsledku polohového efektu transgénu integračná stránka. Napriek nedostatku Klotho v obličkách, kde je endogénna expresia Klotho najhojnejšia, alela EFmKL48 bola schopná zachrániť fenotypy podobné starnutiu, keď sa zaviedla do myší s deficitom Klotho, čo naznačuje, že expresia v obličkách nemusí byť pre proteín Klotho nevyhnutná. funkciu. To je v súlade s predstavou, že humorálny faktor (faktory) môže sprostredkovať funkciu proteínu Klotho. Transgénne myši EFmKL46 aj EFmKL48 vyzerali normálne a žili v priemere o 20–30 % dlhšie ako myši divokého typu [ 22 ]. Predĺženie životnosti pozorované u týchto myší nie je také robustné ako to, ktoré sa pozorovalo u trpasličích myší nesúcich defekty v somatotrofnej osi [ 23 – 25 ] a je potrebné ho potvrdiť v rôznych podmienkach ustajnenia. Napriek tomu sa gén klotho považuje za jeden z génov na potlačenie starnutia identifikovaných u cicavcov, ktorý pri nadmernej expresii predlžuje životnosť a pri narušení spôsobuje syndróm predčasného starnutia. Keďže spotreba potravy transgénnych myší nie je znížená, je nepravdepodobné, že by žili dlhšie len preto, že jedli menej a dobrovoľne obmedzili príjem kalórií [ 22 ]. Ako je diskutované neskôr, transgénne myši, ktoré nadmerne exprimujú Klotho, vykazujú významnú odolnosť voči oxidačnému stresu spojenú so strednou rezistenciou na inzulín / IGF-1, čo môže čiastočne vysvetliť, prečo tieto myši žijú dlhšie ako myši divokého typu.
Ďalší súbor transgénnych myší, ktoré nadmerne exprimujú Klotho, bol vytvorený pomocou indukovateľného promótora (myší promótor metalotioneínu-1) na riadenie expresie transmembránovej formy Klotho [ 26 ]. Klotho-deficientné myši nesúce tento indukovateľný transgén do značnej miery závisia na kŕmení zinkovou vodou pri expresii Klotho. Keď sa tieto myši neliečia, vyvinú sa u nich príznaky predčasného starnutia ako u myší s deficitom Klotho. Po podaní 25 mM roztoku ZnSO 4 ako pitnej vody tieto myši exprimujú exogénne Klotho primárne v gastrointestinálnom trakte, čo zachraňuje všetky fenotypy podobné starnutiu. Ešte dôležitejšie je, že mnoho pokročilých fenotypov podobných starnutiu je zachránených, keď je expresia Klotho indukovaná kŕmením zinkom, aj keď už vyvinuli viaceré fenotypy podobné starnutiu. Okrem toho zníženie expresie Klotho odstránením zinku u týchto zachránených myší s deficitom Klotho rýchlo indukuje niekoľko fenotypov podobných starnutiu vrátane ektopickej kalcifikácie a pľúcneho emfyzému. Tieto pozorovania naznačujú, že zníženie expresie Klotho v dospelosti môže byť príčinou niekoľkých porúch podobných starnutiu a že náhrada Klotho môže byť užitočná na liečbu týchto porúch. V skutočnosti bol Klotho nedávno identifikovaný ako jeden z génov, ktorých expresia bola významne znížená s vekom v mozgu hlodavcov a primátov (opice rhesus) [ 27 ].
4. Funkcie proteínu Klotho
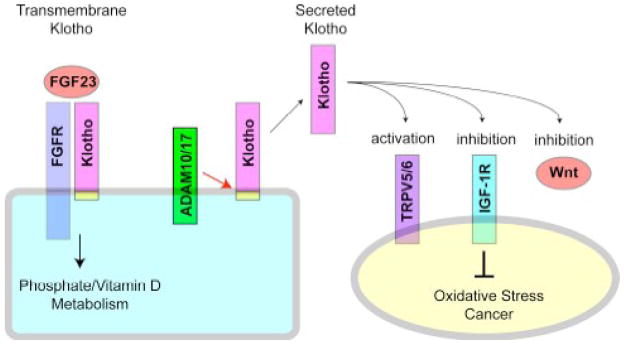
Gén klotho kóduje jednopriechodový transmembránový proteín. Extracelulárna doména proteínu Klotho je odstrihnutá tesne nad plazmatickou membránou proteázami ADAM10 a ADAM17 ukotvenými v membráne, aby sa vytvorila sekretovaná forma proteínu Klotho [ 28 ]. V skutočnosti je celá Klotho ektodoména detegovateľná ako jediný peptid v krvi, moči a cerebrospinálnej tekutine [ 22 , 29 ]. Klotho proteín teda existuje v dvoch formách. Jedna je transmembránová forma exprimovaná primárne v renálnych tubulárnych bunkách a druhá je secernovaná forma cirkulujúca v krvi ( obr. 1 ).
Obrázok 1
Okrem týchto dvoch foriem proteínu Klotho sa mRNA kódujúca inú formu vylučovaného proteínu Klotho vytvára prostredníctvom alternatívneho donorového miesta zostrihu v 3. exóne . Výsledná mRNA kóduje domnelý secernovaný proteín, ktorý pozostáva zo samotnej domény KL1 a chýba mu KL2, transmembránová a intracelulárna doména [ 3 , 4 ]. Skrátená ektodoména (len doména KL1) však nebola v krvi zistená. Tento prehľad sa teda zameriava na funkciu dvoch foriem proteínu Klotho: transmembránovej formy a sekretovanej formy s celou extracelulárnou doménou.
4.1. Funkcia transmembránovej formy Klotho
4.1.1. Regulácia metabolizmu fosfátov
Hladina fosfátov v krvi je určená protiváhou medzi príjmom potravy z čreva, mobilizáciou z kostí (hlavný rezervoár vápnika a fosfátu v tele) a vylučovaním z obličiek do moču [ 30 ]. Metabolizmus fosfátov je regulovaný niekoľkými endokrinnými faktormi. Vitamín D a parathormón (PTH), ktoré boli rozsiahle študované ako endokrinné faktory regulujúce metabolizmus vápnika [ 31 ], sa tiež podieľajú na metabolizme fosfátov. Aktívna forma vitamínu D (1,25-dihydroxyvitamín D 3 ) sa syntetizuje v obličkách a pôsobí v čreve na zvýšenie absorpcie vápnika a fosfátu z potravy. Pôsobí tiež na kosti, stimuluje osteoklastogenézu a podporuje mobilizáciu vápnika a fosfátu z rezervoáru, čím zvyšuje hladinu vápnika aj fosfátu v krvi. PTH pôsobí na obličky tak, že podporuje syntézu vitamínu D a fosfatúriu (vylučovanie fosfátov do moču). Výsledkom je, že na rozdiel od vitamínu D môže PTH selektívne zvyšovať hladiny vápnika v krvi bez súčasného zvýšenia hladín fosfátov v krvi [ 32 ].
Nedávne štúdie identifikovali FGF23 ako nový endokrinný faktor, ktorý znižuje hladiny fosfátov a vitamínu D v krvi [ 33 – 35 ]. FGF23 sa vylučuje z osteocytov ako odpoveď na vysoké hladiny fosfátov a vitamínu D v krvi [ 36 ]. FGF23 pôsobí na obličky tak, že 1) indukuje fosfatúriu potlačením kotransportérov Na-fosfátu v renálnych tubulárnych bunkách a 2) kontrareguluje vitamín D znížením expresie génu Cyp27b1 kódujúceho 1α-hydroxylázu, enzým, ktorý syntetizuje 1,25-dihydroxyvitamín D3 z jeho neaktívneho prekurzora (25-hydroxyvitamín D3 ) a upreguláciou expresie génu Cyp24 kódujúceho 24-hydroxylázu, enzým, ktorý inaktivuje 1,25-dihydroxyvitamín D 3 [ 31 ]. Výsledkom je, že FGF23 znižuje sérový 1,25-dihydroxyvitamín D3 , čo následne znižuje absorpciu fosfátov z čreva. FGF23 teda indukuje negatívnu fosfátovú rovnováhu tým, že funguje ako fosfaturový hormón, ako aj ako kontraregulačný hormón pre vitamín D [ 35 , 37 , 38 ].
FGF23 bol pôvodne identifikovaný ako gén mutovaný u pacientov s autozomálne dominantnou hypofosfatemickou krivicou (ADHR) [ 34 ]. Pacienti s ADHR nesú v géne FGF23 mutácie zosilnenia funkcie , ktoré prepožičiavajú rezistenciu na proteolytickú inaktiváciu proteínu FGF23 a vykazujú zvýšené hladiny FGF23 v krvi, čo vedie k hypofosfatémii a poruche mineralizácie kostí v dôsledku plytvania fosfátmi. Na rozdiel od toho mutácie so stratou funkcie v géne FGF23 spôsobujú hyperfosfatémiu a hypervitaminózu D spojenú s ektopickou kalcifikáciou v rôznych mäkkých tkanivách a krvných cievach, ako sa pozorovalo u myší s knockoutom Fgf23 [ 39 ] a pacientov s familiárnou nádorovou kalcinózou [ 40 ]. Okrem týchto predvídateľných fenotypov sa u myší s deficitom FGF23 vyvinú viaceré fenotypy podobné starnutiu, ktoré sú takmer totožné s fenotypmi pozorovanými u myší s deficitom Klotho. Tieto pozorovania naznačujú, že FGF23 a Klotho môžu fungovať v spoločnej dráhe prenosu signálu.
Identita receptora FGF23 nebola jasná, pretože všetky známe receptory FGF mali extrémne nízku afinitu k FGF23 in vitro [ 41 , 42 ], čo naznačuje existenciu kofaktorov, ktoré zvyšujú afinitu FGF23 k receptoru (receptorom) FGF v jeho cieľový orgán(y). V skutočnosti sa ukázalo, že transmembránový proteín Klotho tvorí komplex s niekoľkými izoformami receptora FGF (FGFR-1c, -3c a -4) na bunkovom povrchu a významne zvyšuje ich afinitu k FGF23. Konkrétne, Klotho funguje ako povinný koreceptor pre FGF23 [ 43 ]. Toto zistenie bolo neskôr potvrdené nezávislou štúdiou [ 44 ]. Skutočnosť, že FGF23 vyžaduje Klotho na väzbu na receptory FGF, vysvetľuje, prečo myši s deficitom Klotho a myši s deficitom FGF23 majú identické fenotypy. Okrem toho expresia Klotho špecifická pre obličky vysvetľuje, prečo môže FGF23 identifikovať obličky ako svoj hlavný cieľový orgán medzi mnohými orgánmi, ktoré exprimujú receptory FGF. Nová endokrinná os kosť-obličky sprostredkovaná FGF23 a Klotho sa teda ukázala ako primárny mechanizmus endokrinnej regulácie metabolizmu fosfátov a vitamínu D.
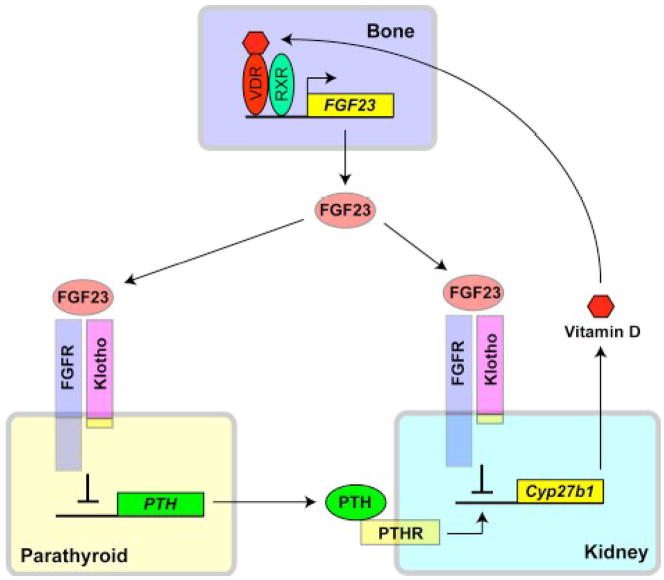
Skutočnosť, že Klotho funguje ako povinný koreceptor pre FGF23, naznačuje, že orgány, ktoré exprimujú Klotho, sú potenciálnymi cieľovými orgánmi pre FGF23, pretože väčšina tkanív exprimuje jednu alebo viacero izoforiem receptora FGF. Prištítna žľaza je jedným z mála orgánov, ktoré endogénne exprimujú Klotho a nedávno bola identifikovaná ako cieľový orgán FGF23 [ 6 ]. FGF23 potláča expresiu a sekréciu PTH v prištítnych telieskach [ 6 , 45 ]. Pretože PTH podporuje biosyntézu vitamínu D v obličkách, táto nová endokrinná os kostných prištítnych teliesok sprostredkovaná FGF23 a Klotho ďalej zvyšuje aktivitu FGF23 ako kontraregulačného hormónu proti vitamínu D. Za zmienku stojí, že vitamín D indukuje expresiu FGF23 v kosti prostredníctvom aktivácia receptora vitamínu D [ 46 ]. Do endokrinnej regulácie metabolizmu fosfátu a vitamínu D sa teda podieľa viacero spätnoväzbových slučiek sprostredkovaných Klotho a FGF23 ( obr. 2 ).
Obrázok 2
Pretože sérový vitamín D podporuje absorpciu fosfátu a vápnika z potravy z čreva, zvýšené hladiny vitamínu D môžu byť príčinou hyperfosfatémie a hyperkalcémie u myší s deficitom Klotho a myší s deficitom FGF23. Zvýšenie hladín vápnika aj fosfátu v krvi vedie k významnému zvýšeniu produktu fosforečnanu vápenatého (Ca × P), čo je predispozícia k ektopickej kalcifikácii krvných ciev a mäkkých tkanív. Dôležité je, že nielen ektopická kalcifikácia, ale aj mnohé ďalšie fenotypy podobné starnutiu pozorované u myší s deficitom FGF23 a Klotho, vrátane hypogonadizmu, hypoglykémie, pľúcneho emfyzému a atrofie kože, svalov a týmusu, sú zachránené diétou s nízkym obsahom fosfátov alebo diétou s nízkym obsahom vitamínu D alebo abláciou aktivity vitamínu D narušením génu receptora vitamínu D [ 47 ] alebo gén la-hydroxylázy [ 9 , 48 – 51 ]. Je potrebné poznamenať, že vysoký obsah vitamínu D môže sám o sebe spustiť apoptózu a potenciálne spôsobiť atrofiu tkaniva [ 52 ]. Tieto pozorovania naznačujú, že fenotypy podobné starnutiu u myší s deficitom FGF23 a myší s deficitom Klotho sú primárne spôsobené toxicitou nadbytku fosfátu a/alebo vitamínu D. Treba poznamenať, že diéta s nízkym obsahom fosfátov ďalej zvyšuje už tak zvýšené hladiny vitamínu D v sére a hladiny vápnika, ale stále môžu zachrániť fenotypy podobné starnutiu u myší s deficitom FGF23 [ 51 ]. Preto je to fosfát, ale nie vitamín D ani vápnik, ktorý je zodpovedný za fenotypy podobné starnutiu. Je pravdepodobné, že diéta s nízkym obsahom vitamínu D alebo narušenie génu receptora vitamínu D alebo génu la-hydorxylázy zachraňujú fenotypy podobné starnutiu prostredníctvom riešenia retencie fosfátov odstránením účinku vitamínu D. Zostáva určiť, či hypervitaminóza D je nevyhnutným predpokladom na to, aby zadržiavanie fosfátov spôsobilo viaceré fenotypy podobné starnutiu. Tieto pozorovania tiež naznačujú nový koncept, že metabolizmus fosfátov sa môže podieľať na regulácii starnutia.
4.1.2. Endokrinné FGF a Klothos
FGF23 patrí do podrodiny FGF19 v superrodine ligandov FGF. Podrodina FGF19 pozostáva z FGF15, FGF19 (ľudský ortológ myšieho FGF15), FGF21 a FGF23 [ 53 ]. Tieto FGF sa tiež súhrnne nazývajú endokrinné FGF, pretože fungujú ako hormóny na rozdiel od iných FGF, ktoré fungujú ako parakrinné a/alebo autokrinné faktory. Nedávne štúdie odhalili nové endokrinné osi sprostredkované týmito endokrinnými FGF. Stručne povedané, FGF19 (ľudský ortológ FGF15) sa vylučuje z buniek črevného epitelu ako odpoveď na žlčovú kyselinu uvoľnenú pri kŕmení [ 54 ]. FGF15/19 pôsobí na pečeň a znižuje syntézu žlčových kyselín prostredníctvom potlačenia expresie génu Cyp7a1 , ktorý kóduje enzým obmedzujúci rýchlosť syntézy žlčových kyselín [ 54 ]. Okrem toho FGF15/19 pôsobí na žlčník, aby vyvolal plnenie žlčových kyselín a obmedzil uvoľňovanie žlčových kyselín do čreva [ 55 ]. FGF15/19 je teda zapojený do postprandiálnej negatívnej spätnej väzby, ktorá reguluje syntézu a uvoľňovanie žlčových kyselín. Na rozdiel od FGF15/19 sa FGF21 vylučuje z pečene nalačno a pôsobí na adipocyty na podporu vychytávania glukózy [ 56 ] a lipolýzy [ 57 ]. Podobne ako FGF23, aj FGF15/19 a FGF21 vyžadujú ko-receptor na väzbu na ich príbuzné receptory FGF s vysokou afinitou. Koreceptorom je βKlotho, proteín súvisiaci s Klotho, ktorý zdieľa ~40% identitu aminokyselinovej sekvencie [ 58 ]. βKlotho je exprimovaný prevažne v pečeni a bielom tukovom tkanive, zatiaľ čo Klotho je exprimovaný hlavne v obličkách. βKlotho tiež tvorí komplex s niekoľkými izoformami receptora FGF a výrazne zvyšuje ich afinitu k FGF15/19 a FGF21 [ 59 ]. Tieto zistenia vysvetľujú, prečo sa u všetkých myší s defektom v βKlotho [ 60 ], FGFR4 [ 61 ] alebo FGF15 [ 54 ] vyvíja zvýšená syntéza žlčových kyselín. Rodina génov Klotho (Klotho a βKlotho) sa teda mohla vyvinúť pri regulácii endokrinných FGF. Vznikajúcim konceptom je, že tkanivovo špecifická expresia členov rodiny génov Klotho určuje cieľové orgány endokrinných FGF. To môže predstavovať nový mechanizmus regulácie interakcie ligand-receptor v cieľových orgánoch [ 62 – 64 ].
4.2. Funkcia sekretovanej formy Klotho
Transmembránová forma proteínu Klotho funguje ako koreceptor pre FGF23, keď tvorí komplex s receptormi FGF na bunkovom povrchu. Vylučovaný proteín Klotho však nemôže fungovať ako rozpustný receptor pre FGF23, pretože samotný proteín Klotho sa nemôže viazať na FGF23 s vysokou afinitou [ 43 ], čo naznačuje, že vylučovaný proteín Klotho môže fungovať nezávisle od FGF23. Vylučovaný Klotho proteín (Klotho ektodoména) má homológiu s glykozidázami rodiny 1, ktoré štiepia glykozidické väzby v cukroch, glykolipidoch a glykoproteínoch. Rekombinantný proteín ektodomény Klotho má in vitro slabú aktivitu β-glukuronidázy [ 65 ], hoci fyziologický význam enzymatickej aktivity proteínu Klotho nebol známy. Nedávno sa ukázalo, že secernovaný Klotho proteín má predpokladanú sialidázovú aktivitu [ 66 ] a podieľa sa na odstraňovaní koncových sialových kyselín z cukrových reťazcov viacerých glykoproteínov na bunkovom povrchu, aby sa zmenila ich aktivita a/alebo abundancia na bunkovom povrchu. Vylučovaný proteín Klotho sa teda ukázal ako nový endokrinný regulátor funkcie glykoproteínu na bunkovom povrchu.
4.2.1. Regulácia aktivity iónových kanálov
Extracelulárna doména proteínu Klotho funguje ako silný aktivátor iónových kanálov prechodného receptora TRPV5 a TRPV6 [ 67 ]. TRPV5 a TRPV6 sú vápnikové kanály exprimované prevažne v renálnych tubulárnych bunkách a duodenálnych epitelových bunkách, v danom poradí, a sú zodpovedné za vstup Ca2 + pri transcelulárnej (re)absorpcii Ca2 + v obličkách a čreve [ 68 ]. Vylučovaný Klotho proteín, keď sa pridal do kultivačného média buniek HEK293 exprimujúcich TRPV5, zvýšil príliv Ca2 + a množstvo TRPV5 na povrchu buniek. Klotho-indukovaná retencia TRPV5 na plazmatickej membráne bola spojená s modifikáciou glykánov TRPV5. Je však nepravdepodobné, že Klotho odstránil glukurónové kyseliny z TRPV5 glykánov svojou slabou β-glukuronidázovou aktivitou, pretože typické N-viazané glykány cicavčích glykoproteínov nemajú glukurónové kyseliny. Endogénne cukrové substráty pre Klotho a mechanizmus, ktorým modifikácia glykánu mení množstvo TRPV5 na bunkovom povrchu, zostali nejasné.
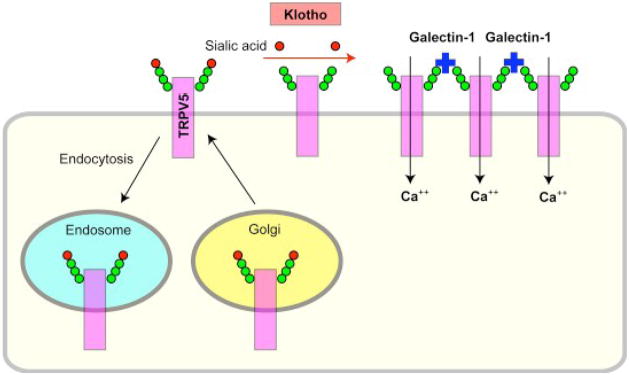
Nedávno sa ukázalo, že Klotho zvyšuje povrchové množstvo TRPV5 odstránením konkrétnych koncových sialových kyselín na TRPV5 z ich glykánových reťazcov. Typické N-viazané glykány majú na svojich koncoch kyseliny sialové. Odstránenie koncových sialových kyselín vylučovaným proteínom Klotho odhaľuje základnú galaktózu alebo disacharid N -acetyllaktozamín. Tieto cukry sú ligandy pre galektín-1, lektín (proteín viažuci cukor), ktorý sa nachádza v extracelulárnej matrici. Väzba TRPV5 na galektín-1 pripútava TRPV5 na bunkový povrch a zabraňuje jeho endocytóze, čo vedie k akumulácii funkčného kanála na plazmatickej membráne ( obr. 3 ) [ 66 ]. Tento účinok Klotho predstavuje nový mechanizmus regulácie aktivity glykoproteínov bunkového povrchu.
Obrázok 3.
Nedávno bolo hlásené, že transmembránová forma Klotho viaže Na + , K + -ATPázu α1 podjednotku a zvyšuje jej množstvo na bunkovom povrchu v reakcii na zníženie extracelulárnej koncentrácie Ca2 + [ 69 ]. Hoci nie je známe, či Klotho modifikuje cukrové reťazce Na + , K + -ATPázy a1 podjednotky, ako to robí TRPV5, Klotho môže byť schopný regulovať prenos viacerých iónových kanálov prostredníctvom modifikácie ich cukrových reťazcov.
4.2.2. Potlačenie signalizácie inzulín/IGF-1
Klotho-deficientné myši sú hypoglykemické a extrémne citlivé na inzulín [ 21 , 47 ]. Naproti tomu transgénne myši s nadmernou expresiou Klotho sú stredne odolné voči inzulínu a IGF-1, hoci si udržiavajú normálnu hladinu glukózy v krvi nalačno a nie sú diabetické [ 22 ]. Tieto pozorovania naznačujú, že Klotho môže inhibovať signálnu dráhu inzulín/IGF-1. V skutočnosti má vylučovaný proteín Klotho aktivitu, ktorá inhibuje autofosforyláciu inzulínového receptora a receptora IGF-1 indukovanú inzulínom a IGF-1, keď sa aplikuje na kultivované bunky [ 8 , 22 ]. Hoci mechanizmus tejto aktivity zostáva ešte určiť, je možné, že secernovaný Klotho proteín môže modifikovať glykány inzulínových/IGF-1 receptorov, čo inhibuje ich aktivitu a/alebo mení abundanciu bunkového povrchu. Je potrebné poznamenať, že už desaťročia je známe, že ošetrenie kultivovaných buniek sialidázou indukuje inzulínovú rezistenciu [ 70 ]. Okrem toho sa u transgénnych myší, ktoré nadmerne exprimujú sialidázu (NEU3) na bunkovom povrchu, vyvinula intolerancia glukózy v dôsledku zvýšenej inzulínovej rezistencie[ 71 ]. Tieto pozorovania naznačujú potenciálne spojenie medzi inzulínovou rezistenciou a odstránením sialových kyselín z bunkového povrchu.
Schopnosť Klotho inhibovať signalizáciu inzulínu/IGF-1 môže súvisieť s vlastnosťami Klotho proti starnutiu, pretože početné línie genetických dôkazov naznačujú, že mierna inhibícia signálnej dráhy podobnej inzulínu je jedným z evolučne zachovaných mechanizmov na potlačenie starnutia. 72 ]. Nedávne štúdie ukázali, že zvýšená inzulínová rezistencia nemusí nutne znamenať cukrovku a krátky život. Skôr je čoraz jasnejšie, že adekvátne potlačenie signálnej dráhy podobnej inzulínu je evolučne zachovaným mechanizmom proti starnutiu a predĺženiu života. Je známe, že mutácie s redukciou funkcie v génoch kódujúcich ortológie inzulínového receptora, substráty inzulínového receptora (IRS) a PI3-kinázu predlžujú životnosť u C elegans a Drosophila [ 73 – 77 ]. U cicavcov sa zvýšená dĺžka života uvádza u myší bez inzulínového receptora v tukovom tkanive [ 78 ], u myší heterozygotných pre nulovú alelu génu pre receptor inzulínu podobného rastového faktora-1 (IGF-1) [ 79 ], u myší bez IRS-1 [ 80 ], myši bez IRS-2 v mozgu [ 81 ] a trpasličie myši s poruchou rastového hormónu endokrinná os (GH)-IGF-1 [ 23 – 25 ]. U ľudí niektorí storoční ľudia vykazujú rezistenciu voči IGF-1, krátkej postave a vysokému sérovému IGF-1 spojenému s mutáciami straty funkcie v géne receptora IGF-1 [ 82 ]. Dôležité je, že niektoré dlhoveké zvieratá vykazujú inzulínovú rezistenciu [ 80 ], čo naznačuje, že zvýšená citlivosť na inzulín nie je predpokladom pre dlhú životnosť a anti-aging. Hoci mnohé zvieratá s dlhým životom skutočne vykazujú zvýšenú citlivosť na inzulín, je vždy spojená s hypoinzulinémiou a oslabenou signalizačnou aktivitou inzulínu/IGF-1 v tkanivách. Zoslabená signalizačná aktivita inzulín/IGF-1 v tkanivách teda vykazuje užšiu súvislosť s predĺžením životnosti ako zvýšená citlivosť na inzulín, avšak presný mechanizmus tohto stavu ešte zostáva určiť.
4.2.3. Potlačenie oxidačného stresu
U C. elegans je predĺženie životnosti inhibíciou signalizácie podobnej inzulínu, ako je pozorované u mutantov daf-2 a age-1, závislé od forkhead transkripčného faktora daf-16 [ 83 ]. Forkhead transkripčné faktory sú negatívne regulované inzulínovou signalizáciou, čo naznačuje, že ich aktivácia hrá rozhodujúcu úlohu pri potláčaní starnutia spôsobeného inhibíciou inzulínovej signalizácie. Cicavčie homológy daf-16 sú transkripčné faktory Forkhead box O (FOXO), FOXO1, FOXO3a a FOXO4. Tieto FOXO sú tiež negatívne regulované signalizáciou inzulín/IGF-1 [ 84 ]: Aktivácia signalizácie inzulín/IGF-1 zvyšuje aktivitu serín-treonín kinázy Akt, ktorá následne fosforyluje FOXO. Fosforylované FOXO sú vylúčené z jadra a nie sú schopné fungovať ako transkripčné faktory. FOXO upregulujú expresiu viacerých cieľových génov, vrátane antioxidačných enzýmov, ako je kataláza a mitochondriálna mangán-superoxiddismutáza (SOD2) [ 85 ]. Kataláza a SOD2 detoxikujú peroxid vodíka a superoxid škodlivých reaktívnych foriem kyslíka (ROS) a znižujú oxidačný stres. Aktivácia FOXO inhibíciou signalizácie inzulínu/IGF-1 teda môže zvýšiť bunkovú ochranu pred oxidačným stresom a môže prispieť k potlačeniu starnutia.
Transgénne myši s nadmernou expresiou Klotho majú vyššiu expresiu SOD2 vo svaloch a menej fosforylovaných FOXO ako myši divokého typu, čo je spojené s menším oxidačným stresom, čo dokazujú nižšie hladiny močového 8-OHdG, markera oxidačného poškodenia DNA [ 86 ]. Okrem toho transgénne myši s nadmernou expresiou Klotho prežijú subletálnu dávku paraquatu, herbicídu, ktorý generuje superoxid, výrazne dlhšie ako myši divokého typu, čo naznačuje, že nadmerná expresia Klotho vyvoláva odolnosť voči oxidačnému stresu. Okrem toho ošetrenie kultivovaných buniek secernovaným proteínom Klotho inhibuje signalizáciu inzulín/IGF-1, aktivuje FOXO, indukuje expresiu SOD2 a znižuje oxidačné poškodenie a apoptózu indukovanú paraquatom [ 86 ] alebo peroxidom vodíka [ 87 ]. Zostáva určiť, či schopnosť Klotho znižovať oxidačný stres primárne závisí od up-regulácie antioxidačných enzýmov.
Oxidačný stres sa podieľa na patogenéze rôznych chorobných stavov vrátane ischémie a zápalu. Ak Klotho dokáže zmierniť oxidačný stres, Klotho môže chrániť tkanivá pred ischémiou a zápalom. Expresia Klotho bola významne potlačená v obličkách vystavených experimentálnemu ischemicko-reperfúznemu poškodeniu. Adenovírusom sprostredkovaná transdukcia Klotho expresie však zabránila ischemickému poškodeniu obličiek a rozvoju akútneho zlyhania obličiek [ 88 ]. V inej správe transgénna nadmerná expresia Klotho v myšom modeli glomerulomefritídy obnovila mitochondriálnu funkciu a potlačila poškodenie mitochondriálnej DNA v obličkách. Potlačil tiež zrýchlenú bunkovú senescenciu a apoptózu spojenú s glomerulonefritídou, čo viedlo k zachovaniu funkcie obličiek a zlepšeniu prežitia [ 89 ]. Tieto pozorovania naznačujú, že Klotho môže vyvolať odolnosť voči oxidačnému stresu a chrániť tkanivá pred oxidačným poškodením.
4.2.4. Produkcia oxidu dusnatého
Oxid dusnatý (NO) sa podieľa na regulácii cievneho tonusu. Vazodilatácia závislá od endotelu v reakcii na acetylcholín je oslabená v aorte a arteriolách myší s deficitom Klotho, čo naznačuje, že nedostatok Klotho spôsobuje zníženie syntézy NO vo vaskulárnych endotelových bunkách [ 90 ]. V súlade s týmto zistením vykazujú myši s deficitom Klotho zhoršenú angiogenézu, ktorá je závislá od NO odvodeného od endotelu [ 91 ]. Systémová syntéza NO je tiež znížená u myší s deficitom Klotho, ako je stanovené vylučovaním metabolitov NO močom [ 90 ]. Dôležité je, že defekty v syntéze NO pozorované u myší s deficitom Klotho nie sú sekundárne k hyperfosfatémii alebo hypervitaminóze D. pretože klotho heterozygotné myši s normálnymi hladinami fosfátu a vitamínu D v krvi majú tiež mierne defekty v syntéze NO. Okrem toho parabióza (chirurgické spojenie dvoch zvierat na umožnenie výmeny humorálnych faktorov) medzi klotho heterozygotnými myšami a myšami divokého typu obnovuje acetylcholínom indukovanú vazodilatáciu u klotho heterozygotných myší, čo naznačuje zapojenie humorálneho faktora (faktorov) do aktivity Klotho proteínu ktorý zachováva syntézu NO [ 90 ]. Okrem toho in vivo dodanie génu Klotho pomocou adenovírusového expresného vektora zvyšuje syntézu NO závislú od endotelu v potkanom modeli viacerých aterogénnych rizikových faktorov [ 92 ]. Mechanizmus regulácie syntézy NO pomocou Klotho zostáva určiť.
4.2.5. Potlačenie signalizácie Wnt
Nedávno bolo publikované, že secernovaný Klotho proteín sa viaže na viaceré Wnt ligandy a inhibuje ich schopnosť aktivovať Wnt signalizáciu, potenciálne prostredníctvom zabránenia väzby Wnt na jeho príbuzný bunkový povrchový receptor [ 93 ]. Aj keď je aktivácia Wnt signalizácie nevyhnutná pre proliferáciu a prežitie kmeňových buniek, nepretržitá aktivácia Wnt signalizácie môže spôsobiť rýchle vyčerpanie a vyčerpanie kmeňových buniek [ 94 , 95 ]. Pretože dysfunkcia kmeňových buniek obmedzuje regeneráciu tkaniva a potenciálne ovplyvňuje procesy starnutia, schopnosť vylučovaného proteínu Klotho inhibovať signalizáciu Wnt môže prispieť k fenotypom podobným starnutiu u myší s deficitom Klotho. Koža myší s deficitom Klotho má znížený počet epidermálnych kmeňových buniek vo vlasových folikuloch. Tieto epidermálne kmeňové bunky vykazujú vyššiu signalizačnú aktivitu Wnt a vyššiu expresiu endogénneho markera starnutia buniek (SAp-galaktozidáza) ako bunky u myší divokého typu, čo naznačuje, že nedostatok Klotho spôsobil nepretržitú aktiváciu signalizácie Wnt a starnutie kmeňových buniek. Znížený počet epidermálnych kmeňových buniek môže tiež vysvetliť zhoršenie hojenia rán u myší s deficitom Klotho. Kostný fenotyp u Klotho-deficientných myší [ 14 , 96 ] možno tiež čiastočne pripísať zmenenej Wnt signalizácii. Klotho-deficientné myši vykazujú zníženú hrúbku kortikálnej kosti spojenú s paradoxne zvýšenou trabekulárnou kosťou v metafýze holennej kosti, kde je signalizácia Wnt selektívne zvýšená v porovnaní s myšami divokého typu. Pretože signalizácia Wnt podporuje proliferáciu / prežitie osteoblastov, selektívne zvýšenie signalizácie Wnt môže vysvetliť, prečo myši s deficitom Klotho majú zvýšenú kosť iba v trabekulárnej kosti.
Bolo publikované, že μ-calpain, vápnik-dependentná proteáza, ktorá štiepi rôzne bunkové proteíny vrátane β-katenínu, bol významne aktivovaný v tkanivách myší s deficitom Klotho [ 97 ]. Aktivácia Wnt signalizácie indukuje akumuláciu cytoplazmatického β-katenínu, ktorý sa následne translokuje do jadra a interaguje s transkripčnými faktormi rodiny T bunkových faktorov (TCF), aby reguloval expresiu ich cieľových génov. Hoci cytoplazmatický β-katenín je primárne degradovaný ubikvitináciou, po ktorej nasleduje proteazomálna degradácia, nedávne štúdie ukázali, že calpain, aktivovaný uvoľňovaním vápnika z intracelulárnych zásob, sa tiež podieľa na degradácii β-katenínu [ 98 ]. Aktivácia calpainu u myší s deficitom Klotho môže byť sekundárnou odpoveďou na rozšírenú Wnt signalizáciu u týchto zvierat. β-katenín sa môže viazať nielen na TCF, ale aj na FOXO a zvyšuje ich transkripčnú aktivitu [ 99 ]. Interakcia medzi β-katenínom a FOXO sa zvyšuje v bunkách pod oxidačným stresom, čo potenciálne posúva β-katenín z TCF na FOXO a vyvoláva zastavenie bunkového cyklu a opravu DNA [ 100 ]. Pochopenie vzťahu medzi Klotho, oxidačným stresom, FOXO a β-katenínom môže byť novým cieľom výskumu v oblasti starnutia, rakoviny a biológie kmeňových buniek.
4.2.6. Klotho ako supresor rakoviny prsníka
Rozsiahle klinické a laboratórne údaje naznačujú kritickú úlohu signalizácie inzulínu/IGF-1 pri rakovine prsníka. Predovšetkým: 1) zvýšené hladiny inzulínu v sére sú spojené s nepriaznivou prognózou rakoviny prsníka [ 101 ]; 2) Vysoké hladiny cirkulujúceho IGF-1 sú spojené so zvýšeným rizikom premenopauzálneho karcinómu prsníka [ 102 ]; a 3) Inhibícia signalizácie inzulín/IGF-1 inhibuje rast buniek rakoviny prsníka [ 103 ]. Keďže vylučovaný proteín Klotho inhibuje aktiváciu inzulínových/IGF-1 receptorov, Klotho môže fungovať ako supresor rakoviny prsníka. V súlade s touto predstavou imunohistochemická analýza polí ľudského prsného tkaniva ukázala, že normálne prsné epitelové bunky exprimujú Klotho proteín, zatiaľ čo jeho expresia je významne znížená alebo stratená pri duktálnom karcinóme in situ a invazívnom duktálnom karcinóme [ 8 ]. Okrem toho niekoľko línií experimentálnych dôkazov podporuje názor, že Klotho funguje ako supresor nádorov. 1) Nútená expresia Klotho v bunkových líniách rakoviny prsníka znižuje ich proliferáciu. 2) Zníženie endogénnej expresie Klotho v bunkách rakoviny prsníka MCF-7 podporuje ich proliferáciu. 3) Nútená expresia Klotho v bunkách MCF-7 zoslabuje IGF-1-indukovanú fosforyláciu IGF-1 receptora, IRS-1, AKT1 a ERK. Podobné účinky sa pozorovali, keď sa bunky MCF-7 ošetrili rekombinantným vylučovaným proteínom Klotho. 4) Knockdown endogénneho Klotho v MCF-7 bunkách zvýšil IGF-1-indukovanú AKT fosforyláciu. 5) Inhibícia IGF-1 signalizácie pomocou Klotho zvýšila expresiu proteínov viažucich CCAAT/enhancer (C/EBP) [ 8 ]. Je známe, že tieto transkripčné faktory sú down-regulované IGF-1 a sú identifikované ako supresory rastu rakoviny prsníka [ 104 ]. Všetky tieto pozorovania sú v súlade s hypotézou, že Klotho môže byť supresorom rakoviny prsníka. Zostáva určiť, či aktivita Klotho proti rakovine prsníka závisí predovšetkým od jeho schopnosti potlačiť signalizáciu IGF-1 alebo od iných neznámych mechanizmov.
4.2.7. Polymorfizmus a mutácie ľudského génu KLOTHO
Funkčný variant ľudského proteínu Klotho obsahuje šesť sekvenčných variácií v úplnej väzbovej nerovnováhe, z ktorých dve vedú k substitúciám aminokyselín F352V a C370S. F (fenylalanín) v tejto polohe je vysoko konzervovaný medzi β-glukozidázami rôznych druhov a jeho substitúcia za V (valín) môže zmeniť vylučovanie a enzymatickú aktivitu proteínu [ 105 ]. Je zaujímavé, že heterozygoti pre tento variant majú výhodu pre dlhovekosť, zatiaľ čo homozygoti sú nevýhodní z hľadiska prežitia, pretože homozygoti sú výrazne nedostatočne zastúpení vo veku [ 105 ]. Na rozdiel od toho majú heterozygoti dlhšiu životnosť ako divoké typy vo viacerých populáciách, čo naznačuje, že variácia génu KLOTHO ovplyvňuje dĺžku ľudského života. Okrem toho je homozygotnosť tohto variantu spojená s tradičnými kardiovaskulárnymi rizikovými faktormi vrátane cholesterolu s nízkou hustotou lipoproteínov a vysokého systolického krvného tlaku a je novo identifikovaná ako nezávislý rizikový faktor mŕtvice a skorého nástupu ochorenia koronárnych artérií. Na rozdiel od toho je heterozygotnosť spojená s nižším rizikom cievnej mozgovej príhody a ischemickej choroby srdca, čo je v súlade s jej asociáciou s dlhou životnosťou [ 106 , 107 ]. Okrem tohto variantu KLOTHO je niekoľko jednonukleotidových polymorfizmov (SNP) spojených s minerálnou hustotou kostí [ 108 – 111 ], metabolizmom glukózy [ 112 ] a kognitívnymi funkciami [ 113 ]
Nedávno boli hlásení dvaja pacienti nesúci mutácie v géne KLOTHO . Jedným je 13-ročné dievča, ktoré vykazuje kalcifikáciu mäkkých tkanív a ciev so zvýšenou hladinou fosfátu, vápnika, vitamínu D a FGF23 v krvi a je nositeľom mutácie straty funkcie v géne KLOTHO (H193R) [ 114 ]. Mutantný proteín Klotho má zníženú schopnosť vytvárať stabilný komplex s receptormi FGF. Hoci pacientovi už bola predpísaná diéta s nízkym obsahom fosfátov a viazačov fosfátov a nevykazuje žiadne ďalšie znaky predčasného starnutia, sledovanie tohto pacienta môže poskytnúť cenné informácie o účinkoch Klotho na znaky citlivé na vek u ľudí. Druhou je 23-ročná pacientka s hypofosfatemickou krivicou a hyperparatyreózou. Má translokáciu s bodom zlomu v blízkosti génu KLOTHO , ktorý je spojený so zvýšenou sérovou hladinou vylučovaného proteínu Klotho. Zostáva určiť, prečo vysoká hladina Klotho v sére spôsobuje hyperparatyreózu.
5. Záverečné poznámky
Objav génu klotho viedol k identifikácii viacerých nových endokrinných osí sprostredkovaných endokrinnými FGF a Klothos, ktoré regulujú rôzne metabolické procesy. Transmembránová forma proteínu Klotho funguje ako koreceptor pre FGF23 a reguluje metabolizmus fosfátu, vápnika a vitamínu D. Extracelulárna doména proteínu Klotho sa uvoľňuje a vylučuje do systémového obehu, kde funguje ako endokrinný faktor. Vylučovaný proteín Klotho riadi viaceré iónové kanály a signálne dráhy rastového faktora vrátane inzulínu, IGF-1 a Wnt, ktoré sa potenciálne podieľajú na biológii rakoviny a kmeňových buniek. Identifikácia spoločného molekulárneho základu pre tieto viacnásobné funkcie Klotho bude obzvlášť dôležitá pre pochopenie vlastností Klotho proti starnutiu.
Poznámky pod čiarou
Vyhlásenie vydavateľa: Toto je súbor PDF s neupraveným rukopisom, ktorý bol prijatý na publikovanie. Ako službu našim zákazníkom poskytujeme túto skorú verziu rukopisu. Rukopis bude pred publikovaním v konečnej citovateľnej podobe podrobený kopírovaniu, sadzbe a kontrole výsledného korektúry. Vezmite prosím na vedomie, že počas výrobného procesu sa môžu objaviť chyby, ktoré by mohli ovplyvniť obsah, a vzťahujú sa naň všetky právne obmedzenia, ktoré sa vzťahujú na časopis.
Referencie
- 1.Kuro-o M, Matsumura Y, Aizawa H a kol. Mutácia myšacieho génu klotho vedie k syndrómu pripomínajúcemu starnutie. Príroda. 1997;390:45–51. doi: 10.1038/36285. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 2.Kuro-o M, Hanaoka K, Hiroi Y, a kol. Hypertenzia citlivá na soľ u transgénnych myší nadmerne exprimujúcich Na(+)-protónový výmenník. Circ Res. 1995;76:148–153. doi: 10.1161/01.res.76.1.148. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 3.Matsumura Y, Aizawa H, Shiraki-Iida T, Nagai R, Kuro-o M, Nabeshima Y. Identifikácia ľudského génu klotho a jeho dvoch transkriptov kódujúcich membránu a vylučovaný proteín klotho. Biochem Biophys Res Commun. 1998;242:626–630. doi: 10.1006/bbrc.1997.8019. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 4.Shiraki-Iida T, Aizawa H, Matsumura Y, a kol. Štruktúra myšacieho génu klotho a jeho dvoch transkriptov kódujúcich membránu a secernovaný proteín. FEBS Lett. 1998;424:6–10. doi: 10.1016/s0014-5793(98)00127-6. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 5.Mian JE. Sekvenčné, štrukturálne, funkčné a fylogenetické analýzy troch rodín glykozidáz. Blood Cells Mol Dis. 1998;24:83–100. doi: 10.1006/bcmd.1998.9998. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 6.Ben-Dov IZ, Galitzer H, Lavi-Moshayoff V, a kol. Prištítne telieska sú cieľovým orgánom pre FGF23 u potkanov. J Clin Invest. 2007;117:4003–4008. doi: 10.1172/JCI32409. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 7.Kamemori M, Ohyama Y, Kurabayashi M, Takahashi K, Nagai R, Furuya N. Expresia proteínu Klotho vo vnútornom uchu. Vypočujte si Res. 2002;171:103–110. doi: 10.1016/s0378-5955(02)00483-5. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 8.Wolf I, Levanon-Cohen S, Bose S, a kol. Klotho: nádorový supresor a modulátor dráh IGF-1 a FGF pri ľudskej rakovine prsníka. Onkogén. 2008;27:7094–7105. doi: 10.1038/onc.2008.292. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 9.Tsujikawa H, Kurotaki Y, Fujimori T, Fukuda K, Nabeshima Y. Klotho, gén súvisiaci so syndrómom pripomínajúcim ľudské predčasné starnutie, funguje v negatívnom regulačnom okruhu endokrinného systému vitamínu D. Mol Endocrinol. 2003;17:2393–2403. doi: 10.1210/me.2003-0048. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 10.Toyama R, Fujimori T, Nabeshima Y, Itoh Y, Tsuji Y, Osamura RY. Zhoršená regulácia gonadotropínov vedie k atrofii ženského reprodukčného systému u myší s deficitom klotho. Endokrinológia. 2006;147:120–129. doi: 10.1210/en.2005-0429. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 11.Min D, Panoskaltsis-Mortari A, Kuro-o M, Hollander GA, Blazar BR, Weinberg KI. Trvalá tymopoéza a zlepšenie funkčnej imunity indukovanej exogénnym podávaním KGF v myších modeloch starnutia. Krv. 2007;109:2529–2537. doi: 10.1182/krv-2006-08-043794. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 12.Yoshida T, Fujimori T, Nabeshima Y. Sprostredkovanie nezvyčajne vysokých koncentrácií 1,25-dihydroxyvitamínu D u homozygotných klotho mutantných myší zvýšenou expresiou renálneho génu 1alfa-hydroxylázy. Endokrinológia. 2002;143:683–689. doi: 10.1210/endo.143.2.8657. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 13.Kawaguchi H, Manabe N, Miyaura C, Chikuda H, Nakamura K, Kuro-o M. Nezávislé poškodenie diferenciácie osteoblastov a osteoklastov u klotho myši vykazujúcej osteopéniu s nízkym obratom. J Clin Invest. 1999;104:229–237. doi: 10.1172/JCI5705. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 14.Yamashita T, Nifuji A, Furuya K, Nabeshima Y, Noda M. Predĺženie epifyzárnej trabekulárnej kosti u transgénnych myší nesúcich mutáciu lokusu génu klotho, ktorá vedie k syndrómu pripomínajúcemu starnutie. J Endocrinol. 1998;159:1–8. doi: 10.1677/joe.0.1590001. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 15.Yamashita T, Yamashita M, Noda M, Nabeshima Y. Mikropočítačová tomografia s vysokým rozlíšením analýzy abnormálnych štruktúr trabekulárnej kosti u myší s mutantom génu klotho. J Endocrinol. 2000;164:239–245. doi: 10.1677/joe.0.1640239. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 16.Suga T, Kurabayashi M, Sando Y a kol. Narušenie génu klotho spôsobuje u myší pľúcny emfyzém. Porucha zachovania integrity pľúc počas postnatálneho života. Am J Respir Cell Mol Biol. 2000;22:26–33. doi: 10.1165/ajrcmb.22.1.3554. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 17.Sato A, Hirai T, Imura A, a kol. Morfologický mechanizmus vývoja pľúcneho emfyzému u klotho myší. Proc Natl Acad Sci US A. 2007;104:2361–2365. doi: 10.1073/pnas.0607882104. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 18.Nagai T, Yamada K, Kim HC a kol. Zhoršenie kognície v genetickom modeli starnúcich myší s mutantným génom klotho: úloha oxidačného stresu. Faseb J. 2003;17:50–52. doi: 10.1096/fj.02-0448fje. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 19.Anamizu Y, Kawaguchi H, Seichi A, a kol. Klotho insuficiencia spôsobuje zníženie transkripčnej aktivity génu ribozomálnej RNA, cytoplazmatickej RNA a drsnej ER v bunkách predného rohu miechy. Acta Neuropathol (Berl) 2005;109:457–466. doi: 10.1007/s00401-004-0971-7. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 20.Lin MT, Beal MF. Mitochondriálna dysfunkcia a oxidačný stres pri neurodegeneratívnych ochoreniach. Príroda. 2006;443:787–795. doi: 10.1038/nature05292. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 21.Utsugi T, Ohno T, Ohyama Y a kol. Znížená produkcia inzulínu a zvýšená citlivosť na inzulín u klotho mutantnej myši, nového zvieracieho modelu pre ľudské starnutie. Metabolizmus. 2000;49:1118–1123. doi: 10.1053/meta.2000.8606. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 22.Kurosu H, Yamamoto M, Clark JD a kol. Potlačenie starnutia u myší pomocou hormónu Klotho. Veda. 2005;309:1829–1833. doi: 10.1126/science.1112766. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 23.Brown-Borg HM, Borg KE, Meliska CJ, Bartke A. Trpasličí myši a proces starnutia [list] Nature. 1996;384:33. doi: 10.1038/384033a0. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 24.Flurkey K, Papaconstantinou J, Harrison DE. Snellova trpasličia mutácia Pit1(dw) môže predĺžiť životnosť myší. Mech Aging Dev. 2002;123:121–130. doi: 10.1016/s0047-6374(01)00339-6. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 25.Bartke A, Brown-Borg H. Predĺženie života u trpasličej myši. Curr Top Dev Biol. 2004;63:189–225. doi: 10.1016/S0070-2153(04)63006-7. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 26.Masuda H, Chikuda H, Suga T, Kawaguchi H, Kuro-o M. Regulácia viacerých fenotypov podobných starnutiu indukovateľnou expresiou génu klotho u mutantných myší klotho. Mech Aging Dev. 2005;126:1274–1283. doi: 10.1016/j.mad.2005.07.007. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 27.Duce JA, Podvin S, Hollander W, Kipling D, Rosene DL, Abraham ČR. Analýza génového profilu naznačuje, že Klotho je dôležitým prispievateľom k zmenám starnutia v bielej hmote mozgu opice rhesus. Glia. 2008;56:106–117. doi: 10.1002/glia.20593. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 28.Chen CD, Podvin S, Gillespie E, Leeman SE, Abraham ČR. Inzulín stimuluje štiepenie a uvoľňovanie extracelulárnej domény Klotho pomocou ADAM10 a ADAM17. Proc Natl Acad Sci US A. 2007;104:19796–19801. doi: 10.1073/pnas.0709805104. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 29.Imura A, Iwano A, Tohyama O, a kol. Vylučovaný proteín Klotho v sére a CSF: implikácia pre posttranslačné štiepenie pri uvoľňovaní proteínu Klotho z bunkovej membrány. FEBS Lett. 2004;565:143–147. doi: 10.1016/j.febslet.2004.03.090. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 30.Schiavi SC, Kumar R. Fosfatonínová dráha: nové poznatky o homeostáze fosfátov. Kidney Int. 2004;65:1–14. doi: 10.1111/j.1523-1755.2004.00355.x. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 31.Dusso AS, Brown AJ, Slatopolsky E. Vitamin D. Am J Physiol Renal Physiol. 2005;289:F8–28. doi: 10.1152/ajprenal.00336.2004. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 32.Berndt T, Kumar R. Fosfatoníny a regulácia homeostázy fosfátov. Annu Rev Physiol. 2007;69:341–359. doi: 10.1146/annurev.physiol.69.040705.141729. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 33.Kuro-o M. Klotho ako regulátor signalizácie fibroblastového rastového faktora a metabolizmu fosfátu/vápnika. Curr Opin Nephrol Hypertens. 2006;15:437–441. doi: 10.1097/01.mnh.0000232885.81142.83. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 34.White KE, Evans WE, O’Rlordan JLH a kol. Autozomálne dominantná hypofosfatemická rachitída je spojená s mutáciami v FGF23. Nat Genet. 2000;26:345–348. doi: 10.1038/81664. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 35.Hádky LD. Regulácia fosfátovej homeostázy a mineralizácie skeletu FGF23, PHEX a MEPE. Am J Physiol Endocrinol Metab. 2003;285:E1–9. doi: 10.1152/ajpendo.00016.2003. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 36.Saito H, Maeda A, Ohtomo S, a kol. Cirkulujúci FGF-23 je regulovaný 1alfa,25-dihydroxyvitamínom D3 a fosforom in vivo. J Biol Chem. 2005;280:2543–2549. doi: 10.1074/jbc.M408903200. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 37.Liu S, Tang W, Zhou J, a kol. Fibroblastový rastový faktor 23 je kontraregulačný fosfaturový hormón pre vitamín D. J Am Soc Nephrol. 2006;17:1305–1315. doi: 10.1681/ASN.2005111185. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 38.Liu S, Gupta A, Quarles LD. Vznikajúca úloha fibroblastového rastového faktora 23 v osi kosti-obličky regulujúcej systémovú fosfátovú homeostázu a mineralizáciu extracelulárnej matrice. Curr Opin Nephrol Hypertens. 2007;16:329–335. doi: 10.1097/MNH.0b013e3281ca6ffd. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 39.Shimada T, Kakitani M, Yamazaki Y a kol. Cielená ablácia Fgf23 demonštruje zásadnú fyziologickú úlohu FGF23 v metabolizme fosfátov a vitamínu D. J Clin Invest. 2004;113:561–568. doi: 10.1172/JCI19081. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 40.Yu X, Biela KE. FGF23 a poruchy homeostázy fosfátov. Cytokine Growth Factor Rev. 2005;16:221–232. doi: 10.1016/j.cytogfr.2005.01.002. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 41.Yu X, Ibrahimi OA, Goetz R a kol. Analýza biochemických mechanizmov pre endokrinné účinky fibroblastového rastového faktora-23. Endokrinológia. 2005;146:4647–4656. doi: 10.1210/en.2005-0670. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 42.Zhang X, Ibrahimi OA, Olsen SK, Umemori H, Mohammadi M, Ornitz DM. Receptorová špecifickosť rodiny fibroblastových rastových faktorov. Kompletná cicavčia rodina FGF. J Biol Chem. 2006;281:15694–15700. doi: 10.1074/jbc.M601252200. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 43.Kurosu H, Ogawa Y, Miyoshi M a kol. Regulácia signalizácie fibroblastového rastového faktora-23 pomocou klotho. J Biol Chem. 2006;281:6120–6123. doi: 10.1074/jbc.C500457200. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 44.Urakawa I, Yamazaki Y, Shimada T a kol. Klotho konvertuje kanonický receptor FGF na špecifický receptor pre FGF23. Príroda. 2006;444:770–774. doi: 10.1038/nature05315. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 45.Krajisnik T, Bjorklund P, Marsell R, et al. Fibroblastový rastový faktor-23 reguluje expresiu parathormónu a 1alfa-hydroxylázy v kultivovaných bunkách prištítnych teliesok hovädzieho dobytka. J Endocrinol. 2007;195:125–131. doi: 10.1677/JOE-07-0267. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 46.Shimada T, Hasegawa H, Yamazaki Y a kol. FGF-23 je silný regulátor metabolizmu vitamínu D a homeostázy fosfátov. J Bone Miner Res. 2004;19:429–435. doi: 10.1359/JBMR.0301264. Epub 2003 december 2029. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 47.Hesse M, Frohlich LF, Zeitz U, Lanske B, Erben RG. Ablácia signalizácie vitamínu D zachraňuje homeostázu kostí, minerálov a glukózy u myší s deficitom Fgf-23. Matrix Biol. 2007;26:75–84. doi: 10.1016/j.matbio.2006.10.003. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 48.Morishita K, Shirai A, Kubota M a kol. Progresia starnutia u klotho mutantných myší môže byť modifikovaná diétnym fosforom a zinkom. J Nutr. 2001;131:3182–3188. doi: 10.1093/jn/131.12.3182. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 49.Segawa H, Yamanaka S, Ohno Y a kol. Korelácia medzi hyperfosfatémiou a aktivitou kotransportéra Na-Pi typu II u klotho myší. Am J Physiol Renálny Physiol. 2007;292:F769–779. doi: 10.1152/ajprenal.00248.2006. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 50.Razzaque MS, Sitara D, Taguchi T, St-Arnaud R, Lanske B. Fenotyp predčasného starnutia u myší s nulovým rastovým faktorom 23 fibroblastov je proces sprostredkovaný vitamínom D. Faseb J. 2006;20:720–722. doi: 10.1096/fj.05-5432fje. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 51.Stubbs JR, Liu S, Tang W a kol. Úloha hyperfosfatémie a 1,25-dihydroxyvitamínu D pri vaskulárnej kalcifikácii a mortalite u myší s nulovým fibroblastickým rastovým faktorom 23. J Am Soc Nephrol. 2007;18:2116–2124. doi: 10.1681/ASN.2006121385. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 52.Medici D, Razzaque MS, Deluca S, a kol. Signalizácia FGF-23-Klotho stimuluje proliferáciu a zabraňuje apoptóze vyvolanej vitamínom D. J Cell Biol. 2008;182:459–465. doi: 10.1083/jcb.200803024. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 53.Itoh N, Ornitz DM. Evolúcia génových rodín Fgf a Fgfr. Trends Genet. 2004;20:563–569. doi: 10.1016/j.tig.2004.08.007. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 54.Inagaki T, Choi M, Moschetta A, a kol. Fibroblastový rastový faktor 15 funguje ako enterohepatický signál na reguláciu homeostázy žlčových kyselín. Cell Metab. 2005;2:217–225. doi: 10.1016/j.cmet.2005.09.001. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 55.Choi M, Moschetta A, Bookout AL, a kol. Identifikácia hormonálneho základu pre plnenie žlčníka. Nat Med. 2006;12:1253–1255. doi: 10,1038/nm1501. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 56.Kharitonenkov A, Shiyanova TL, Koester A, a kol. FGF-21 ako nový metabolický regulátor. J Clin Invest. 2005;115:1627–1635. doi: 10.1172/JCI23606. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 57.Inagaki T, Dutchak P, Zhao G, a kol. Endokrinná regulácia odozvy nalačno indukciou fibroblastového rastového faktora sprostredkovanou PPARalfa 21. Bunkový metabolizmus. 2007;5:415–425. doi: 10.1016/j.cmet.2007.05.003. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 58.Ito S, Kinoshita S, Shiraishi N, a kol. Molekulárne klonovanie a analýzy expresie myšieho betaklotho, ktorý kóduje nový proteín rodiny Klotho. Mech Dev. 2000;98:115–119. doi: 10.1016/s0925-4773(00)00439-1. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 59.Kurosu H, Choi M, Ogawa Y a kol. Tkanivovo špecifická expresia izoforiem betaKlotho a fibroblastového rastového faktora (FGF) určuje metabolickú aktivitu FGF19 a FGF21. J Biol Chem. 2007;282:26687–26695. doi: 10.1074/jbc.M704165200. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 60.Ito S, Fujimori T, Furuya A, Satoh J, Nabeshima Y, Nabeshima Y. Zhoršená negatívna spätná väzba potlačenia syntézy žlčových kyselín u myší, ktorým chýba betaKlotho. J Clin Invest. 2005;115:2202–2208. doi: 10.1172/JCI23076. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 61.Yu C, Wang F, Kan M a kol. Zvýšený metabolizmus cholesterolu a syntéza žlčových kyselín u myší, ktorým chýba membránový tyrozínkinázový receptor FGFR4. J Biol Chem. 2000;275:15482–15489. doi: 10.1074/jbc.275.20.15482. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 62.Kurosu H, Kuro-o M. Rodina génov Klotho a rastové faktory endokrinných fibroblastov. Mol Cell Endocrinol. 2008 doi: 10.1016/j.mce.2008.10.052. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 63.Kurosu H, Kuro-o M. Rodina génov Klotho a rastové faktory endokrinných fibroblastov. Curr Opin Nephrol Hypertens. 2008;17:368–372. doi: 10.1097/MNH.0b013e3282ffd994. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 64.Kuro-o M. Endokrinné FGF a Klothos: vznikajúce koncepty. Trendy Endocrinol Metab. 2008;19:239–245. doi: 10.1016/j.tem.2008.06.002. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 65.Tohyama O, Imura A, Iwano A, a kol. Klotho je nová beta-glukuronidáza schopná hydrolyzovať steroidné beta-glukuronidy. J Biol Chem. 2004;279:9777–9784. doi: 10.1074/jbc.M312392200. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 66.Cha SK, Ortega B, Kurosu H, Rosenblatt KP, Kuro-o M, Huang CL. Odstránenie kyseliny sialovej zahŕňajúce Klotho spôsobuje retenciu kanála TRPV5 na bunkovom povrchu prostredníctvom väzby na galektín-1. Proc Natl Acad Sci US A. 2008;105:9805–9810. doi: 10.1073/pnas.0803223105. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 67.Chang Q, Hoefs S, van der Kemp AW, Topala CN, Bindels RJ, Hoenderop JG. Beta-glukuronidáza klotho hydrolyzuje a aktivuje TRPV5 kanál. Veda. 2005;310:490–493. doi: 10.1126/science.1114245. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 68.Hoenderop JG, Nilius B, Bindels RJ. Absorpcia vápnika cez epitel. Physiol Rev. 2005;85:373–422. doi: 10.1152/physrev.00003.2004. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 69.Imura A, Tsuji Y, Murata M, a kol. alfa-Klotho ako regulátor homeostázy vápnika. Veda. 2007;316:1615–1618. doi: 10.1126/science.1135901. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 70.Salhanick AI, Amatruda JM. Úloha kyseliny sialovej v účinku inzulínu a inzulínovej rezistencii diabetes mellitus. Am J Physiol. 1988;255:E173–179. doi: 10.1152/ajpendo.1988.255.2.E173. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 71.Sasaki A, Hata K, Suzuki S, a kol. Nadmerná expresia sialidázy spojenej s plazmatickou membránou zoslabuje inzulínovú signalizáciu u transgénnych myší. J Biol Chem. 2003;278:27896–27902. doi: 10.1074/jbc.M212200200. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 72.Tatar M, Bartke A, Antebi A. Endokrinná regulácia starnutia pomocou signálov podobných inzulínu. Veda. 2003;299:1346–1351. doi: 10.1126/science.1081447. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 73.Kenyon C. The Plasticity of Aging: Insights from Long-Lid Mutants. Cell. 2005;120:449–460. doi: 10.1016/j.cell.2005.02.002. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 74.Kenyon C, Chang J, Gensch E, Rudner A, Tabtiang R. A C. mutant elegans, ktorý žije dvakrát dlhšie ako divoký typ. Príroda. 1993;366:461–464. doi: 10.1038/366461a0. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 75.Morris JZ, Tissenbaum HA, Ruvkun G. Člen rodiny fosfatidylinozitol-3-OH kináz regulujúci dlhovekosť a diapauzu u Caenorhabditis elegans. prírody. 1996;382:536–539. doi: 10.1038/382536a0. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 76.Tatar M, Kopelman A, Epstein D, Tu MP, Yin CM, Garofalo RS. Homológ mutantného inzulínového receptora Drosophila, ktorý predlžuje životnosť a zhoršuje neuroendokrinnú funkciu. Veda. 2001;292:107–110. doi: 10.1126/science.1057987. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 77.Clancy DJ, Gems D, Harshman LG a spol. Predĺženie životnosti stratou CHICO, substrátového proteínu inzulínového receptora Drosophila. Veda. 2001;292:104–106. doi: 10.1126/science.1057991. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 78.Bluher M, Kahn BB, Kahn ČR. Predĺžená životnosť u myší, ktorým chýba inzulínový receptor v tukovom tkanive. Veda. 2003;299:572–574. doi: 10.1126/science.1078223. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 79.Holzenberger M, Dupont J, Ducos B a kol. Receptor IGF-1 reguluje dĺžku života a odolnosť voči oxidačnému stresu u myší. Príroda. 2003;421:182–187. doi: 10.1038/nature01298. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 80.Selman C, Lingard S, Choudhury AI a kol. Dôkaz predĺženia životnosti a oneskorených biomarkerov súvisiacich s vekom u myší s nulovým substrátom inzulínového receptora 1. FASEB J. 2008;22:807–818. doi: 10.1096/fj.07-9261com. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 81.Taguchi A, Wartschow LM, White MF. Signalizácia IRS2 mozgu koordinuje dĺžku života a homeostázu živín. Veda. 2007;317:369–372. doi: 10.1126/science.1142179. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 82.Suh Y, Atzmon G, Cho MO a kol. Funkčne významné mutácie receptora rastového faktora I podobného inzulínu u storočných ľudí. Proc Natl Acad Sci US A. 2008;105:3438–3442. doi: 10.1073/pnas.0705467105. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 83.Ogg S, Paradis S, Gottlieb S, a kol. Transkripčný faktor hlavy vidlice DAF-16 prenáša u C. elegans metabolické signály podobné inzulínu a signály dlhovekosti. Príroda. 1997;389:994–999. doi: 10.1038/40194. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 84.Brunet A, Bonni A, Zigmond MJ a kol. Akt podporuje prežitie buniek fosforyláciou a inhibíciou transkripčného faktora Forkhead. Cell. 1999;96:857–868. doi: 10.1016/s0092-8674(00)80595-4. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 85.Kops GJ, Dansen TB, Polderman PE a kol. Forkhead transkripčný faktor FOXO3a chráni pokojné bunky pred oxidačným stresom. Príroda. 2002;419:316–321. doi: 10.1038/nature01036. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 86.Yamamoto M, Clark JD, Pastor JV a kol. Regulácia oxidačného stresu hormónom proti starnutiu Klotho. J Biol Chem. 2005;280:38029–38034. doi: 10.1074/jbc.M509039200. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 87.Ikushima M, Rakugi H, Ishikawa K, a kol. Antiapoptotické a anti-senescenčné účinky Klotho na vaskulárne endotelové bunky. Biochem Biophys Res Commun. 2006;339:827–832. doi: 10.1016/j.bbrc.2005.11.094. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 88.Sugiura H, Yoshida T, Tsuchiya K a kol. Klotho znižuje apoptózu pri experimentálnom ischemickom akútnom zlyhaní obličiek. Transplantácia nefrolového číselníka. 2005;20:2636–2645. doi: 10.1093/ndt/gfi165. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 89.Haruna Y, Kashihara N, Satoh M, a kol. Zlepšenie progresívneho poškodenia obličiek genetickou manipuláciou génu Klotho. Proc Natl Acad Sci USA A. 2007;104:2331–2336. doi: 10.1073/pnas.0611079104. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 90.Saito Y, Yamagishi T, Nakamura T a kol. Klotho proteín chráni pred endoteliálnou dysfunkciou. Biochem Biophys Res Commun. 1998;248:324–329. doi: 10.1006/bbrc.1998.8943. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 91.Shimada T, Takeshita Y, Murohara T a kol. Angiogenéza a vaskulogenéza sú u klotho myši v predčasnom starnutí narušené. Obeh. 2004;110:1148–1155. doi: 10.1161/01.CIR.0000139854.74847.99. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 92.Saito Y, Nakamura T, Ohyama Y a kol. In vivo dodanie klotho génu chráni pred endoteliálnou dysfunkciou pri syndróme viacerých rizikových faktorov [In Process Citation] Biochem Biophys Res Commun. 2000;276:767–772. doi: 10.1006/bbrc.2000.3470. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 93.Liu H, Fergusson MM, Castilho RM a kol. Rozšírená signalizácia Wnt v cicavčom modeli zrýchleného starnutia. Veda. 2007;317:803–806. doi: 10.1126/science.1143578. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 94.Scheller M, Huelsken J, Rosenbauer F, a kol. Defekty hematopoetických kmeňových buniek a viacerých línií generované konštitutívnou aktiváciou beta-katenínu. Nat Immunol. 2006;7:1037–1047. doi: 10.1038/ni1387. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 95.Kirstetter P, Anderson K, Porse BT, Jacobsen SE, Nerlov C. Aktivácia kanonickej dráhy Wnt vedie k strate repopulácie hematopoetických kmeňových buniek a blokovaniu viaclínovej diferenciácie. Nat Immunol. 2006;7:1048–1056. doi: 10.1038/ni1381. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 96.Kawaguchi H, Manabe N, Miyaura C, Chikuda H, Nakamura K, Kuro-o M. Nezávislé poškodenie diferenciácie osteoblastov a osteoklastov u klotho myši vykazujúcej osteopéniu s nízkym obratom. J Clin Invest. 1999;104:229–237. doi: 10.1172/JCI5705. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 97.Manya H, Inomata M, Fujimori T, a kol. Nedostatok proteínu Klotho vedie k nadmernej aktivácii mu-calpainu. J Biol Chem. 2002;277:35503–35508. doi: 10.1074/jbc.M206033200. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 98.Li G, Iyengar R. Calpain ako efektor Gq signálnej dráhy na inhibíciu Wnt/beta-katenínu regulovanej bunkovej proliferácie. Proc Natl Acad Sci US A. 2002;99:13254–13259. doi: 10.1073/pnas.202355799. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 99.Essers MA, de Vries-Smits LM, Barker N, Polderman PE, Burgering BM, Korswagen HC. Funkčná interakcia medzi beta-katenínom a FOXO v signalizácii oxidačného stresu. Veda. 2005;308:1181–1184. doi: 10.1126/science.1109083. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 100.Kops GJ, Medema RH, Glassford J a kol. Riadenie výstupu a vstupu bunkového cyklu transkripčnými faktormi vidlíc regulovanými proteínkinázou B. Mol Cell Biol. 2002;22:2025–2036. doi: 10.1128/MCB.22.7.2025-2036.2002. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 101.Wolf I, Sadetzki S, Gluck I, a kol. Asociácia medzi diabetes mellitus a nepriaznivými charakteristikami rakoviny prsníka pri prezentácii. Eur J Cancer. 2006;42:1077–1082. doi: 10.1016/j.ejca.2006.01.027. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 102.Yee D. Zacielenie na dráhy rastového faktora podobného inzulínu. Br J Cancer. 2006;94:465–468. doi: 10.1038/sj.bjc.6602963. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 103.Bartucci M, Morelli C, Mauro L, Ando S, Surmacz E. Signalizácia a funkcia diferenciálneho receptora inzulínu podobného rastového faktora I v bunkách rakoviny prsníka MCF-7 pozitívnych na estrogénový receptor (ER) a MDA-MB-231 negatívnych na ER. Cancer Res. 2001;61:6747–6754. [ PubMed ] [ Študovňa Google ]
- 104.Gery S, Tanosaki S, Bose S, Bose N, Vadgama J, Koeffler HP. Down-regulácia a inhibičná úloha C/EBPalpha pri rakovine prsníka. Clin Cancer Res. 2005;11:3184–3190. doi: 10.1158/1078-0432.CCR-04-2625. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 105.Arking DE, Krebsová A, Macek M, Sr, et al. Asociácia ľudského starnutia s funkčným variantom klotho. Proc Natl Acad Sci US A. 2002;99:856–861. doi: 10.1073/pnas.022484299. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 106.Arking DE, Becker DM, Yanek LR a kol. Stav alely KLOTHO a riziko skorého nástupu okultného ochorenia koronárnych artérií. Am J Hum Genet. 2003;72:1154–1161. doi: 10.1086/375035. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]
- 107.Arking DE, Atzmon G, Arking A, Barzilai N, Dietz HC. Asociácia medzi funkčným variantom génu KLOTHO a lipoproteínovým cholesterolom s vysokou hustotou, krvným tlakom, mŕtvicou a dlhovekosťou. Circ Res. 2005;96:412–418. doi: 10.1161/01.RES.0000157171.04054.30. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 108.Kawano K, Ogata N, Chiano M a kol. Polymorfizmy génu Klotho spojené s hustotou kostí starších žien po menopauze. J Bone Miner Res. 2002;17:1744–1751. doi: 10.1359/jbmr.2002.17.10.1744. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 109.Ogata N, Matsumura Y, Shiraki M a kol. Asociácia polymorfizmu génu klotho s hustotou kostí a spondylózou bedrovej chrbtice u žien po menopauze. Kosť. 2002;31:37–42. doi: 10.1016/s8756-3282(02)00786-x. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 110.Yamada Y, Ando F, Niino N, Shimokata H. Asociácia polymorfizmov androgénneho receptora a génov klotho s kostnou minerálnou hustotou u japonských žien. J Mol Med. 2005;83:50–57. doi: 10.1007/s00109-004-0578-4. Epub 2004 november 2004. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 111.Zarrabeitia MT, Hernandez JL, Valero C, a kol. Polymorfizmus génu Klotho a kostná hmota u mužov. Calcif Tissue Int. 2007;80:10–14. doi: 10.1007/s00223-006-0233-x. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 112.Rhee EJ, Oh KW, Yun EJ a kol. Vzťah medzi polymorfizmami G395A v promótore a C1818T v exóne 4 génu KLOTHO s metabolizmom glukózy a kardiovaskulárnymi rizikovými faktormi u kórejských žien. J Endocrinol Invest. 2006;29:613–618. doi: 10.1007/BF03344160. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 113.Kachiwala SJ, Harris SE, Wright AF a kol. Genetické vplyvy na oxidačný stres a ich spojenie s normálnym kognitívnym starnutím. Neurosci Lett. 2005;386:116–120. doi: 10.1016/j.neulet.2005.05.067. [ DOI ] [ PubMed ] [ Študovňa Google ]
- 114.Ichikawa S, Imel EA, Kreiter ML a kol. Homozygotná missense mutácia v ľudskom KLOTHO spôsobuje závažnú nádorovú kalcinózu. J Clin Invest. 2007;117:2692–2701. doi: 10.1172/JCI31330. [ DOI ] [ bezplatný článok PMC ] [ PubMed ] [ Google Scholar ]