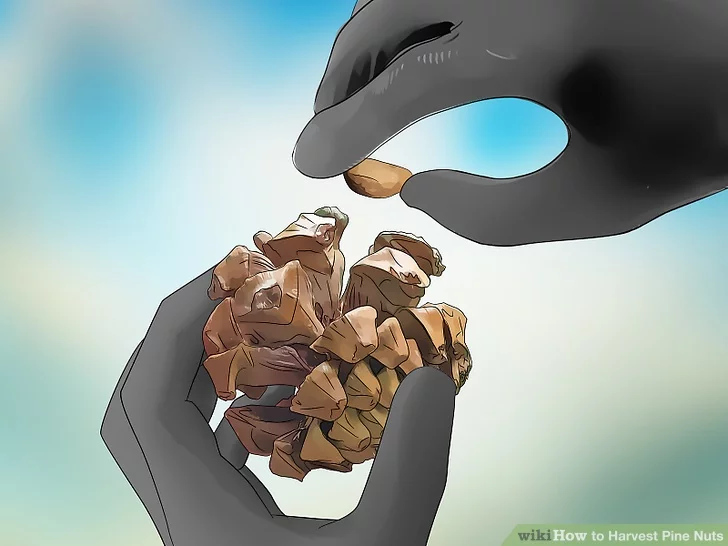Obsah
ToggleBorrelia burgdorferi a Treponema pallidum : porovnanie funkčnej genomiky, environmentálnych adaptácií a patogénnych mechanizmov
Spirochety sú rôznorodou skupinou baktérií, ktoré sa nachádzajú v pôde, hlboko v morských sedimentoch, sú komenzálne v črevách termitov a iných článkonožcov alebo sú obligátnymi parazitmi stavovcov. Dve patogénne spirochéty, ktoré sú stredobodom tejto perspektívy, sú Borrelia burgdorferi sensu lato, pôvodca lymskej choroby, a Treponema pallidum subspecies pallidum , pôvodca pohlavného syfilisu. Aj keď sú tieto organizmy spojené starovekým pôvodom a podobnou morfológiou (obrázok(Obrázok 1),1), ako aj z dôvodu proteínovej povahy infekcií, ktoré spôsobujú, existuje veľa rozdielov v ich životných cykloch, environmentálnych adaptáciách a vplyve na ľudské zdravie a správanie. Špecifické mechanizmy prispievajúce k multisystémovému ochoreniu a pretrvávajúcim, dlhodobým infekciám spôsobeným oboma organizmami napriek významným imunitným odpovediam ešte nie sú známe.
T. pallidum spojené s povrchom ľudského lymfocytu. Snímka z rastrovacieho elektrónového mikroskopu demonštruje vlnovú štruktúru charakteristickú pre spirochéty.
Centrá pre kontrolu a prevenciu chorôb oznámili 16 801 prípadov lymskej boreliózy a 37 977 prípadov syfilisu v Spojených štátoch v roku 1998. Syfilis bol prvýkrát pozorovaný pred viac ako 500 rokmi, hoci bakteriálna príčina bola stanovená až v roku 1905 ( 1 ). Lymská borelióza bola opísaná pred 25 rokmi s jej pôvodcom objaveným koncom roku 1981 ( 2 ), ale pokrok smerom k zvládaniu boreliózy nastal rýchlo a vakcína proti tejto chorobe je teraz schválená na použitie u ľudí a je dostupná v Spojených štátoch ( 3 ). Tento kritický pokrok bol čiastočne umožnený vďaka schopnosti kultivovať spirochéty lymskej choroby in vitro vďaka predchádzajúcemu vývoju Kellyho média ( 4 ) na kultiváciu borélií s recidivujúcou horúčkou. Naproti tomu T. pallidum sa musí pestovať v semenníkoch živých králikov, aby sa získali baktérie na experimentálne použitie ( 5 ). Zatiaľ čo proti syfilisu zatiaľ nie je dostupná žiadna vakcína, povinné spojenie spirochéty s ľuďmi a prenos sexuálnym kontaktom robí eradikáciu tejto choroby prinajmenšom predstaviteľnou. Likvidácia lymskej boreliózy nie je dosiahnuteľným cieľom, pretože B. burgdorferi je v prírode rozšírený a udržiava sa v zoonotických cykloch zahŕňajúcich mnoho druhov cicavcov, niektorých vtákov a prenos malými kliešťami, ktoré sa živia krvou. Nedávno boli publikované genómové sekvencie oboch týchto baktérií ( 6 – 8 ). Tu porovnávame biológiu a genómy týchto dvoch spirochetálnych patogénov s odkazom na ich rôzne hostiteľské asociácie a spôsoby prenosu.
Genomická štruktúra
Nápadným rozdielom medzi B. burgdorferi a T. pallidum je ich celková genómová štruktúra. Hoci oba patogény majú malé genómy, v porovnaní s mnohými dobre známymi baktériami, ako sú Escherichia coli a Mycobacterium tuberculosis , genómová štruktúra B. burgdorferi je jednou z najkomplexnejších známych u prokaryotov. Táto spirochéta obsahuje lineárny chromozóm s dĺžkou 910 725 bp s priemerným obsahom guanínu + cytozínu (G+C) 28,6 % ( 6 ). Identifikovalo sa tiež 21 extrachromozomálnych prvkov, vrátane 12 lineárnych a 9 kruhových plazmidov, spolu ďalších 610 694 bp ( 8 ). Medzi izolátmi sú značné rozdiely v obsahu plazmidov. Niektoré z týchto extrachromozomálnych prvkov sa pri sériovom šírení rýchlo strácajú.
Naproti tomu T. pallidum obsahuje jeden kruhový chromozóm s 1 138 006 bp, priemerný obsah G+C 52,8 % a žiadne extrachromozomálne prvky ( 7 ), vďaka čomu je jeho celkový genóm približne o 25 % menší ako genóm B. burgdorferi . Dôležité je, že žiadny z 1041 predpovedaných otvorených čítacích rámcov (ORF) T. pallidum nie je homológny so žiadnym z 535 intaktných ORF alebo 167 pseudogénov kódovaných plazmidmi B. burgdorferi ( 7 , 8 ). V skutočnosti viac ako 90 % ORF plazmidu B. burgdorferi nesúvisí so žiadnou známou bakteriálnou sekvenciou ( 8 ). Nové gény nachádzajúce sa v plazmidoch B. burgdorferi môžu preto prispievať k schopnosti tohto patogénu prežiť a udržať si svoj zložitý životný cyklus, pričom sa striedajú teplokrvné živočíchy a chladnokrvné kliešte ako hostitelia.
Lipoproteín a interakcie patogén-hostiteľ
Genóm B. burgdorferi obsahuje najmenej 132 génov kódujúcich domnelé lipoproteíny, ale len 22 takýchto génov je prítomných v T. pallidum ( 7 , 8 ). Lipoproteínové gény obsahujú 5 % chromozomálnych ORF v B. burgdorferi a 2,1 % z tých v T. pallidum . Hodnota T. pallidum sa približuje hodnotám iných typov baktérií, ako je Helicobacter pylori, v ktorom 1,3 % jeho genómu kóduje lipoproteíny ( 7 , 8 ). Zaujímavé je, že 14,5 až 17 % funkčne kompletných ORF na plazmidoch B. burgdorferi kóduje lipoproteíny ( 7 , 8 ). Dôvody tejto proporcionálne väčšej kódovacej kapacity pre lipoproteíny v B. burgdorferi v porovnaní s mnohými inými baktériami nie sú známe.
Lipoproteíny sú prevládajúcimi membránovými proteínovými imunogénmi pre T. pallidum aj B. burgdorferi ( 9 , 10 ). Žiadne lipoproteíny neboli definitívne lokalizované na vonkajšom povrchu T. pallidum . Na rozdiel od toho väčšina povrchovo exponovaných proteínov vytvorených B. burgdorferi sú lipoproteíny. Dva dobre charakterizované lipoproteíny sú vonkajší povrchový proteín A (OspA) a OspC. Gén OspA je fylogeneticky konzervovaný a jeho proteínový produkt je imunogén v nedávno schválenej ľudskej vakcíne proti lymskej borelióze ( 3 ). Naopak, gén OspC má značnú sekvenčnú heterogenitu medzi prírodnými izolátmi na úrovni DNA aj aminokyselín. Tento gén je tiež rozdielne exprimovaný pri vyšších teplotách a predpokladá sa, že jeho proteínový produkt je zapojený do prenosu spirochét počas uhryznutia kliešťom a skorej kolonizácie u stavovcov ( 11 ).
Rozdiel v počte a umiestnení lipoproteínov v bunkách tvorených týmito dvoma spirochétami naznačuje funkčnú úlohu boreliových lipoproteínov pri prežití u rôznych hostiteľov a/alebo prenose kliešťami. Syntéza mnohých boreliových lipoproteínov sa zvyšuje, keď sa teplota rastu posunie z 23 °C na 35 °C ( 11 , 12 ), čo je zmena, o ktorej sa predpokladá, že napodobňuje otepľovanie, ku ktorému dochádza, keď B. burgdorferi prechádza z kliešťov na cicavce. V súlade s touto myšlienkou sú mnohé lipoproteíny B. burgdorferi rozpoznávané sérami z infikovaných zvierat ( 9 , 12 ), čo naznačuje, že cicavec je počas infekcie vystavený týmto proteínom. Tieto pozorovania naznačujú, že mnohé z lipoproteínov B. burgdorferi sú zapojené do interakcií hostiteľ-patogén a predpokladáme, že to platí aj pre T. pallidum .
Vzhľadom na dôkazy, že boreliové a treponémové lipoproteíny interagujú s imunitným systémom cicavcov na začiatku infekcie, mnohé štúdie skúmali ich potenciálnu úlohu pri produkcii cytokínov a aktivácii imunitných buniek. Lipoproteíny vonkajšej membrány B. burgdorferi aktivujú makrofágy, endotelové bunky, neutrofily a B bunky ( 13 ). Kožný zápal charakterizovaný infiltráciou neutrofilov, heterofilov a mononukleárnych buniek bol pozorovaný u myší a králikov po injekciách lipopeptidov B. burgdorferi a T. pallidum ( 14 ). Lipoproteíny sa teda môžu podieľať na počiatočných zápalových procesoch, ktoré sa vyskytujú pri erythema migrans a primárnej lézii pri syfilise.
Patogenéza spojená s lymskou boreliózou podnietila výskum úlohy spirochétových lipoproteínov v dráhe ochorenia ( 15 – 17 ). Pikomolárne množstvá OspA zvyšujú CD10 a CD11b, znižujú CD62-L a aktivujú neutrofily ( 15 ), čo naznačuje účasť lipoproteínov na tkanivovo špecifickom artritickom zápale, kde je známe, že neutrofily sú prevládajúcim infiltrátom. Toll-like receptor 2 sa podieľa aj na prenose signálu pre boreliové a treponémové lipopeptidy a lipoproteíny ( 18 , 19 ), čo je integrálny proces potenciálne zapojený do zápalových procesov spojených s lymskou artritídou. Okrem toho spirochéty B. burgdorferi a T. pallidum , ako aj lipoproteíny a lipopeptidy odvodené z týchto organizmov môžu indukovať pro- a protizápalové cytokíny, vrátane TNF, IL-1β, IL-6, IL-8, IL-10 a IL-12 ( 16 , 18 , 19 ) v monocytoch prostredníctvom počiatočnej signalizácie alebo väzbovej udalosti s receptorom CD-14 ( 16 , 17 ). Brown a kol. ( 13 ) pozorovali, že u myší s deficitom IL-10, protizápalového cytokínu, sa po infekcii B. burgdorferi vyvinula závažnejšia artritída ako u normálnych myší s rovnakým genetickým pozadím. Prekvapivo bol počet spirochét v členkoch myší s deficitom IL-10 desaťkrát nižší ako u normálnych myší a ich titre IgG voči spirochetálnym antigénom boli výrazne vyššie. Je zrejmé, že interakcie medzi B. burgdorferi a bunkovou a humorálnou imunitnou odpoveďou hostiteľa sú zložité a ich účinok na vyvolanie a závažnosť lymskej artritídy si vyžaduje ďalšie skúmanie.
Množstvo lipoproteínov v B. burgdorferi v porovnaní s inými bakteriálnymi patogénmi naznačuje, že modifikácia lipidov má zásadnú úlohu spojenú so spirochetálnym rámcom, aktivitou alebo funkciou proteínu. Napríklad prístup protilátky k exponovanej slučke integrálneho proteínu vonkajšej membrány P66 B. burgdorferi je blokovaný prítomnosťou OspA ( 20 ). Ani B. burgdorferi, ani T. pallidum neprodukujú skutočný LPS a analýzy ich príslušných genómov naznačujú, že dráhy obsahujúce biosyntetické gény podobné LPS neexistujú ( 6 , 7 ). Obom spirochétám chýba schopnosť predlžovať mastné kyseliny s dlhým reťazcom, takže ich zloženie mastných kyselín odráža zloženie prítomné v kultivačnom médiu alebo hostiteľovi. Lipidové časti membránovo asociovaných proteínov indukujú imunologickú stimuláciu u cicavčieho hostiteľa, podobne ako LPS u iných bakteriálnych patogénov. Imunostimulačný proces sprostredkovaný lipoproteínmi môže viesť k obmedzeniu a kontrole zápalových procesov alebo v prípade citlivých hostiteľov k lymskej artritíde, s chronickosťou vyplývajúcou z nízkych hladín perzistentných spirochét.
Variácie vonkajších povrchových proteínov
B. burgdorferi aj T. pallidum obsahujú genetické systémy s potenciálom pre antigénne variácie povrchových molekúl. Borrelia hermsii obsahuje variabilný hlavný proteínový systém (Vmp), ktorý kóduje povrchovo exponované lipoproteíny dvoch veľkostných tried, variabilné malé proteíny (Vsp) alebo variabilné veľké proteíny (Vlp). Systém podobný Vmp (Vls) nedávno objavený v B. burgdorferi kóduje proteíny, ktoré sú najviac podobné rodine Vlp B. hermsii . B. burgdorferi má 15 tichých génov vls susediacich s miestom expresie ( vlsE ), ktoré sa nachádza v blízkosti teloméry plazmidu s veľkosťou 28 kb ( 21 ) (obr.(Obrázok 2).2). K rekombinácii génov vls dochádza skoro počas infekcie cicavcov a zahŕňa udalosť génovej konverzie, v ktorej tichá kazeta vls nahrádza zodpovedajúcu oblasť v géne vls nachádzajúceho sa v mieste expresie vlsE . Systém vls má potenciál produkovať milióny antigénnych variantov počas infekcie cicavčieho hostiteľa ( 21 ) a špekulovalo sa, že variácia Vls prispieva k perzistencii organizmu in vivo.
Usporiadanie približne 10 kb vls lokusu v B. burgdorferi umiestneného blízko pravej teloméry lineárneho plazmidu 28-1. Smery kódovania alebo výrazu sú znázornené vodorovnými šípkami. Rámček 1 predstavuje exprimovaný gén, zatiaľ čo rámčeky 2 až 16 predstavujú tiché génové kazety. Obrázok modifikovaný podľa Zhang et al. ( 21 ).
Chronická syfilitická infekcia pozorovaná u neliečených jedincov, kde sú obdobia latencie prerušované epizódami aktívneho ochorenia, naznačuje, že tieto baktérie sa môžu vyhnúť imunitnému systému hostiteľa jedným alebo viacerými mechanizmami. Doposiaľ nebol vo vonkajšej membráne T. pallidum definitívne lokalizovaný ani identifikovaný žiadny antigén , čo je faktor, ktorý prispieva k myšlienke, že spirochéta je „skrytý patogén“. V genóme T. pallidum bola objavená génová rodina s 12 členmi, nazývaná tpr . Tieto proteíny sú homológne s hlavným proteínom obalu (Msp) Treponema denticola , molekuly, o ktorej sa uvádza, že je povrchovo exponovaná a podieľa sa na prichytávaní buniek. Hoci génom tpr chýba konsenzus lipoproteínová sekvencia, predpokladá sa, že tri členovia (TprF, TprI a TprK) sú asociované s vonkajšou membránou T. pallidum ( 22 ). Prítomnosť viacerých alel tprK v rámci rovnakého izolátu T. pallidum a heterogenita génu tprK medzi izolátmi ( 23 ) naznačuje, že existuje viacero subpopulácií alebo genetických variantov. Prítomnosť komplexnej rodiny génov tpr s viacerými alelami génu tprK tiež naznačuje, že tprK má schopnosť podstúpiť rekombináciu s tvorbou nových alel alebo génových variantov v izoláte. Pretože gény tprK nie sú obmedzené na jeden lokus s jedným promótorom, mechanizmus generovania génovej variácie musí byť odlišný od mechanizmu používaného u borélií v lokusoch vmp a vls . Akokoľvek sa táto diverzita vytvorí, gén(y) tprK alebo iní členovia rodiny génov tpr zjavne pomáhajú vysvetliť nedostatok krížovej imunity u zvierat vystavených nehomológnym kmeňom ( 23 ).
Fenotypová reakcia na zmeny teploty
Teplota je dôležitým environmentálnym signálom, ktorý spúšťa adaptáciu patogénnych baktérií na ich hostiteľov. Teplotné rozsahy B. burgdorferi a T. pallidum sa výrazne líšia. Napríklad spirochéta lymskej choroby zažíva značnú zmenu teploty, keď sa striedajú teplokrvné cicavce a studenokrvné kliešte. Na rozdiel od toho je teplota pre T. pallidum obmedzená na úzky rozsah, ktorý jej ukladá ľudská homeostáza. Teplotne indukovaná diferenciálna expresia potenciálnych determinantov virulencie bola viac skúmaná u B. burgdorferi , pretože tento organizmus môže rásť nepretržite v tekutom, acelulárnom médiu a môže byť analyzovaný v kliešťoch chovaných pri rôznych teplotách okolia.
Niekoľko preukázaných alebo predpokladaných vonkajších povrchových lipoproteínov B. burgdorferi je rozdielne exprimovaných pri teplotách, ktoré korelujú s infekciou kliešťov alebo cicavcov. Počas prirodzeného prenosového cyklu je OspA produkovaný spirochétou iba v kliešťoch a nie u cicavcov ( 11 , 24 , 25 ), čo naznačuje, že rast pri vyšších teplotách znižuje produkciu tohto proteínu. Tento koncept podporujú pozorovania, že množstvo OspA exprimovaného baktériami klesá, keď sú spirochéty kokultivované pri teplote hostiteľa cicavca s kliešťovými bunkami ( 26 ), alebo keď sú prítomné v prisatých, infikovaných kliešťoch kŕmiacich sa na myšiach (zahrievajúcich sa na takmer 37 ° C) ( 24,25 ) . Neprítomnosť humorálnej imunitnej odpovede na OspA u myší a ľudí infikovaných uhryznutím kliešťom naznačuje, že tieto OspA-negatívne spirochéty iniciujú a pretrvávajú počas infekcie. Na rozdiel od OspA, OspC neprodukujú spirochéty v nekŕmených kliešťoch žijúcich pri teplote okolia. Avšak počas prvých 48 hodín, kedy sa infikované kliešte prichytia a kŕmia, spirochéty rýchlo upregulujú OspC, takže 75 % spirochét v strednom čreve kliešťa exprimuje tento proteín ( 25 ). Upregulácia OspC môže byť reprodukovaná v Kellyho médiu zvýšením inkubačnej teploty z 23 °C na 35–37 °C ( 11 ). Sérokonverzia na OspC u cicavcov infikovaných uhryznutím kliešťom podporuje prítomnosť OspC na týchto spirochétach počas prenosu. Rýchla upregulácia OspC počas kŕmenia kliešťom naznačuje, že tento proteín sa podieľa na prenose a skorej kolonizácii spirochéty u cicavcov. Tieto fenotypové zmeny expresie proteínov OspA a OspC spojené s prirodzeným cyklom prenosu a udržiavania B. burgdorferi sú zhrnuté na obrázkuObrázok 3.3. Ostatné lipoproteíny, ako sú Erps, Mlps, OspE, OspF a OppAV, sú tiež upregulované, keď sa spirochéty pestujú pri vyšších teplotách ( 12 , 27 – 29 ), ale profil expresie týchto proteínov vo voľne žijúcich a kŕmiacich sa kliešťoch zostáva nezmenený. určený.
Prirodzený udržiavací cyklus a súvisiace biologické parametre pre B. burgdorferi . ( a ) V prírode sa spirochéta udržiava striedaním infekcií u bielonohých myší a nezrelých kliešťov Ixodes . Larvy (L) získavajú spirochéty kŕmením infikovanými myšami a udržiavajú infekciu prostredníctvom transstadiálneho (TST) molt. Infikované nymfy (N) prenášajú spirochéty počas nasledujúceho krvného jedla. ( b ) Spirochety sú vystavené striedavým teplotám počas infekcií kliešťami a cicavcami a iným parametrom spojeným s prichytením a kŕmením kliešťa. ( c ) OspA a OspC sú rozdielne exprimované spirochétami počas prenosového cyklu so striedavými hostiteľmi kliešťami a cicavcami. ( d ) Všeobecný trend v titre protilátok proti OspA a OspC u myší infikovaných uhryznutím kliešťom, čo podporuje dôkaz o nedostatku expresie OspA počas infekcie a skorej prítomnosti OspC po uhryznutí kliešťom.
Zatiaľ čo T. pallidum možno pestovať in vitro počas obmedzeného počtu dní prostredníctvom kokultivácie s epitelovými bunkami králika bavlníka (Sf1Ep), tento proces sa musí vykonávať pri 33 °C ( 30 ). Existujú nepriame dôkazy, že T. pallidum mení expresiu potenciálnych determinantov virulencie pri rôznych teplotách. Napríklad exacerbácia syfilitických kožných lézií sa vyskytuje u experimentálne infikovaných králikov s oholeným chrbtom, keď sú zvieratá držané v miestnostiach ochladených na 16–18 °C ( 5 ). Okrem toho mierne nižšia teplota ľudských príveskov a výskyt klasických sekundárnych syfilitických kožných lézií na rukách a nohách naznačujú, že T. pallidum rastie optimálne pri teplote o niekoľko stupňov menej ako 37 °C.
Čo sa týka vysokej teploty, B. burgdorferi aj T. pallidum postrádajú ς faktor 32 ( 6 , 7 ), primárny mediátor reakcie tepelného šoku, hoci existujú dôkazy, že B. burgdorferi môže vyvolať reakciu tepelného šoku, zatiaľ čo T pallidum nemôže. In vitro kultivácia B. burgdorferi pri rôznych teplotách ukazuje, že spirochéta sa replikuje najrýchlejšie pri 37 °C. Zvýšenie teploty na 39 °C výrazne spomaľuje rast, zatiaľ čo 24-hodinová expozícia pri 41 °C zabíja všetky spirochéty v kultúre. Preto je optimálna teplota rastu B. burgdorferi iba 4 °C pod hornou letálnou hranicou. Nízka tolerancia spirochét voči vysokým teplotám je dobre známa a môže čiastočne vysvetliť obmedzenú distribúciu B. burgdorferi v miernych zemepisných šírkach a jej absenciu v trópoch, kde môžu byť infikované kliešte vystavené vysokým teplotám, ktoré sú škodlivé pre prežitie spirochét. Je zaujímavé, že tepelná citlivosť T. pallidum bola využívaná na začiatku 20. storočia pred objavom penicilínu pomocou liečby horúčky s maláriou alebo recidivujúcej horúčky na liečbu pacientov s celkovou parézou ( 31 ).
Záverečné poznámky
Okrem morfologických a fylogenetických podobností, ktoré existujú medzi T. pallidum a B. burgdorferi , choroby, ktoré spôsobujú, zahŕňajú viacstupňové proteínové klinické prejavy, ktoré zahŕňajú dermatologické a neurologické postihnutie a chronicky infikovaný stav u neliečeného hostiteľa. Výskumníci T. pallidum včas rozpoznali paralely medzi spirochétou syfilis a novo vznikajúcou spirochétou prenášanou kliešťami a prispeli svojimi odbornými znalosťami k pochopeniu biológie a patogenézy borélií. V skutočnosti schopnosť kultivovať borélie in vitro prilákala mnohých výskumníkov pracujúcich na T. pallidum po objave B. burgdorferi . Určenie kompletných genómov B. burgdorferi a T. pallidum ( 6 , 7 ) už prispelo k lepšiemu pochopeniu chromozomálnej štruktúry, génovej regulácie a špecifických fyziologických potrieb, ako je pozorovanie, že železo nie je potrebné na prežitie ( 32 , 33 ). Porovnanie genómu T. pallidum s inými bakteriálnymi genómami môže prispieť k vývoju zostavy základných živín pre médium, ktoré bude poskytovať kontinuálny rast in vitro. Ak takýto pokrok nedôjde, môžeme očakávať pokračujúce oneskorenie vedeckého pokroku s T. pallidum . Pretože techniky na inaktiváciu génov boli úspešné u B. burgdorferi ( 34 ), ale zatiaľ nie u T. pallidum , informačná medzera sa pravdepodobne zväčší, ale tieto prístupy môžu poskytnúť rámec pre budúce genetické snahy o spirochétu syfilis.
Približne 0,61 megabázových párov DNA jedinečných pre plazmidy B. burgdorferi kódujú početné lipoproteínové gény, z ktorých niektoré sú rozdielne regulované teplotou. Mechanizmy tepelného snímania spirochétami ešte nie sú známe, ale pravdepodobne zdieľajú stratégie používané inými baktériami ( 35 ). Na základe údajov o expresii sa mnohé z odlišne regulovaných lipoproteínov môžu podieľať na adaptácii na cyklovanie medzi chladnokrvnými kliešťami a teplokrvnými stavovcami. Takýto rozsiahly repertoár proteínov môže byť zbytočný pre T. pallidum , ktorý nevyžaduje vektor článkonožcov.
Jedným z nápadných rozdielov medzi týmito organizmami je schopnosť T. pallidum prechádzať ľudskou placentou, čo má za následok potenciálne ničivé následky vrodeného syfilisu. Transplacentárny prenos B. burgdorferi nebol preukázaný v štúdiách na zvieratách a je zriedkavý alebo neexistuje u ľudí, ale transplacentárny prenos je dobre zdokumentovaný v prípade B. hermsii a iných spirochét, ktoré spôsobujú recidivujúcu horúčku. Určenie genómových sekvencií týchto iných patogénov môže poskytnúť pohľad na mechanizmy zodpovedné za transplacentárny prenos.
Poďakovanie
Ospravedlňujeme sa kolegom, že z priestorových dôvodov neuvádzame veľa relevantných prác. Ďakujeme Daveovi Dorwardovi za skenovaciu elektrónovú mikroskopiu a Garymu Hettrickovi za grafické práce.