Preklad: Dr.FYTO Team
- Ústav lekárskej mikrobiológie a kontroly infekcií, Univerzitná nemocnica vo Frankfurte, Goethe University Frankfurt, Frankfurt, Nemecko
Recidivujúca horúčka (RF) je považovaná za zanedbanú chorobu prenášanú článkonožcami spôsobenú množstvom rôznych ľudských patogénnych druhov Borrelia ( B. ). Tieto RF borélie sú rozdelené do skupín druhov prenášaných kliešťami vrátane B. duttonii, B. hermsii, B. parkeri, B. turicatae, B. hispanica, B. persica, B. caucasica a B. myiamotoi a voš -borélia druh B. recurrentis . Ako typické krvné patogény dosahujúce vysoké koncentrácie buniek v ľudskej krvi musia RF borélie (RFB) prekonať vrodenú imunitu, najmä komplement ako prvú obrannú líniu. Jedna prominentná stratégia vyvinutá RFB na obídenie vrodenej imunity zahŕňa inaktiváciu komplementu náborom odlišných komplementových regulačných proteínov, napr. -1 (FHL-1) a proteíny súvisiace s faktorom H FHR-1 a FHR-2, alebo väzba jednotlivých zložiek komplementu a plazminogénu, v danom poradí. V minulosti bolo identifikovaných a charakterizovaných množstvo multifunkčných molekúl viažucich komplement a plazminogén z rôznych druhov Borrelia , ktoré vykazujú značnú heterogenitu vo svojich sekvenciách, štruktúrach, lokalizácii génov a ich schopnosti viazať proteíny odvodené od hostiteľa. Okrem toho majú RFB jedinečný systém antigénnej variácie, ktorý im umožňuje meniť zloženie povrchovo exponovaných variabilných hlavných proteínov, čím sa vyhýba získanej imunitnej odpovedi ľudského hostiteľa. Tento prehľad sa zameriava na súčasné poznatky o stratégiách vyhýbania sa imunite pomocou RFB a zdôrazňuje úlohu molekúl interferujúcich s komplementom a molekúl spojených s infekciou pre patogenézu RFB.
Úvod
Recidivujúca horúčka (RF), bakteriálne ochorenie prenášané ektoparazitmi spôsobené druhmi Borrelia, je charakterizované opakujúcimi sa epizódami vysokej horúčky a spirochetémie v krvi infikovaných jedincov ( 1 – 4 ). RF je zanedbávané a objavujúce sa bakteriálne ochorenie v Amerike a niektorých afrických krajinách, najmä v regiónoch s vysokým výskytom infikovaných kliešťov argásidových a ixodidových rodu Ornithodoros , respektíve Ixodes , alebo voš ľudského tela Pediculus humanus ( 2 , 4 ) . Zatiaľ čo mäkký kliešťom prenášaný RF (STBRF) sa vyskytuje hlavne pozdĺž západného pobrežia Severnej Ameriky a endemický v miernych a tropických afrických územiach, výskyt tvrdých kliešťov prenášaných RF (HTBRF) priamo koreluje s distribúciou kliešťov ixodidov v severná pologuľa ( 5 , 6 ). Na rozdiel od toho je LBRF geograficky obmedzený na krajiny pozdĺž Afrického rohu, najmä na Eritreu, Etiópiu a Južný Sudán ( 4 ). Napriek svojmu ohniskovému rozdeleniu má LBRF potenciál dramaticky sa znovu objaviť, keď sa zmenia sociodemografické faktory ako vojna, hladomor, politické nepokoje a neisté hygienické podmienky v preplnených táboroch ( 7 – 11 ). Klinické príznaky STBRF a LBRF sa objavia náhle medzi 2. a 18. dňom po infekcii vysokou horúčkou, často sprevádzané zimnicou, bolesťami hlavy, zimnicou, nevoľnosťou, vracaním, myalgiou a hnačkou ( 2 , 4 ). Závažnejšie klinické prejavy postihujú rôzne orgány ako pečeň (hepatosplenomegália, dysfunkcia pečene, zlyhanie pečene), slezina (prasknutie), gastrointestinálny trakt (krvácanie), pľúca (akútny pľúcny edém, syndróm akútnej respiračnej tiesne), srdce (zlyhanie myokardu) a centrálny nervový systém (meningizmus, paréza tváre, vertigo, rigidita) ( 4 ). Čo sa týka HTBRF, ako najčastejšie symptómy sa uvádza horúčka, bolesť hlavy, zimnica, artralgia, únava a malátnosť a závažné neurologické prejavy ako meningoencefalitída sa vyskytujú prevažne u pacientov s oslabenou imunitou ( 6 , 12 , 13 ). Podobne ako spirochéty Lymskej choroby, RFB využíva rôzne stratégie vyhýbania sa imunite, aby sa vyhla rozpoznaniu a obchádzala vrodené a adaptívne imunitné reakcie. V tomto dokumente sumarizujeme súčasné poznatky o potenciálnych patogénnych faktoroch identifikovaných v rôznych RFB, ktoré pôsobia proti komplementovým a humorálnym imunitným odpovediam ľudského hostiteľa.
Systém doplnkov v skratke
Komplement funguje ako prvá obranná línia proti vniknutým patogénom a pozostáva z mnohých regulátorov, inhibítorov a neaktívnych prekurzorových molekúl naviazaných na tekutú fázu a membránu, z ktorých väčšina pôsobí pri aktivácii spoločne a eliminujú mikróby ( 14 ). Rovnako ako domino efekt môže byť komplementová kaskáda nezávisle aktivovaná tromi odlišnými dráhami: alternatívnou (AP), klasickou (CP) a lektínovou dráhou (LP) ( 15 , 16 ).
AP je spontánne aktivovaný takzvaným tick-over-procesom, ktorý vedie ku kovalentnému naviazaniu aktivovaných molekúl C3b na mikrobiálne povrchy a umožňuje tak nepretržité monitorovanie invazívnych ľudských patogénov (opsonizácia) ( 17 , 18 ). Aktivácia CP sa spúšťa väzbou C1q na povrchovo viazané klastre IgM alebo IgG a LP využíva lektín viažuci manózu (MBL), kolektoríny a fikolíny na rozpoznanie sacharidových skupín na povrchu bakteriálnych buniek ( 15 , 16 , 19 – 21 ). Po aktivácii sa vytvoria buď C3 konvertázy C3bBb (AP) alebo C4b2a (CP a LP), čo vedie k masívnej tvorbe aktivovaného C3b, ktorý sa kovalentne viaže na cudzie povrchy. Ďalšia downstream aktivácia je riadená väzbou C3b na C3 konvertázy, čo vedie k vytvoreniu C5 konvertáz C3bBb3b alebo C4b2a3b. Vytvorením C5 konvertázy sa C5 štiepi na C5a a C5b, ktoré sa kovalentne viaže na cieľový povrch. Tento kritický aktivačný krok inicializuje terminálnu sekvenciu (TS) a zostavenie komplexu C5b-9 alebo MAC atakujúceho póry. MAC, kruhovitá štruktúra, sa skladá z mnohých molekúl C9, z ktorých všetky sa integrujú do mikrobiálnej membrány a v konečnom dôsledku spôsobujú lýzu ( 22 – 24 ).
Na ochranu vlastných povrchov pred nadmernou aktiváciou je komplement prísne kontrolovaný rôznymi rozpustnými a bunkami viazanými regulačnými proteínmi komplementu ( 25 ). Čo sa týka rozpustných regulátorov, AP je regulovaný faktorom H (FH) a proteínom podobným faktoru H 1 (FHL-1) (vytvoreným alternatívnym zostrihom génu cfh ). Oba regulátory inaktivujú C3b na iC3b pôsobením ako kofaktory pre faktor I, čím urýchľujú rozpad C3 konvertázy viazanej na membránu. Na rozdiel od FH a FHL-1 sa predpokladá, že proteín 1 súvisiaci s faktorom H (FHR-1) je regulátorom TS a zdá sa, že blokuje štiepnu aktivitu C5 konvertáz inhibíciou tvorby C5a ( 26 ). . Úloha ďalších štyroch FHR proteínov v regulácii komplementu je zatiaľ nejasná. Nedávne údaje poskytujú určitý dôkaz, že tieto proteíny môžu zvyšovať aktiváciu komplementu, a teda majú opačnú regulačnú funkciu v porovnaní s FH a FHL-1 ( 27 ). Počiatočná aktivácia CP a LP je riadená inhibítorom C1 esterázy (C1-INH) inaktiváciou serínových proteáz C1r, C1s, MASP-1 a MASP-2. Okrem toho sú následné aktivačné kroky CP ukončené väzbou proteínu viažuceho C4b (C4BP) na C4b. Tento rozpustný regulátor pôsobí ako kofaktor pre degradáciu C4b sprostredkovanú Faktorom I. TS je blokovaný zabránením integrácie rozpustných preformujúcich komplexov sC5b-9 do cieľovej membrány prostredníctvom vitronektínu a klusterínu ( 16 ).
Nábor regulačných proteínov komplementu, efektívna stratégia RFB na únik zabíjania sprostredkovaného komplementom
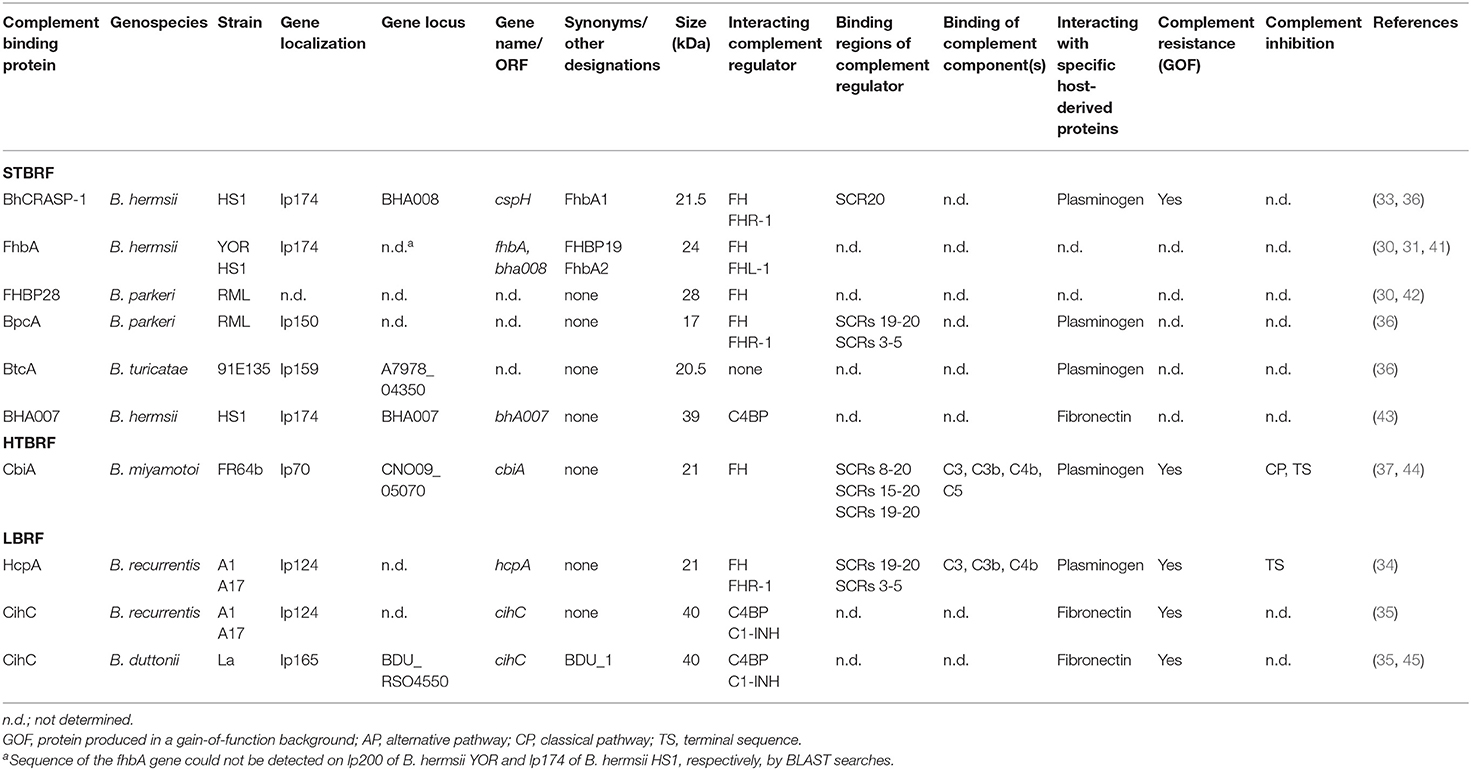
Bezprostredne po vstupe do cicavčieho hostiteľa sa RFB tvár doplní ako prvá obranná línia. Kontroverzne sa však diskutovalo o úlohe komplementu pri odstraňovaní spirochét. Ukázalo sa, že IgM je schopný účinne zabíjať B. hermsii v priebehu bakteriémie u infikovaných myší s deficitom C3 a C5 mechanizmom nezávislým od komplementu, zatiaľ čo myši s deficitom B buniek vykazovali veľmi vysoký obsah spirochét v krvi ( 28 , 29 ). Tieto zistenia viedli k predpokladu, že vrodená imunita hrá v patobiológii týchto patogénov podriadenú úlohu. Na druhej strane RFB produkuje proteíny viažuce komplement, z ktorých väčšina pôsobí na rôznych úrovniach aktivácie, aby chránili spirochéty pred komplementom sprostredkovanou bakteriolýzou ( 30 – 37 ). To zahŕňa proteíny B. hermsii, B. parkeri, B. duttonii, B. miyamotoi a B. recurrentis , v danom poradí. Prehľad charakteristík týchto podozrivých povrchových proteínov relevantných pre infekciu je uvedený nižšie.
Inaktivácia alternatívnej cesty naviazaním komplementového regulátora FH
Získavanie regulátorov aktivácie komplementu je jednou z najbežnejších stratégií, ktoré využívajú mnohé ľudské patogénne mikroorganizmy na vyhýbanie sa komplementu ( 38 – 40 ). Medzi druhmi RFB bolo opísaných najmenej sedem proteínov interagujúcich s FH vrátane BhCRASP-1 (FhbA1) z B. hermsii HS1 a FhbA2 (FhbA, FHBP19) z B. hermsii YOR, FHBP28 a BpcA z B. parkeri , CbiA z B. miyamotoi a HcpA z B. duttonii a B. recurrentis ( 30 , 31 , 33 , 34 , 36 , 37 ) ( tabuľka 1 ). Všetky proteíny interagujúce s FH majú spoločnú väzbu na C-koncové domény, z čoho vyplýva, že regulačné domény umiestnené na N-konci FH sú prístupné, aby si zachovali svoju degradačnú aktivitu C3b sprostredkovanú Faktorom I ( 33 , 34 , 36 , 37 ) ( Tabuľka 1 ). Navyše, BhCRASP-1, HcpA, BpcA a CbiA, v tomto poradí, uľahčujú rezistenciu voči komplementu, keď sú ektopicky produkované v geneticky manipulovaných spirochétách (kmene so ziskom funkcie) ( 33 , 34 , 36 , 37 ).
V rámci druhu Borrelia sú proteíny viažuce FH vysoko konzervované a vykazujú hodnoty sekvenčnej identity > 93 % ( 32 ), ale medzi RFB sú tieto percentá dosť nízke (36 – 45 %). Či by nedostatok sekvenčnej podobnosti mohol zodpovedať za iný záhyb, sa zdá byť trochu otázne, najmä vo svetle chýbajúcich trojrozmerných štruktúr. Je zaujímavé, že vo všetkých siedmich proteínoch bolo možné identifikovať aspoň štyri konzervované motívy (LDxNQKQALIxF, LGN-KxKQFLQxLH, SFSSxNFxD a LEQKKExAL), čo zvyšuje možnosť nekontinuálneho miesta viazania FH. Ďalšie štúdie skúmajúce varianty FhbA2, FHBP28, HcpA a BpcA tiež poskytujú dôkaz, že do interakcie s FH sú zapojené viaceré oblasti ( 30 , 34 , 36 , 41 ). Dôležité je, že infekčné štúdie využívajúce delečný mutant fhbA preukázali, že FhbA2 je jediným proteínom viažucim FH v B. hermsii a neprítomnosť FhbA nemala vplyv na sérovú rezistenciu alebo infekčnosť spirochét, čo naznačuje funkčne nadbytočné úlohy, ktoré hrá iný komplement -interagujúce proteíny, ako je diskutované nižšie ( 46 ).
Inaktivácia klasickej a lektínovej dráhy väzbou C1-INH a C4BP
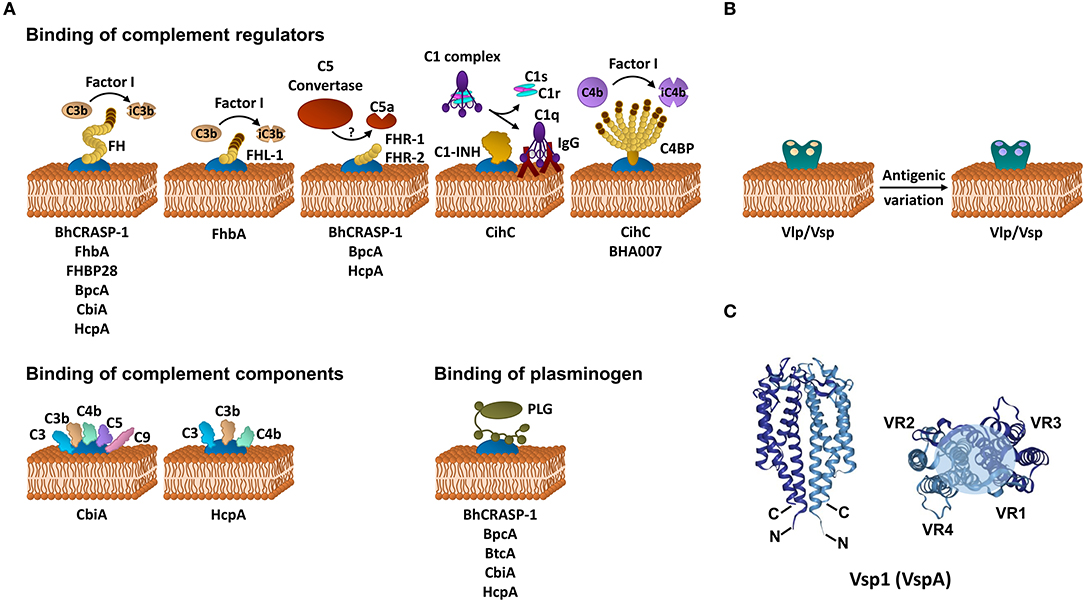
K dnešnému dňu je CihC z B. recurrentis jediným proteínom vykazujúcim vlastnosti inaktivujúce komplement na CP a LP väzbou na proteín viažuci C1-INH a C4BP ( 35 ). Ortologické proteíny vykazujúce sekvenčnú identitu medzi 44 a 91 % boli detegované v B. duttonii Ly (BDU_1026), B. hermsii (BHA007), B. turicatae (BTA001), B. parkeri (BpA001) a B. crocidurae Achema a DOU (BCD_1370), ale v LD sa nenašli žiadne homológne sekvencie spirochéty ( 42 , 43 ). Funkčné analýzy odhalili, že podobne ako FH, aj C4BP naviazaný na boreliový povrch si zachoval svoju inhibičnú aktivitu na komplement pre degradáciu C4b sprostredkovanú faktorom I, čím sa zamerala na aktiváciu CP a LP ( obrázok 1A , tabuľka 1 ). Predtým Meri a spol. tiež preukázali inaktiváciu CP väzbou funkčného aktívneho C4BP na povrch B. recurrentis a B. duttonii ( 45 ). Okrem toho CihC tiež podporuje ukončenie CP v počiatočných aktivačných krokoch väzbou C1-INH, čo naznačuje, že táto boreliová molekula vykazuje multifunkčné vlastnosti inhibujúce komplement. Delécie na N- a C-konci CihC nezrušili väzbu C4BP alebo C1-INH, čo viedlo k predpokladu, že centrálne oblasti môžu byť zodpovedné za väzbu ( tabuľka 1 ). Rozhodujúca úloha CihC pri sprostredkovaní sérovej rezistencie RFB bola preukázaná použitím kmeňov so ziskom funkcie exprimujúcich cihC , ktoré vykazovali rezistentný fenotyp po stimulácii séra ( 35 ). Na rozdiel od CihC sa proteín BHA007 z B. hermsii viaže iba na C4BP, ale nie na C1-INH ( 42 ). Vďaka ich funkčným vlastnostiam interagovať s fibronektínom boli tieto molekuly všeobecne pomenované ako „proteíny viažuce fibronektín“ a zoskupené spolu s proteínom BBK32 viažucim fibronektín spirochét Lymskej choroby ( 42 ). Napriek ich nízkej sekvenčnej podobnosti zistenie, že BBK32 umožňuje prežitie spirochét v krvnom riečisku ( 48 ), podporuje možnosť, že ortológy CihC môžu hrať úlohu aj pri infekcii ľudského hostiteľa. Čo sa týka inaktivácie CP, CbiA z B. miyamotoi už skôr dokázalo, že silne inhibuje aktiváciu CP, nezávisle od interakcie s C4BP zatiaľ neznámym mechanizmom ( 37 ) ( obrázok 1A , tabuľka 1). Je lákavé špekulovať, či väzba C4b na CbiA obmedzuje downstream aktiváciu CP ukončením tvorby C3 konvertázy ( 37 ).
Obrázok 1 . Stratégie imunitného úniku RFB. (A) Inhibícia komplementu odlišnými boreliovými proteínmi pôsobiacimi na určitých úrovniach aktivačnej kaskády. (B) Imunitný únik RFB multifázovou antigénnou variáciou. (C) Schematické znázornenie štruktúry diméru Vsp1 (VspA) B. turicatae [PDB 2GA0, upravené z ( 47 )]. Monomérne jednotky sú znázornené tmavomodrou alebo svetlomodrou farbou. Variabilné sekvencie sú distribuované v rámci druhého a tretieho a-helixu, ako aj všetkých oblastí slučky a sú zhrnuté vo variabilnej oblasti (VR) 1–4. Svetlomodrý kruh v hornej časti diméru označuje oblasť s najvyššou variabilitou. FH, faktor H; FHL-1, proteín podobný faktoru H 1; FHR, proteín súvisiaci s faktorom H; C4BP, C1-INH, inhibítor C1 esterázy; C4b väzbový proteín; iC3b, inaktivovaný C3b; iC4b, inaktivovaný C4b, IgG, imunoglobulín G.
Inhibícia sekvencie terminálov a zostavy MAC
Ukončenie finálnych aktivačných krokov väzbou na komplexy tvoriace póry alebo neskoré zložky komplementu negatívne ovplyvňuje zostavenie MAC, ako sa ukázalo pre CbiA a HcpA ( 37 ) ( obrázok 1A , tabuľka 1 ). Najmä CbiA silne inhibuje TS, pravdepodobne prostredníctvom väzby C5 a C9, zatiaľ čo HcpA mierne ovplyvňuje komplement na tejto úrovni a BpcA a BtcA nemajú vôbec vplyv. Interferencia s TS zvyšuje proces inaktivácie komplementu sprostredkovaný odlišnými vonkajšími povrchovými proteínmi.
Inaktivácia komplementu získaním plazminogénu
Odlišné proteíny interagujúce s komplementom, vrátane BhCRASP-1, HcpA a CbiA, vykazujú viacnásobné väzbové špecificity k proteínom z tekutej fázy odvodeným od hostiteľa, ako je plazminogén ( 33 , 34 , 36 , 44 ) ( obrázok 1A , tabuľka 1 ). Je známe, že plazminogén sa viaže na C3, C3b, C3d a C5 a po aktivácii na plazmín dochádza k degradácii C3 a C5 ( 49 ). Plazminogén je tiež schopný zosilniť degradáciu C3b sprostredkovanú Faktorom I v prítomnosti FH ( 49 ). Predchádzajúce štúdie preukázali, že plazmín(ogén) naviazaný na B. hermsii HS1, B. recurrentis A1 a B. parkeri znižuje množstvo molekúl C3b uložených na boreliovom povrchu ( 33 , 34 , 36 ) alebo vedie k degradácii C3b pri purifikácii Použili sa HcpA, BpcA a CbiA ( 34 , 36 , 44 ). Degradácia C3 a C5 sa teda javí ako ďalšia stratégia RFB na úspešné prekonanie imunitnej obrany hostiteľa.
Priama interakcia s jednotlivými komponentmi doplnkov
HcpA a CbiA sa tiež do určitej miery viažu na jednotlivé zložky komplementu, konkrétne na C3, C3b, C4 a C4b, v danom poradí, ako aj na C5 (CbiA), hoci význam týchto interakcií pri inaktivácii komplementu si vyžaduje ďalšie skúmanie ( 37 ) ( obrázok 1A tabuľka 1 ) .
Záverom možno povedať, že tieto zistenia naznačujú zapojenie týchto molekúl do vyhýbania sa imunite, najmä preto, že inaktivácia kľúčovej zložky komplementu C3b sa považuje za účinný nástroj na prežitie baktérií a môže zodpovedať za mimoriadnu patogenézu RFB v ľudskom hostiteľovi.
Antigénna variácia, výkonný mechanizmus RFB na únik pred imunitou
Aby sa vyhli klírensu humorálnou imunitnou odpoveďou ľudského hostiteľa, RFB sú schopné produkovať hromadný repertoár antigénne odlišných sérotypov v danej bunkovej populácii geneticky riadeným procesom nazývaným antigénna variácia ( 50 ). Barbour a Stoenner vo svojej priekopníckej práci odhalili, že fenomén prepínania sérotypov je spontánny, reverzibilný a viacfázový proces, ktorý vytvára vonkajšie povrchové proteíny, ktoré nesú sérotypovo špecifické epitopy ( 50 ) ( obrázok 1B ). Tieto imunodominantné, variabilné hlavné lipoproteíny (Vmps) sú rozdelené do dvoch rôznych, vysoko polymorfných proteínových rodín: variabilné malé proteíny, Vsp (~20 kDa) a variabilné veľké proteíny, Vlp (~36 kDa), ktoré sú rozdelené do ďalších štyroch podrodín. : α, β, γ a δ ( 50 – 52 ). Molekulárny mechanizmus antigénnej variácie zjavne nepodlieha procesu, ktorý je pod tlakom miestneho prostredia, hostiteľských faktorov alebo imunitného systému hostiteľa. Uvedomujúc si, že z jednej bunky vzniká viacero sérotypov, možno teda teoreticky vytvoriť veľa variantov produkciou veľmi rôznorodých súborov Vlps a Vmps počas infekcie. Predchádzajúce štúdie odhalili, že počas infekcie cicavcov môže vzniknúť 60–70 antigénne odlišných variantov B. hermsii ( 52 ). Takáto značná diverzita sa dosahuje viacerými cyklami genetických preskupení génov kódujúcich Vmp vrátane (i) nerecipročnej rekombinácie tichých alebo archívnych génov vmp s aktívnym, transkribovaným génom vmp (génová konverzia), (ii) intramolekulárneho preskupenia DNA, a (iii) prepnutie miesta expresie vedúce k modifikácii transkriptu ( 53 , 54 ). Zdá sa, že mechanizmus intermolekulovej rekombinácie prebieha aj v starom svete RFB B. duttonii ( 55 ). Gény variabilného antigénu kódujúce Vlps a Vsps boli tiež detegované v B. turicatae, B. crocidurae, B. duttonii ( 56 , 57 ), B. miyamotoi ( 58 , 59 ) a B. recurrentis ( 60 , 61 ). Geneticky sú tiché alebo archívne gény vmp rozptýlené na rôznych lineárnych plazmidoch s veľkosťou 28–53 kb, zatiaľ čo aktívny, promótorom riadený expresný lokus sa nachádza iba na jednom plazmide ( 53 , 61 ). Takýto aktívny gén vlp alebo vsp môže byť vymenený za akýkoľvek archívny alebo tichý gén vlp a vspgén, ale frekvencia nahradenia sa medzi týmito génmi líši ( 62 ). Neustála výmena génov vmp nepochybne vytvorí početné polymorfné Vmps, čo umožní spirochétam zostať o krok vpred pred adaptívnou imunitnou odpoveďou, a tak sa úspešne vyhnúť obrane hostiteľa. V štúdii s použitím geneticky modifikovaných buniek B. hermsii , ktorým chýba schopnosť podstúpiť antigénnu variáciu, Raffel a kol. jasne preukázali, že Vmps sú potrebné na vyvolanie vysokej spirochetémie v krvi a na vyvolanie recidívy u infikovaných myší, pričom kolonizácia kliešťov týmito oslabenými spirochétami zostáva nedotknutá ( 63 ). Je zaujímavé, že bunky s nedostatkom Vmp vykazovali zníženú kondíciu v porovnaní s WT a rekonštituovanými spirochétami.
Spresnenia kryštálovej štruktúry Vsp a Vlp odhalili podobný sklad pre obe skupiny proteínov, ktoré sú prevažne zložené z 2-násobne symetrického diméru. Každá monomérna jednotka pozostáva zo štyroch a-helikálnych zväzkov spojených dvoma slučkovými oblasťami ( 47 , 64 ) ( obrázok 1C ). N-koniec je ukotvený v spirochetálnej membráne, zatiaľ čo flexibilný C-koniec je zložený späť a orientovaný tesne k N-koncu. Oblasti variabilnej slučky sú vystavené prostrediu a slúžia ako ligandy pre protilátky. Je zaujímavé, že najkonzervovanejšie oblasti sú orientované na vonkajšiu stranu proteínu, o ktorom je známe, že sú cieľmi pre anti-Vmp protilátky vyvolané počas infekcie. Za zmienku stojí, že OspC, hlavný vonkajší povrchový proteín B. burgdorferi , je fylogeneticky a štrukturálne príbuzný a zdieľa spoločný špirálovitý záhyb s Vsps, čo naznačuje, že tieto proteíny môžu vykazovať podobnú úlohu pri vyhýbaní sa imunite ( 47 , 65 ).
Záverečné poznámky
Počas posledných desaťročí bolo opísaných množstvo molekúl interagujúcich s komplementom, z ktorých všetky sa určitým spôsobom dotýkajú prvej línie obrany hostiteľa tým, že bránia aktivácii komplementu. V synergii s antigénnym variačným systémom sú RFB schopné opakovane obchádzať tak vrodený imunitný systém, ako aj získanú imunitnú odpoveď. Pochopenie molekulárnych princípov toho, ako tieto molekuly interferujú s vrodenou imunitou, môže pripraviť cestu pre vývoj nových terapeutík na liečbu pacientov s RF alebo pacientov trpiacich nedostatkom komplementu a môže dokonca slúžiť ako preventívne opatrenia pre infekčné choroby vo všeobecnosti. Povrchovo exponované molekuly môžu byť tiež súčasťou novej vakcíny alebo môžu byť použité na generovanie nových imunotestov ( 32 ). Budúce štúdie by nepochybne mali odhaliť dôležité otázky týkajúce sa úlohy funkčne nadbytočných, anti-komplementových proteínov v patogenéze týchto novo sa objavujúcich patogénov.
Autorské príspevky
FR a PK napísali rukopis a pripravili obrázok a tabuľku. Všetci autori prispeli k článku a schválili predloženú verziu.
Financovanie
Táto práca bola podporená LOEWE Center DRUID (Novel Drug Targets against Poverty-Related and Neglected Tropical Infectious Diseases), projekt C3 (PK).
Konflikt záujmov
Autori vyhlasujú, že výskum bol vykonaný bez akýchkoľvek obchodných alebo finančných vzťahov, ktoré by mohli byť chápané ako potenciálny konflikt záujmov.
Poďakovanie
Ďakujeme Arno Koenigs a Yi-Pin Lin za kritické čítanie a užitočné návrhy týkajúce sa rukopisu. Tiež by sme sa chceli poďakovať dvom recenzentom za pozorné čítanie nášho rukopisu a ich cenné a bystré komentáre.
Skratky
BpcA, B. parkeri komplementový regulátor viažuci proteín A; BtcA, B. turicatae proteín viažuci plazminogén; CbiA, komplement viažuci a inhibičný proteín A; CihC, inhibícia komplementu prostredníctvom C4BP; C1-INH, inhibítor C1 esterázy; C4BP, proteín viažuci C4b; FhbA, proteín A viažuci FH; FH, faktor H; FHL-1, proteín podobný FH-1; FHR, proteín súvisiaci s FH; HcpA, regulátor ľudského komplementu a proteín A viažuci plazminogén; HTBRF, recidivujúca horúčka prenášaná kliešťami; GAG, glykozaminoglykány; LBRF, všami prenášaná recidivujúca horúčka; MAC, komplex membránového útoku; RCA, regulátory aktivácie komplementu; RF, recidivujúca horúčka; RFB, recidivujúca horúčka borreliae; SCR, krátke konsenzuálne opakovania; STBRF, recidivujúca horúčka prenášaná kliešťami; Vlp, variabilný veľký proteín; Vmp, variabilný hlavný proteín; Vsp, variabilný malý proteín.
Referencie
1. Dworkin MS, Schwan TG, Anderson DE Jr., Borchardt SM. Recidivujúca horúčka prenášaná kliešťami. Infikovať Dis Clin North Am. (2008) 22:449-68. doi: 10.1016/j.idc.2008.03.006
2. Lopez JE, Krishnavahjala A, Garcia MN, Bermudez S. Spirochéty recidivujúcej horúčky prenášané kliešťami v Amerike. Vet Sci . (2016) 3:16. doi: 10.3390/vetsci3030016
3. Talagrand-Reboul E, Boyer PH, Bergstrom S, Vial L, Boulanger N. Recidivujúce horúčky: zanedbané choroby prenášané kliešťami. Front Cell Infect Microbiol . (2018) 8:98. doi: 10.3389/fcimb.2018.00098
4. Warrell DA. Všami prenášaná recidivujúca horúčka ( infekcia Borrelia recurrentis ). Epidemiol Infect . (2019) 147:e106. doi: 10.1017/S0950268819000116
5. Mzdári A, Staarink PJ, Sprong H, Hovius JW. Borrelia miyamotoi : rozšírená spirochéta s recidivujúcou horúčkou prenášanou kliešťami. Trendy Parasitol . (2015) 31:260–9. doi: 10.1016/j.pt.2015.03.008
6. Kameň BL, Brissette CA. Imunitný únik hostiteľa lymskou boréliou a recidivujúcou horúčkou: zistenia, ktoré budú viesť budúce štúdie o Borrelia miyamotoi . Front Immunol . (2017) 8:12. doi: 10.3389/fimmu.2017.00012
7. Hoch M, Wieser A, Loscher T, Margos G, Purner F, Zuhl J a kol. Všami prenášaná recidivujúca horúčka ( Borrelia recurrentis ) diagnostikovaná u 15 utečencov zo severovýchodnej Afriky: epidemiológia a preventívne kontrolné opatrenia, Bavorsko, Nemecko, júl až október 2015. Euro Surveill . (2015) 20. doi: 10.2807/1560-7917.ES.2015.20.42.30046
8. Antinori S, Mediannikov O, Corbellino M, Raoult D. Všami prenášaná recidivujúca horúčka medzi východoafrickými utečencami v Európe. Travel Med Infect Dis . (2016) 14:110–4. doi: 10.1016/j.tmaid.2016.01.004
9. Cutler SJ. Utečenecká kríza a opätovný výskyt zabudnutých infekcií v Európe. Clin Microbiol Infect . (2016) 22:8–9. doi: 10.1016/j.cmi.2015.10.018
10. Darcis G, Hayette MP, Bontems S, Sauvage AS, Meuris C, Van Esbroeck M a kol. Všami prenášaná recidivujúca horúčka u utečenca zo Somálska prichádzajúceho do Belgicka. J Travel Med. (2016) 23. doi: 10.1093/jtm/taw009
11. Grecchi C, Zanotti P, Pontarelli A, Chiari E, Tomasoni LR, Gulletta M a kol. Všami prenášaná recidivujúca horúčka u utečenca z Mali. Infekcia . (2017) 45:373–6. doi: 10.1007/s15010-017-0987-2
12. Platonov AE, Karan LS, Kolyasnikova NM, Machneva NA, Toporkova MG, Maleev VV, et al. Ľudia infikovaní recidivujúcou horúčkou spirochétou Borrelia miyamotoi , Rusko. Emerg Infect Dis . (2011) 17:1816–23. doi: 10.3201/eid1710.101474
13. Hovius JW, de Wever B, Sohne M, Brouwer MC, Coumou J, Wagemakers A, et al. Prípad meningoencefalitídy spôsobenej recidivujúcou horúčkou spirochétou Borrelia miyamotoi v Európe. Lancet . (2013) 382:658. doi: 10.1016/S0140-6736(13)61644-X
14. Ricklin D, Hajishengallis G, Yang K, Lambris JD. Doplnok: kľúčový systém pre imunitný dohľad a homeostázu. Nat Immunol . (2010) 11:785–97. doi: 10.1038/ni.1923
15. Walport MJ. Doplnok – Prvá z dvoch častí. N Engl J Med . (2001) 344:1058-66. doi: 10.1056/NEJM200104053441406
16. Merle NS, kostol JV, Fremeaux-Bacchi V, Roumenina LT. Systém komplementu I. časť – molekulárne mechanizmy aktivácie a regulácie. Front Immunol . (2015) 6:262. doi: 10.3389/fimmu.2015.00262
17. Pangburn MK, Schreiber RD, Muller-Eberhard HJ. Tvorba počiatočnej C3 konvertázy alternatívnej komplementovej dráhy. Získanie aktivít podobných C3b spontánnou hydrolýzou predpokladaného tioesteru v natívnom C3 . J Exp Med. (1981) 154:856-67. doi: 10.1084/jem.154.3.856
18. Bexborn F, Andersson PO, Chen H, Nilsson B, Ekdahl KN. Prehodnotená teória tick-over: tvorba a regulácia rozpustnej alternatívnej C3 konvertázy komplementu. (C3(H20 ) Bb) . Mol Immunol . (2008) 45:2370–9. doi: 10.1016/j.molimm.2007.11.003
19. Fujita T, Matsushita M, Endo Y. Dráha lektín-doplnok – jeho úloha vo vrodenej imunite a evolúcii. Immunol Rev. (2004) 198:185-202. doi: 10.1111/j.0105-2896.2004.0123.x
20. Kishore U, Ghai R, Greenhough TJ, Shrive AK, Bonifati DM, Gadjeva MG, et al. Štrukturálna a funkčná anatómia globulárnej domény proteínu komplementu C1q. Immunol Lett . (2004) 95:113-28. doi: 10.1016/j.imlet.2004.06.015
21. Kjaer TR, Thiel S, Andersen GR. Smerom k štruktúrne založenému chápaniu lektínovej dráhy komplementu. Mol Immunol . (2013) 56:413–22. doi: 10.1016/j.molimm.2013.05.007
22. Carroll MC. Systém komplementu v regulácii adaptívnej imunity. Nat Immunol . (2004) 5:981–6. doi: 10.1038/ni1113
23. Aleshin AE, DiScipio RG, Stec B, Liddington RC. Kryštálová štruktúra C5b-6 naznačuje štrukturálny základ pre zostavenie komplexu membránového útoku. J Biol Chem . (2012) 287:19642–52. doi: 10.1074/jbc.M112.361121
24. Hadders MA, Bubeck D, Roversi P, Hakobyan S, Forneris F, Morgan BP a kol. Zostavenie a regulácia komplexu membránového útoku založeného na štruktúrach C5b6 a sC5b9. Cell Rep . (2012) 1:200–7. doi: 10.1016/j.celrep.2012.02.003
25. Zipfel PF, Skerka C. Regulátory komplementu a inhibičné proteíny. Nat Rev Immunol . (2009) 9:729–40. doi: 10.1038/nri2620
26. Heinen S, Hartmann A, Lauer N, Wiehl U, Dahse HM, Schirmer S, a kol. Proteín 1. súvisiaci s faktorom H (CFHR-1) inhibuje aktivitu C5 konvertázy komplementu a tvorbu terminálneho komplexu . Krv . (2009) 114:2439-47. doi: 10.1182/blood-2009-02-205641
27. Cserhalmi M, Papp A, Brandus B, Uzonyi B, Jozsi M. Regulácia regulátorov: úloha proteínov súvisiacich s komplementovým faktorom H. Semin Immunol . (2019) 45:101341. doi: 10.1016/j.smim.2019.101341
28. Newman K Jr., Johnson RC. In vivo dôkaz, že intaktná lytická komplementová dráha nie je nevyhnutná pre úspešné odstránenie cirkulujúcej Borrelia turicatae z krvi myší. Infect Immun . (1981) 31:465-9. doi: 10.1128/IAI.31.1.465-469.1981
29. Connolly SE, Benach JL. Špičkové: spirochetémia myšacej recidivujúcej horúčky je odstránená baktericídnymi protilátkami nezávislými od komplementu. J Immunol . (2001) 167:3029-32. doi: 10.4049/jimmunol.167.6.3029
30. McDowell JV, Tran E, Hamilton D, Wolfgang J, Miller K, Marconi RT. Analýza schopnosti druhov spirochét spojených s recidivujúcou horúčkou, vtáčou boreliózou a epizootickým potratom hovädzieho dobytka viazať faktor H a štiepiť c3b. J Clin Microbiol . (2003) 41:3905-10. doi: 10.1128/JCM.41.8.3905-3910.2003
31. Hovis KM, McDowell JV, Griffin L, Marconi RT. Identifikácia a charakterizácia proteínu viažuceho faktor H kódovaného lineárnym plazmidom. (FhbA) spirochéty s recidivujúcou horúčkou Borrelia hermsii . J Bacteriol . (2004) 186:2612-8. doi: 10.1128/JB.186.9.2612-2618.2004
32. Hovis KM, Jones JP, Sadlon T, Raval G, Gordon DL, Marconi RT. Molekulárne analýzy interakcie Borrelia hermsii FhbA s regulačnými proteínmi komplementu faktor H a proteín podobný faktoru H 1. Infect Immun . (2006) 74:2007–14. doi: 10.1128/IAI.74.4.2007-2014.2006
33. Rossmann E, Kraiczy P, Herzberger P, Skerka C, Kirschfink M, Simon MM a kol. Dvojitá väzbová špecifickosť povrchového proteínu získavajúceho regulátor komplementu spojeného s Borrelia hermsii pre faktor H a plazminogén odhaľuje predpokladaný faktor virulencie spirochét s recidivujúcou horúčkou. J Immunol . (2007) 178:7292-301. doi: 10.4049/jimmunol.178.11.7292
34. Grosskinsky S, Schott M, Brenner C, Cutler SJ, Kraiczy P, Zipfel PF, et al. Borrelia recurrentis využíva nový multifunkčný povrchový proteín s antikomplementovým, antiopsonickým a invazívnym potenciálom uniknúť vrodenej imunite. PLoS ONE . (2009) 4:e4858. doi: 10.1371/journal.pone.0004858
35. Grosskinsky S, Schott M, Brenner C, Cutler SJ, Simon MM, Wallich R. Ľudské regulátory komplementu C4b-viažuci proteín a inhibítor C1 esterázy interagujú s novým vonkajším povrchovým proteínom Borrelia recurrentis . PLoS Negl Trop Dis . (2010) 4:e698. doi: 10.1371/journal.pntd.0000698
36. Schott M, Grosskinsky S, Brenner C, Kraiczy P, Wallich R. Molekulárna charakterizácia interakcie Borrelia parkeri a Borrelia turicatae s regulátormi ľudského komplementu. Infect Immun . (2010) 78:2199-208. doi: 10.1128/IAI.00089-10
37. Röttgerding F, Wagemakers A, Koetsveld J, Fingerle V, Kirschfink M, Hovius JW, et al. Imunitný únik Borrelia miyamotoi : CbiA, nový vonkajší povrchový proteín vykazujúci vlastnosti viazania a inaktivácie komplementu. Sci Rep . (2017) 7:303. doi: 10.1038/s41598-017-00412-4
38. Kraiczy P, Wurzner R. Únik komplementu z ľudských patogénnych baktérií získaním regulátorov komplementu. Mol Immunol . (2006) 43:31–44. doi: 10.1016/j.molimm.2005.06.016
39. Lambris JD, Ricklin D, Geisbrecht BV. Doplňte úniky ľudskými patogénmi. Nat Rev Microbiol . (2008) 6:132–42. doi: 10.1038/nrmicro1824
40. Hovingh ES, van den Broek B, Jongerius I. Únos regulačných proteínov komplementu pre bakteriálny imunitný únik. Predné Microbiol. (2016) 7:2004. doi: 10.3389/fmicb.2016.02004
41. Hovis KM, Freedman JC, Zhang H, Forbes JL, Marconi RT. Identifikácia antiparalelnej coiled-coil/loop domény potrebnej na väzbu ligandu FhbA proteínom Borrelia hermsii : ďalší dôkaz o úlohe FhbA v interakcii hostiteľ-patogén. Infikovať imunitu . (2008) 76:2113-22. doi: 10.1128/IAI.01266-07
42. Lewis ER, Marcsisin RA, Campeau Miller SA, Hue F, Phillips A, Aucoin DP a kol. Fibronektín viažuci proteín Borrelia hermsii exprimovaný v krvi myší s recidivujúcou horúčkou. Infect Immun . (2014) 82:2520–31. doi: 10.1128/IAI.01582-14
43. Miller SC, Porcella SF, Raffel SJ, Schwan TG, Barbour AG. Veľké lineárne plazmidy druhov Borrelia , ktoré spôsobujú recidivujúcu horúčku. J Bacteriol . (2013) 195:3629–39. doi: 10.1128/JB.00347-13
44. Nguyen NTT, Rottgerding F, Devraj G, Lin YP, Koenigs A, Kraiczy P. Komplement viažuci a inhibičný proteín CbiA Borrelia miyamotoi degraduje zložky extracelulárnej matrice interakciou s plazmínom(ogénom). Front Cell Infect Microbiol . (2018) 8:23. doi: 10.3389/fcimb.2018.00023
45. Meri T, Cutler SJ, Blom AM, Meri S, Jokiranta TS. Spirochéty s relapsujúcou horúčkou Borrelia recurrentis a B. duttonii získavajú regulátory komplementu C4b-viažuci proteín a faktor H. Infect Immun. (2006) 74:4157-63. doi: 10.1128/IAI.00007-06
46. Fine LM, Miller DP, Mallory KL, Tegels BK, Earnhart CG, Marconi RT. Borrelia hermsii faktor H viažuci proteín FhbA nie je potrebný pre infekčnosť u myší alebo pre rezistenciu na ľudský komplement in vitro . Infect Immun . (2014) 82:3324–32. doi: 10.1128/IAI.01892-14
47. Lawson CL, Yung BH, Barbour AG, Zuckert WR. Kryštalická štruktúra variabilného povrchového proteínu 1. (Vsp1) z Borrelia turicatae spojeného s neurotropizmom . J Bacteriol . (2006) 188:4522–30. doi: 10.1128/JB.00028-06
48. Caine JA, Coburn J. Krátkodobý model infekcie Borrelia burgdorferi identifikuje tkanivové tropizmy a prežitie krvného riečišťa spôsobené adhéznymi proteínmi. Infect Immun . (2015) 83:3184-94. doi: 10.1128/IAI.00349-15
49. Barthel D, Schindler S, Zipfel PF. Plazminogén je inhibítor komplementu. J Biol Chem . (2012) 287:18831–42. doi: 10.1074/jbc.M111.323287
50. Barbour AG, Tessier SL, Stoenner HG. Variabilné hlavné proteíny Borrellia hermsii . J Exp Med . (1982) 156:1312-24. doi: 10.1084/jem.156.5.1312
51. Restrepo BI, Kitten T, Carter CJ, Infante D, Barbour AG. Subtelomérne expresné oblasti lineárnych plazmidov Borrelia hermsii sú vysoko polymorfné. Mol Microbiol . (1992) 6:3299-311. doi: 10.1111/j.1365-2958.1992.tb02198.x
52. Dai Q, Restrepo BI, Porcella SF, Raffel SJ, Schwan TG, Barbour AG. Antigénna variácia Borrelia hermsii nastáva prostredníctvom rekombinácie medzi extragénnymi repetitívnymi prvkami na lineárnych plazmidoch. Mol Microbiol . (2006) 60:1329-43. doi: 10.1111/j.1365-2958.2006.05177.x
53. Kitten T, Barbour AG. Juxtapozícia exprimovaných variabilných antigénových génov s konzervovanou telomérou v baktérii Borrelia hermsii . Proc Natl Acad Sci USA . (1990) 87:6077-81. doi: 10.1073/pnas.87.16.6077
54. Restrepo BI, Carter CJ, Barbour AG. Aktivácia pseudogénu vmp v Borrelia hermsii : alternatívny mechanizmus antigénnej variácie počas recidivujúcej horúčky. Mol Microbiol. (1994) 13:287-99. doi: 10.1111/j.1365-2958.1994.tb00423.x
55. Takahashi Y, Cutler SJ, Fukunaga M. Konverzia veľkosti lineárneho plazmidu v pôvodcovi recidivujúcej horúčky Borrelia duttonii . Microbiol Immunol . (2000) 44:1071-4. doi: 10.1111/j.1348-0421.2000.tb02605.x
56. Pennington PM, Cadavid D, Barbour AG. Charakterizácia VspB Borrelia turicatae , hlavného proteínu vonkajšej membrány exprimovaného v krvi a tkanivách myší. Infect Immun . (1999) 67:4637-45. doi: 10.1128/IAI.67.9.4637-4645.1999
57. Shamaei-Tousi A, Martin P, Bergh A, Burman N, Brannstrom T, Bergstrom S. Spirochéta recidivujúcej horúčky agregujúca erytrocyty Borrelia crocidurae indukuje tvorbu mikroembólií. J Infect Dis . (1999) 180:1929-38. doi: 10.1086/315118
58. Hamase A, Takahashi Y, Nohgi K, Fukunaga M. Homológia génov variabilných hlavných proteínov medzi Borrelia hermsii a Borrelia miyamotoi . FEMS Microbiol Lett . (1996) 140:131-7. doi: 10.1111/j.1574-6968.1996.tb08326.x
59. Wagemakers A, Koetsveld J, Narasimhan S, Wickel M, Deponte K, Bleijlevens B, et al. Variabilné hlavné proteíny ako ciele pre špecifické protilátky proti Borrelia miyamotoi . J Immunol . (2016) 196:4185–95. doi: 10,4049/jimmunol.1600014
60. Vidal V, Scragg IG, Cutler SJ, Rockett KA, Fekade D, Warrell DA a kol. Variabilný hlavný lipoproteín je hlavným faktorom indukujúcim TNF všami prenášanej recidivujúcej horúčky. Nat Med . (1998) 4:1416-20. doi: 10.1038/4007
61. Lescot M, Audic S, Robert C, Nguyen TT, Blanc G, Cutler SJ a kol. Genóm Borrelia recurrentis, pôvodca smrteľnej recidivujúcej horúčky prenášanej všami, je degradovanou podskupinou Borrelia duttonii prenášaných kliešťami. PLoS Genet . (2008) 4:e1000185. doi: 10.1371/journal.pgen.1000185
62. Stoenner HG, Dodd T, Larsen C. Antigénna variácia Borrelia hermsii . J Exp Med . (1982) 156:1297-311. doi: 10.1084/jem.156.5.1297
63. Raffel SJ, Battisti JM, Fischer RJ, Schwan TG. Inaktivácia génov pre antigénnu variáciu v spirochéte s recidivujúcou horúčkou Borrelia hermsii znižuje infekčnosť u myší a prenos kliešťami. PLoS Pathog . (2014) 10:e1004056. doi: 10.1371/journal.ppat.1004056
64. Zückert WR, Lloyd JE, Stewart PE, Rosa PA, Barbour AG. Medzidruhové povrchové zobrazenie funkčných spirochetálnych lipoproteínov pomocou rekombinantnej Borrelia burgdorferi . Infect Immun . (2004) 72:1463-9. doi: 10.1128/IAI.72.3.1463-1469.2004
65. Eicken C, Sharma V, Klabunde T, Owens RT, Pikas DS, Hook M a kol. Kryštalická štruktúra vonkajšieho povrchového proteínu C antigénu lymskej choroby z Borrelia burgdorferi . J Biol Chem . (2001) 276:10010-5. doi: 10.1074/jbc.M010062200
Kľúčové slová: spirochéty, borélie , recidivujúca horúčka, vyhýbanie sa imunite, komplement, antigénna variácia, vrodená imunita, adaptívna imunita
Citácia: Röttgerding F a Kraiczy P (2020) Immune Evasion Strategies of Relapsing Fever Spirochetes. Predné. Immunol. 11:1560. doi: 10.3389/fimmu.2020.01560
Prijaté: 9. apríla 2020; Prijaté: 12. júna 2020;
Zverejnené: 23. júla 2020.
Upravil:
Reinhard Würzner , Innsbruck Medical University, Rakúsko
Skontroloval:
Taru Meri , Univerzita v Helsinkách, Fínsko
Job E. Lopez , Baylor College of Medicine, Spojené štáty
Copyright © 2020 Röttgerding a Kraiczy. Toto je článok s otvoreným prístupom distribuovaný v súlade s podmienkami licencie Creative Commons Attribution License (CC BY) . Použitie, distribúcia alebo reprodukcia na iných fórach je povolená za predpokladu, že sú uvedení pôvodní autori a vlastník autorských práv a že sa cituje pôvodná publikácia v tomto časopise v súlade s uznávanou akademickou praxou. Nie je povolené žiadne použitie, distribúcia alebo reprodukcia, ktorá nie je v súlade s týmito podmienkami.
*Korespondencia: Peter Kraiczy, kraiczy@em.uni-frankfurt.de
Zrieknutie sa zodpovednosti: Všetky tvrdenia vyjadrené v tomto článku sú výlučne tvrdeniami autorov a nemusia nevyhnutne predstavovať tvrdenia ich pridružených organizácií alebo tvrdenia vydavateľa, redaktorov a recenzentov. Žiadny produkt, ktorý môže byť hodnotený v tomto článku, alebo tvrdenie, ktoré môže uviesť jeho výrobca, nie je zaručené ani schválené vydavateľom.


 Florian Röttgerding
Florian Röttgerding Peter Kraiczy
Peter Kraiczy