Abstrakt
Abies alba (Pinaceae), jedľa strieborná, je rozšírený druh nahosemenných rastlín v Európe, ktorý je dôležitý pre svoj ekologický, hospodársky, sociálny a kultúrny význam, ako aj pre svoje využitie na potravinové a bioremediačné účely. Rôzne časti rastliny (listy, konáre, šišky, drevo, kôra) sú tiež farmaceuticky zaujímavé kvôli svojmu zloženiu účinných látok. Za posledné tri desaťročia sa tomuto druhu venovalo pôsobivé množstvo výskumu. Variabilita chemického zloženia éterických olejov (či už pochádzajú z listov, oleoživice z konárov alebo iných častí rastliny) je pôsobivá aj v prípade exemplárov zozbieraných z rovnakej zemepisnej oblasti. Pre éterické oleje pripravené z ihličia alebo vetvičiek a konárov sú hlavnými zlúčeninami limonén, β-pinén, α-pinén, kamfén, β-fellandrén a bornyl acetát, aj keď sa zdá, že ich široké variácie zodpovedajú viacerým chemotypom. Kôra aj drevo sú bohaté na lignany a fenolové zlúčeniny. Matairesinol je zrejme dominantným lignanom v kôre a secoisolariciresinol a lariciresinol sú dominantné vo vzorkách dreva. Farmakologické štúdie so sľubnými výsledkami hodnotili antioxidačný účinok (najmä vďaka éterickým olejom), ale aj antimikrobiálne, protinádorové, probiotické, antidiabetické, antisteatické a antipsoriatické účinky.
1. Úvod
Abies je rod rastlín, ktorý prvýkrát opísal Philipp Miller (1691–1771) v roku 1754. Druhý najväčší rod čeľade Pinaceae, je považovaný za zložitejší v porovnaní s ostatnými rodmi z tejto čeľade a všetky jeho taxóny sú pôvodne rozšírené po celej severnej pologuli [1,2]. Špekuluje sa, že názov Abies je odvodený z latinského slova abeo, čo znamená odísť, a interpretuje sa ako narážka na jeho veľkú výšku. Rod Abies sa odhaduje na 52 druhov s akceptovaným statusom, ku ktorým je potrebné pridať ďalších 58 druhov, ktorých stav ešte nebol zistený [3].
Abies alba (Pinaceae), jedľa strieborná, patrí medzi najrozšírenejšie druhy stromov v Európe (najmä v strednej a východnej Európe, s okrajovými skupinami v južných oblastiach Európy – Balkáne a Pyreneje). V celej Európe je dôležitý pre svoj veľký environmentálny, hospodársky, sociálny a kultúrny význam [4,5]. V strednej Európe je jedľa strieborná najbežnejším druhom stromu, zatiaľ čo vo Švajčiarsku predstavuje asi jednu sedminu celého lesného porastu [6,7].
Mladé exempláre spočiatku rastú pomaly, ale rast sa zrýchľuje, keď sa strom blíži k zrelosti. Podobne ako väčšina nahosemenných rastlín je jednodomý a má rovnú, monopodálnu, stĺpovitú stonku, zatiaľ čo kôra kmeňa je strieborno-sivastá, hladšia u mladých stromov a tmavšia a popraskaná, s ružovkastými zlommi u starších stromov (obrázok 1) [8,9,10]. A. alba patrí medzi najvyššie druhy svojho rodu, dosahuje výšku až 60 m [8]. Jeho listy („ihličie“) pretrvávajú na strome 6–8 rokov a majú tmavozelenú farbu, zatiaľ čo na axiálnej strane vykazujú dva striebristé, pozdĺžne pásy pozostávajúce zo šiestich až ôsmich línií prieduchov (horná strana ihly, lesklá a tmavozelená, je bez prieduchov alebo ich má len niekoľko blízko špičky) (obrázok 2) [8, 10]. Koncové a subterminálne púčiky môžu mať veľmi vysoký obsah živice [9]. Samčie šišky sa zvyčajne vyskytujú pod samičimi šiškami na strome a sú (purpurové) červenkasté až žltkasté, solitérne, previsnuté, podobné amentom, majú peltátové mikrosporofyly, usporiadané v špirále a majú dve mikrosporangie (peľové vaky) [9]. Samičie šišky sa zvyknú vyskytovať v horných oblastiach koruny, sú uložené axilárne, osamelé a v čase opelenia sú umiestnené vzpriamene, sú 3–5 cm dlhé a nazelenalé (s fialovým nádychom, keď sa vyskytujú neskoro na jar) [10,11]. V zrelosti dosahujú samičie šišky dĺžku 8–20 cm a šírku 3–5 cm. Sú hojne živicové a rozpadajú sa v dôsledku špirálovito pripevnených listenov, šupín semien a semien padajúcich z dlhých, drsných, drevitých rachis. Ten zostáva trvalý na konároch [9,10,11]. Semená sú 7–13 mm dlhé, trojuholníkové, lesklé, s červenožltkastými krídlami a 10–14 mm dlhé [11]. Zatiaľ čo kôra, listy a šišky obsahujú živicové kanáliky, drevo takéto kanáliky neobsahuje, s výnimkou traumatizácie [9]. Z pohľadu svojho statusu na červenom zozname, Abies alba Mill. je druh najmenšieho záujmu [12].
Obrázok 1.
Obrázok 2.
V 19. storočí bolo prvýkrát navrhnuté jeho použitie na potravinárske účely vo forme jedlového piva strieborného [13]. Nedávno bol navrhnutý extrakt získaný z jeho ihiel na obohatenie celozrnného chleba v pomere až 35% (prah vnímania chuti), jeho pridanie zvyšuje antioxidačné vlastnosti chleba a technologické vlastnosti cesta a chleba [14]. Jeho kôra bola navrhnutá ako dobrý sorbent na odstraňovanie medi z odpadových vôd so zníženým obsahom medi [15].
Táto naratívna recenzia je založená na komplexnom vyhľadávaní v Pubmed, Web of Science, Scopus a Google Scholar, pričom ako kľúčové slová používali „Abies a alba“, „striebro a jedľa“ alebo „strieborná“. Odkazy na relevantnosť vrátených výsledkov boli použité aj na identifikáciu potenciálne dodatočných odkazov, hoci v malom počte prípadov sme neboli schopní získať úplné texty článkov starších ako z roku 1990. Publikácie v anglickom, francúzskom alebo nemeckom jazyku boli ponechané na analýzu a syntézu v tomto prehľade.
2. Použité diely a metódy extrakcie
Doteraz bolo ihličie jedle striebornej (v rozsiahlych štúdiách) skúmané najmä kvôli obsahu esenciálnych olejov. Namiesto toho sa kôra a drevo, najmä v posledných dvoch desaťročiach, skúmali kvôli obsahu lignanov a fenolov. Zatiaľ čo povaha chemických zlúčenín v každej časti rastliny bude prediskutovaná v časti o fytochémii tohto článku, tu rozoberieme niektoré všeobecné aspekty rôznych častí používaných na účely extrakcie, výťažnosti extrakcie a premenných, ktoré ich ovplyvňujú, a spomenieme niekoľko komerčných extraktov, ktoré vzbudili záujem publikácií.
Hoci sa ihličie menej skúmalo na získanie extraktov s rôznymi rozpúšťadlami, v poslednej dobe sa pokročilo vo využívaní vody na získanie lacných a prírodných extraktov pomocou hydrodynamickej kavitácie [ 16 ], ale ich bioaktivita zatiaľ nebola zaznamenaná. Extrakty získané z ihličia zmesou etanolu a toluénu boli obzvlášť bohaté na látky (vyššie výťažky), najmä terpény, v porovnaní s kôrou a šiškami [ 17 ].
Keďže jedľa strieborná sa používa najmä pre svoje drevo a do istej miery aj pre živicu a éterické oleje, jej kôra je skôr zvyškom alebo vedľajším produktom, ktorý by sa mohol použiť na farmaceutické účely [ 4 ]. Z ekonomického hľadiska sa kôra po dreve považuje za druhý najužitočnejší produkt lesníctva a môže pozostávať z 10 – 15 % kmeňa (z hľadiska objemu) [ 18 ]. Kôra je nielen ekonomicky vedľajším produktom, ktorý sa oplatí využiť, ale na základe údajov z iných rodov Gymnosperm sa odhaduje, že kôra je oveľa bohatšia na extrahovateľné chemické zlúčeniny ako kmeňové drevo, pričom obsahuje až šesťkrát vyššie množstvo ako kmeňové drevo [ 18 ]. Chemické zloženie kôry je ovplyvnené variáciami nielen medzi stromami, ale aj v rámci toho istého jedinca, pretože s vekom sa jej tkanivá menia v štruktúre a zložení [ 18 ]. V prípade monoterpénových zlúčenín z kortikálneho oleoresínu sa uvádza široká variabilita medzi stromami [ 19 ]. Vo všeobecnosti sa zloženie oleoresínu ihličnanov považuje za prejav genotypových informácií, pretože je menej citlivé na vplyvy prostredia. Preto sa považuje za obzvlášť užitočné na chemotaxonomické účely v prípade nahosemenných rastlín, pretože umožňuje charakterizáciu stromov rôzneho pôvodu alebo klonov v rámci toho istého druhu [ 19 ]. Užitočnosť živice produkovanej rôznymi rastlinnými tkanivami ako (chemo)taxonomického nástroja je založená na skutočnosti, že sa zdá, že je pod kontrolou relatívne malého počtu génov a je málo ovplyvnená environmentálnymi premennými [ 19 ].
V kôre stonky a konárov bol zaznamenaný priemerný obsah 16,7 % ( hm./hm . , suchá hmotnosť ) látok extrahovateľných vodou [ 18 ]. Priemerný obsah extrahovateľných látok vo vode sa medzi vnútornou a vonkajšou vrstvou kôry významne nelíšil ( p = 0,62, ANOVA) [ 18 ], hoci sa uvádza, že (u iných druhov) „vnútorná kôra typicky obsahuje viac extrahovateľných látok ako zrelá vonkajšia kôra“ [ 20 ]. n -hexánové „extrakty“ ( v skutočnosti frakcie hydroetanolového extraktu, t. j. lipofilné zlúčeniny) mali tendenciu s výškou výrazne rásť [ 20 ]. Celkový výťažok extrakcie z kôry s použitím hydroetanolovej zmesi (50:50 obj./obj . ) mal tendenciu stúpať od základne stonky smerom ku korune, kde dosahuje relatívne stabilnú úroveň, pričom konáre ho málo ovplyvňujú [ 20 ].
Drevo je ďalším vedľajším produktom viacerých priemyselných odvetví, ktorý by sa mohol preskúmať na extrakciu rôznych chemických zlúčenín, najmä lignanov a fenolov. V porovnaní s inými druhmi jedle jedle ( A. sibirica Ledeb, A. lasiocarpa (Hook.) Nutt. a A. balsamea (L.) Mill.) patria výťažky extrakcie A. alba medzi najnižšie pre beľové drevo (0,70 % sušiny), medzi najvyššie pre jadrové drevo (2,1 % sušiny) a na priemernej úrovni pre živé hrče (13 %) a mŕtve hrče (15 %) [ 21 ].
Uzly sú základňami bočných konárov alebo spiacich púčikov vo vnútri kmeňa stromu. Uzly poskytujú najvyšší výťažok extrakcie s lipofilnými (hexán) aj hydrofilnými (acetón-voda) rozpúšťadlami (20,1 mg/g a 210,4 mg/g), zatiaľ čo beľ poskytuje najnižší výťažok (4,7 mg/g a 14,8 mg/g) [ 22 ]. Výťažok extrakcie jadrového dreva bol len mierne vyšší ako u beľového dreva, zatiaľ čo výťažok extrakcie živých uzlov a dreva konárov bol podobný a o niečo nižší ako u mŕtvych uzlov, ale určite lepší ako u beľového a jadrového dreva [ 22 ]. Výťažok extrakcie acetónu aj hexánu ako rozpúšťadiel mal tendenciu klesať pri uzlovom dreve od základne koruny smerom k vrcholu [ 23 ]. Výťažok extrakcie hexánom z uzlového dreva sa pohyboval medzi 0,13 % a 6,9 % v závislosti od polohy a použitého harmonogramu prerieďovania. Mladé uzly (z vrcholov kmeňa) mali tendenciu mať najnižší výťažok [ 24 ]. Podobný vzťah bol zaznamenaný aj pri extrakcii čistým etanolom; hrče odobraté pod základňou koruny poskytli ešte vyššie výnosy, ale iba v prípade nepreriedených stromov (zatiaľ čo preriedené stromy generovali slabé výnosy) [ 23 ]. Acetónové extrakty získané z dreva hrčov sa značne líšili, medzi 1,02 % a 34,1 %, v závislosti od polohy a harmonogramu preriedenia. Mladé hrče (z vrcholu kmeňa) mali najnižšie výnosy, zatiaľ čo tie blízko živej základne koruny mali tendenciu mať najvyššie výnosy. Riedke zóny hrčov boli bohatšie na extraktívne látky ako husté zóny [ 24 ].
V prípade konárov sa uvádza, že optimálna extrakcia sa dá dosiahnuť pri teplote 100 °C, s použitím pomeru vzorky k vode 1:10 a relatívne dlhého času extrakcie (90 minút). Extrahovateľné zložky konárov klesli približne o 40 %, keďže odobratá časť bola ďalej od kmeňa [ 13 ].
Bolo hlásené, že šišky sú veľmi chudobné na fenoly a flavonoidy [ 17 ], čo by mohlo byť čiastočne zodpovedné za nižší záujem o fytochemický výskum tejto časti rastliny.
Belinal® je priemyselne vyrábaný polyfenolický extrakt získaný z konárov A. alba (t. j. prevažne z dreva) s in vitro antioxidačnými účinkami podobnými účinkom epigalokatechín galátu a lepšími ako resveratrol, kyselina askorbová alebo butylovaný hydroxytoluén [ 25 ] . V skutočnosti ide o frakciu extraktu rozpustnú v etylacetáte pripravenú s vodou pri teplote 70 °C počas 2 hodín a o tomto extrakte boli publikované najmenej dva vedecké práce [ 26 ].
Abigenol ® je ďalší extrakt získaný s vodou podobným spôsobom ako Belinal ® , ale z kôry [ 25 ], pri teplote 70 °C. V skutočnosti ide o etylacetátovú rozpustnú frakciu takto získaného vodného extraktu, suspendovanú v polyetylénglykole 400, čo je dôvod, prečo má tekutú, viskóznu konzistenciu [ 4 ]. Jeho polyfenolický profil je podobný profilu Belinalu ® a jeho antioxidačná aktivita bola údajne vyššia ako u Pycnogenolu (známy komerčný extrakt získaný z kôry Pinus maritima Lam., syn. Pinus pinaster Aiton) [ 25 ].
Extrakt z kmeňa jedle striebornej (SFTE) bol pripravený s použitím vody ako extrakčného rozpúšťadla (DER 100:1) a štandardizovaný v kyseline protokatechovej (7,7 g/l) a kyseline p -kumarovej (3,7 g/l). Je to tiež frakcia vodného extraktu rozpustná v etylacetáte suspendovaná v polyetylénglykole 400, a preto má viskóznu, tekutú konzistenciu [ 27 ]. Je veľmi podobný Belinalu® a Abigenolu® , ktoré sa získavajú rovnakým spôsobom; jediný rozdiel je v prípade Abigenolu® ; extrahovanou časťou rastliny je kôra [ 4 ].
3. Fytochémia
A. alba Mill. vzbudila záujem v oblasti fytochémie v najmenej troch hlavných smeroch: esenciálne oleje obsiahnuté vo viacerých častiach rastliny; polyfenoly (najmä v kôre); a lignany (najmä v kôre a dreve).
3.1. Terpenoidy a ďalšie zložky esenciálnych olejov
Väčšina častí stromu A. alba obsahuje esenciálne oleje s podobným, ale nie identickým zložením a výťažkami, pričom hlavnými zlúčeninami sú monoterpénové uhľovodíky, s menším množstvom seskviterpénových uhľovodíkov a len malým zastúpením oxygenovaných zlúčenín (väčšinou monoterpény, veľmi málo seskviterpénov). Navyše, ako uvidíme, existujú široké inter- a intraindividuálne variácie, pričom mnohé vzorce zloženia zodpovedajú významnému počtu chemotypov, ktoré ešte neboli klasifikované štandardizovaným spôsobom. Prvé fytochemické štúdie týkajúce sa esenciálnych olejov z A. alba Mill. sa zrejme uskutočnili v 70. rokoch 20. storočia v Poľsku a pripisujú sa J. Jończykovi [ 28 , 29 ]. Éterický olej získaný parnou destiláciou čerstvých ihličia (olej z ihličia jedle) je známy pod latinským názvom Abietis albae aetheroleum , zatiaľ čo olej pripravený zo šišiek je známy ako Oleum templini . Z jeho živice sa získava terpentín, známy ako štrasburský alebo alsaský terpentín, ktorý údajne obsahuje esenciálny olej, živicové kyseliny, horké zlúčeniny a kyselinu jantárovú [ 30 ]. Esenciálne oleje obsahujú aj iné časti rastliny, preto budú nižšie diskutované samostatne pre každý zdroj a prípadne aj pre spôsob prípravy.
3.1.1. Esenciálny olej z listov
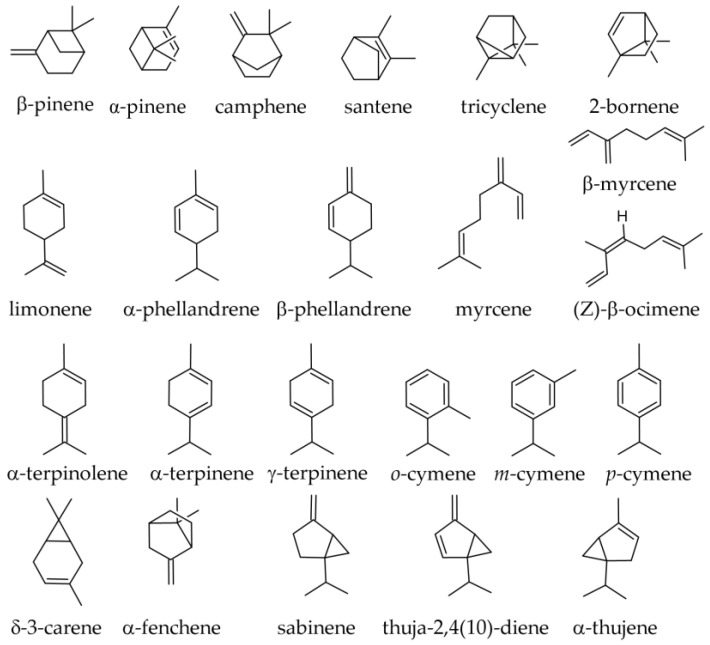
Ihličie je relatívne bohaté na monoterpény a niektoré z týchto monoterpénov sa uvoľňujú do ovzdušia. Štúdia zameraná na odhad emisií monoterpénov z jedľového lesa strieborného vo Francúzsku uviedla, že hlavné emisie monoterpénov pozostávali z limonénu (viac ako 50 % všetkých emisií), α-pinénu a kamfénu. Tento druh sa považuje za slabého emitora monoterpénov (približne 1 μg g −1 h −1 v suchom stave), pričom jeho hladiny sú podobné ako u iných ihličnanov [ 31 ]. Vo vzorkách odobratých z Francúzska (les Collet d’Allevard) boli nasledujúce monoterpénové uhľovodíky hlásené ako emitované listami tohto druhu (pomocou efluviálneho vzorkovača nad hladinou; predpokladá sa, že emitované terpény do značnej miery odrážajú terpény obsiahnuté v ihličí) ( obrázok 3 ): α-pinén (52 %); limonén a +β-felandrén (neoddelené v GC analýze) (21,1 %); β-pinén (12,2 %); myrcén (1,9 %); kamfén (0,9 %); a v stopách tricyklén a sabinén [ 32 ].
Obrázok 3.
Esenciálne oleje získané z listov majú rôzne uplatnenie v kozmetickom priemysle, najmä ako prísada do osviežovačov vzduchu, vôní/parfumov a domácich produktov [ 33 ]. Bolo ocenené, že spomedzi esenciálnych olejov získaných z hlavných európskych ihličia má olej pripravený z listov A. alba „asi najpríjemnejšiu vôňu“. Vďaka tejto vlastnosti sa tento olej v Európe široko používa v rôznych produktoch, ako sú osviežovače vzduchu, dezodoranty, prípravky do kúpeľa, inhalačné produkty určené na liečbu kašľa a prechladnutia, ako aj iné farmaceutické prípravky, ako sú masti [ 34 ].
Esenciálny olej získaný hydrodestiláciou z ihličia A. alba zozbieraného v Albánsku mal príjemnú vôňu a jeho farba sa pohybovala od svetložltej po bezfarebnú. Výťažky sa pohybovali medzi 0,36 a 0,88 ml/g čerstvého tkaniva pre ihličie zozbierané počas zimy (november – december) a medzi 0,13 a 0,40 pre ihličie zozbierané počas leta (máj – jún). V súlade s predchádzajúcim výskumom to odhaľuje pokles produkcie oleoresínu z ihličia od jesene do jari a vyšší výťažok pre zimné vzorky ako pre letné vzorky [ 19 ].
Všetky analyzované vzorky z rôznych európskych krajín uvádzali ako hlavné zlúčeniny limonén (34 – 55 % – Nemecko, Rakúsko, Francúzsko, Grécko) alebo β-pinén (20 – 33 % – Srbsko, Čierna Hora) [ 1 ]. Ďalšími významnými zlúčeninami boli aj monoterpény: kamfén (15 – 17 %); α-pinén (11 – 17 %); a bornylacetát (9 – 14 %) [ 1 ]. Vo vzorke pripravenej z listov a vetvičiek kórejských vzoriek bol dominantnou zlúčeninou bornylacetát (30,31 %), nasledovaný kamfénom (19,81 %), 3-karénom (13,85 %) a tricyklénom [ 35 ]. Esenciálny olej z A. alba sa zdá byť chudobnejší na α-pinén (31,2 ± 5,8 % oproti 18,0 ± 3,6 %) ako z A. cephalonica Loudon, zatiaľ čo obsah β-pinénu sa významne nelíši; Namiesto toho bol esenciálny olej z A. alba bohatší na limonén + β-felandrén (21,7 ± 11,1 % oproti 10,4 ± 4,8 %) [ 2 ]. Obsah β-pinénu aj α-pinénu sa zdá byť nižší v esenciálnom oleji z ihlíc A. alba v porovnaní s obsahom v ihličkách A. x borisii-regis Mattf. (30,6 ± 11,0 oproti 38,0 ± 10,8 % pre β-pinén; 18,0 ± 3,6 oproti 24,2 ± 4,9 % pre α-pinén); namiesto toho sa zdá, že obsah limonénu + β-felandrénu je vyšší v A. alba ako v A. x borisii-regis (21,7 ± 11,1 oproti 12,9 ± 5,3) [ 2 ].
V prípade monoterpénových zlúčenín v listových esenciálnych olejoch sa uvádza široká variabilita medzi jednotlivými stromami. V štúdii vykonanej v Albánsku mali tri populácie podobný profil, pričom vedúce zlúčeniny boli v nasledujúcom poradí: β-pinén > kamfén > α-pinén > limonén; štvrtá populácia mala odlišný chemický profil esenciálneho oleja, pričom vedúce zlúčeniny boli v nasledujúcom poradí: β-pinén > α-pinén > limonén > kamfén [ 19 ]. Vo vzorkách z Čiernej Hory bola zaznamenaná nasledujúca variácia vedúcich zlúčenín: β-pinén > α-pinén > kamfén > bornylacetát > limonén [ 34 ]. Ďalšia štúdia založená na vzorkách z Južných Karpát a Balkánskeho polostrova tiež uviedla zdanlivo rovnaký vzorec: β-pinén > kamfén > α-pinén > limonén [ 2 ], zatiaľ čo štúdia založená na vzorkách z južného Balkánu (Grécko a Srbsko) zistila mierne odlišný vzorec: β-pinén > kamfén > limonén > α-pinén, pričom rozdiel medzi limonénom a α-pinénom bol taký malý, že boli prakticky v rovnakom pomere; v tejto vzorke však bola vysoká hladina α-fenchylacetátu (14,2 %), vyššia ako obsah limonénu alebo α-pinénu [ 36 ]. Vzorka z Talianska, ako aj komerčná vzorka zrejme z Nemecka, uviedli nasledujúce poradie vedúcich zlúčenín: limonén > α-pinén > kamfén > β-pinén [ 37 , 38 ]. Vo vzorkách z Botanickej záhrady Univerzity vo Würzburgu sa hlavné zlúčeniny menili nasledovne: limonén > kamfén > α-pinén > santén (hladina β-pinénu bola veľmi nízka, iba 0,5 %) [ 38 ].
β-pinén mal vyššie hladiny v albánskych vzorkách ako vo vzorkách z juhovýchodnej Európy a Kalábrie; namiesto toho boli α-pinén a kamfén v albánskych vzorkách hlásené v nižších množstvách ako vo vzorkách z východnej a juhovýchodnej Európy. Wolf (1994) uvádzal β-felandrén s priemernou koncentráciou 5,4 % (ale s vysokou variabilitou, od 0 % do 54 %), zatiaľ čo v albánskych vzorkách úplne chýbal [ 19 ]. Vo vzorkách z Južných Karpát a Balkánskeho polostrova bol β-felandrén hlásený spolu s limonénom v množstve 21,7 % ± 11,1 [ 2 ], ale zjavne chýbal vo vzorke pochádzajúcej z Talianska [ 37 ].
V esenciálnych olejoch z listov získaných zo vzoriek zozbieraných počas leta z niekoľkých krajín Južných Karpát a Balkánskeho polostrova (Rumunsko, Srbsko, Severné Macedónsko a Bulharsko) J. S. Nikolicom a kol. (2021) boli hlavnými zlúčeninami prevažne monoterpénové uhľovodíky (95,8 % ± 2,4 %); oxygenované monoterpény predstavovali 2,6 ± 1,8 %, seskviterpénové uhľovodíky 1,5 ± 1,4 %, zatiaľ čo oxygenované seskviterpény boli detegované iba v stopách [ 2 ]. Namiesto toho vo vzorkách esenciálnych olejov iba zo Srbska (tiež z ihličia zozbieraného počas leta) Z. S. Mitic a kol. (2022) uviedli rôzne pomery terpénových zlúčenín: 66,4 % monoterpénových uhľovodíkov; 12,1 % oxygenovaných monoterpénov; 18,0 % seskviterpénových uhľovodíkov; a 1 % oxygenovaných seskviterpénov [ 39 ].
V esenciálnych olejoch získaných zo vzoriek zozbieraných v Albánsku autori identifikovali viac ako 60 zlúčenín, čo zodpovedá približne 92 – 96 % oleoresínu. V esenciálnom oleji získanom z albánskych vzoriek predstavovali monoterpénové uhľovodíky 70,3 – 77,2 % vzoriek pripravených z ihličia zozbieraného v zime, ale iba 40,3 – 47,9 % vzoriek pripravených z ihličia zozbieraného v lete [ 19 ]. Vo vzorkách z Južných Karpát a Balkánskeho polostrova, hoci boli tiež zozbierané v lete – začiatkom jesene, predstavovali monoterpénové uhľovodíky 95,8 ± 2,4 % [ 2 ]. Vo vzorkách zozbieraných na južnom Balkáne (Grécko a Srbsko) okolo konca augusta predstavovali monoterpénové uhľovodíky 84,1 % [ 36 ]. To isté platilo aj pre vzorky zozbierané vo Francúzsku (les Collet d’Allevard) počas leta (polovica júna): autori informovali výlučne o monoterpénoch [ 32 ]. Naopak, zatiaľ čo seskviterpénové uhľovodíky predstavovali 2,8 – 5,1 % albánskych zimných vzoriek, ich podiel pokrýval 23,0 – 32,6 % letných vzoriek [ 19 ]. Avšak vo vzorkách z Južných Karpát a Balkánskeho polostrova predstavovali seskviterpénové uhľovodíky iba 1,5 ± 1,4 % [ 2 ]. Okysličené monoterpény mali tendenciu kolísať menej, 10,1 – 22,05 % pre zimné vzorky a 11,3 – 21,4 % pre letné vzorky; avšak v prípade jednotlivých zlúčenín, ako je uvedené nižšie, môžu stále existovať značné rozdiely medzi zimnými a letnými vzorkami [ 19 ].
Monoterpénové uhľovodíky zaznamenané v zimných a letných vzorkách z Albánska sú uvedené v tabuľke 1. Väčšina monoterpénových uhľovodíkov je v letných vzorkách zastúpená menej, pričom α-terpinolén je jediný, ktorého podiel sa v letných vzorkách zvýšil.
Tabuľka 1.
Zmena obsahu monoterpénových uhľovodíkov v albánskych vzorkách ihličkového esenciálneho oleja zozbieraného v rôznych ročných obdobiach [ 19 ].
| Monoterpén | Podiel v zimných vzorkách (%) | Podiel v letných vzorkách (%) |
|---|---|---|
| β-pinén | 24,7 – 31,6 | 14,5 – 18,4 |
| kamfén | 10,8 – 17,2 | 3,0 – 5,4 |
| limonén | 9,6 – 17,5 | 6,5 – 10,2 |
| α-pinén | 9,5 – 11,7 | 8,4 – 15,2 |
| santén | 2.1 – 3.2 | 0,3 – 1,0 |
| tricyklén | 1,3 – 1,8 | 0,3 – 0,7 |
| myrcén | 1,0–1,2 | 0,6 – 0,8 |
| α-terpinolén | 0,6 – 0,8 | 0,8 – 1,7 |
| α-felandrén | 0,1 – 0,2 | 0,1 – 0,2 |
| Z-ß-ocimene | stopy – 0,2 | stopy |
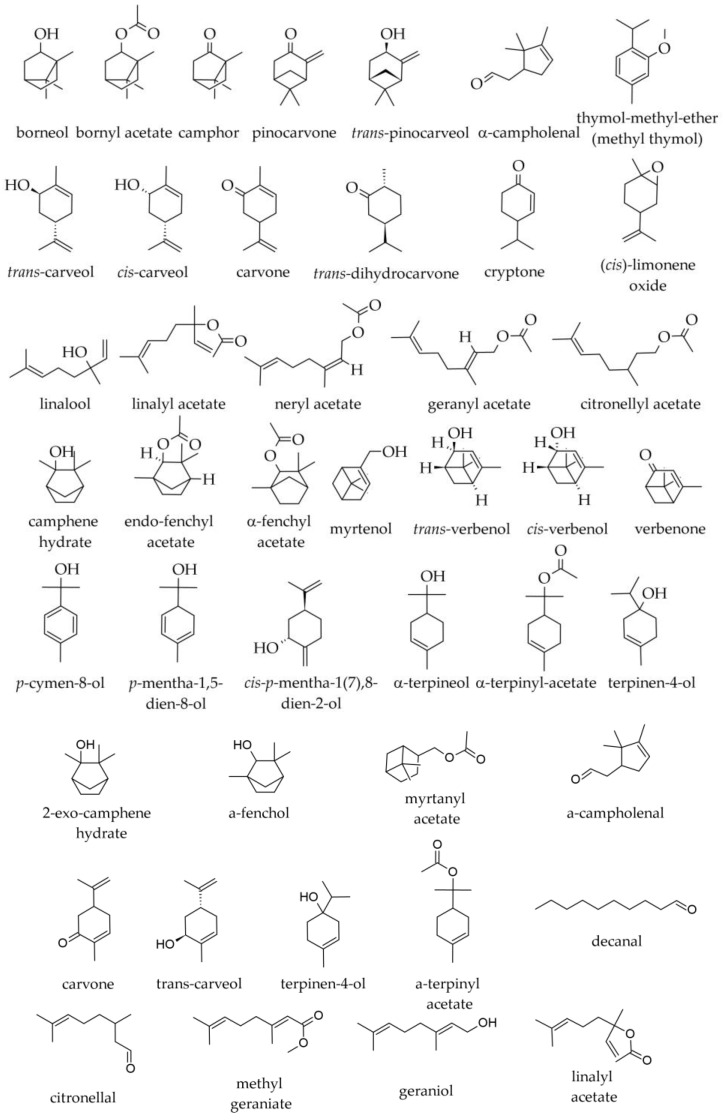
Okysličené monoterpény zaznamenané v albánskych zimných a letných vzorkách sú zhrnuté v tabuľke 2. V porovnaní so zimnými vzorkami vykazujú letné vzorky oxidované monoterpény zvýšenie aj zníženie. Hladiny bornylacetátu mali tendenciu pozitívne korelovať s kamfénom, zatiaľ čo bornylacetát aj kamfén negatívne korelovali s obsahom borneolu a α-terpineolu [ 19 ].
Tabuľka 2.
Zmena obsahu okysličených monoterpénov v albánskych vzorkách ihličkového esenciálneho oleja zozbieraného v rôznych ročných obdobiach [ 19 ].
| Oxidovaný monoterpén | Podiel v zimných vzorkách (%) | Podiel v letných vzorkách (%) |
|---|---|---|
| Bornylacetát | 5,68 – 17,6 % | 1,6 – 2,4 % |
| α-Terpineol | 1,21 – 2,0 % | 1,21 – 2,0 % |
| Borneol | 0,4 – 1,7 % | 2,3 – 5,5 % |
| α-terpinylacetát | 0,35 – 1,4 % | 0,2 – 0,4 % |
| Linalool acetát | 0,1 – 1,0 % | Stopy |
| Linalool | 0,1 – 0,92 % | stopy – 0,2 % |
| Kamfénhydrát | stopy – 0,2 % | 0,2 – 0,4 % |
| p -Ment-1-én-9-ol-acetát | stopy – 0,2 % | 0,2 – 0,7 % |
| α-kamfolenal | stopy – 0,1 % | 0,2 – 0,5 % |
| Gáfor | stopy – 0,1 % | 0,1 – 0,2 % |
| cis -Pinokamfón | stopy – 0,1 % | 0,1 – 0,3 % |
| Terpín-4-ol | stopy – 0,1 % | stopy – 0,4 % |
| Endo-fenchol | Stopy | 0,2 – 0,4 % |
| Trans-pinokarveol | Stopy | 0,4 – 1,0 % |
Vo vzorkách ihličia A. alba zozbieraných v Južných Karpatoch a na Balkánskom polostrove/južnom Balkáne počas leta a začiatku jesene boli zaznamenané nasledujúce monoterpénové uhľovodíky: β-pinén (19,8 – 30,6 %); limonén + β-felandrén (21,7 %); limonén (11,0 %); kamfén (10,9 – 19,2 %); α-pinén (10,9 – 18,0 %); α-fenchylacetát (0,0 – 14,2 %); tricyklén (1,7 – 3,9 %); α-tujén (stopy – 2,8 %); myrcén (0,9 – 1,3 %); santén (0,5 – 0,8 %); terpinolén (0,4 – 0,9 %); α-felandrén (0,1 – 0,9 %); α-terpinén (stopy – 0,2 %); γ-terpinén (stopy – 0,2 %); a chýbajúci alebo v stopách o -cymén a sabinén [ 2 , 36 , 39 ]. Vo vzorkách z Albánska bol obsah limonénu odhadnutý na 10,7 % a β-felandrénu na 6,3 % [ 36 , 39 ].
Medzi okysličenými monoterpénmi a inými neterpenickými okysličenými zlúčeninami ( obrázok 4 ) sa vo vzorkách z Južných Karpát a Balkánskeho polostrova/južného Balkánu našli: bornylacetát (1,9 – 8,8 %); borneol (0,9 – 2,8 %); valenén (0,0 – 1,8 %); α-terpinylacetát (stopy – 0,4 %); α-terpineol (stopy – 0,3 %); geranylacetát (stopy – 0,2 %); (E)-2-hexenal (0,1 %); linalool (stopy – 0,1 %); kamfénhydrát (stopy – 0,1 %); linalylacetát (stopy – 0,1 %); metyltymol (t. j. tymol metyléter, 0,0 – 0,1 %); nerylacetát (0,0 – 0,1 %); terpinen-4-ol (stopy – 0,1 %); a iba v stopách gáfor, δ-3-karén, citronellol, cyklohexanol, eukalyptol, α-fenchol, 2-heptylacetát, hexanal, hexanol, (Z)-3-hexenol, cis – p -ment-2-én-1-ol, trans – p- ment-2-én-1-ol, 2-nonanón a cis -pinokamfón [ 2 , 36 , 39 ]. Vo vzorke komerčného pôvodu z Nemecka predstavoval α-terpinylacetát 0,5 %, zatiaľ čo v esenciálnom oleji pripravenom z ihličia z Botanickej záhrady Univerzity vo Würzburgu nebol zistený [ 38 ].
Obrázok 4.
Podobné zloženie ako tie, ktoré sú uvedené vyššie, s veľkými kvantitatívnymi odchýlkami, bolo zaznamenané aj vo vzorkách iného pôvodu, pričom ročné obdobie často nebolo uvedené. Vo vzorke zo Slovenska bol α-pinén hlavnou zlúčeninou, prítomnou vo vyššom množstve ako β-pinén [ 40 ]. Vo vzorke z Talianska a komerčnej vzorke z Nemecka bol limonén hlavnou zlúčeninou (32,5 – 34,08 %), nasledovaný α-pinénom (30,8 – 31,66 %), kamfénom (5,76 – 11,2 %), β-pinénom (2,99 – 7,5 %), β-karyofylénom (4,21 – 5,8 %) a bornylacetátom (1,29 – 4,2 %) [ 37 , 38 ]. V rôznych vzorkách boli zaznamenané nasledujúce monoterpénové uhľovodíky: α-pinén (2,13 – 30,8 %); β-pinén (0,5 – 32,8 %); α-limonén (6,1 – 54,74 %); kamfén (5,76–19,81 %); tricyklén (0,52–12,90 %); a-fenchén (0,0–2,6 %); santén (0,01–5,00 %); o -cymén (0,0–1,5 %); β-felandrén (stopy – 4,9 %); γ-terpinén (stopy – 1,1 %); δ-3-karén (0,0–13,85 %); β-myrcén (0,6–1,86 %); a-terpinolén (0,3–0,5 %); 2-bornén (bornylén, 0,0–0,2 %); p -cymén (0,0–0,57 %); a-terpinén (0,0–1,24 %); a v stopách, ak nie úplne chýbajú, (Z)-β-farnesén, β-fenchén, pseudolimonén, α-felandrén a sabinén [ 35 , 37 , 38 , 40 ]. V kórejskej vzorke mali δ-3-karén a tricyklén nezvyčajne vysoké hladiny (13,85 % a 12,90 %) [ 35 ] v porovnaní s veľkým počtom európskych vzoriek, kde mali oveľa nižšie hodnoty (pod 3,5 %).
Okysličené monoterpény zaznamenané vo vzorkách iného pôvodu boli bornylacetát (0,96 – 9,0 %), α-terpineol (0,2 – 0,6 %), citronelylacetát (0,0 – 0,4 %), gáfor (0,0 – 0,2 %), endo-fenchylacetát (0,2 %), cis -limonénoxid (0,2 %), trans- pinokarveol (stopy – 0,2 %), borneol (0,1 %), α-kamfolenal (0,0 – 0,1 %), kryptón (0,0 – 0,1 %), pinokarvón (0,0 – 0,1 %) a v stopách karvón, p -cymen-8-ol, myrtenol, 4-terpinenol, trans -verbenol a verbenón [ 34 , 37 , 38 ].
Komerčná vzorka od nemeckej spoločnosti (Farfalla Essential AG) uvádzala nasledujúce monoterpény, ale v zdrojovom dokumente nebolo uvedené ani ročné obdobie, ani časti rastliny, z ktorých bol olej získaný: δ-limonén (40,0 %); α-pinén (32,8 %); (+)-kamfén (6,48 %); β-pinén (2,82 %); santén (1,20 %); a myrcén (1,09 %) [ 41 ].
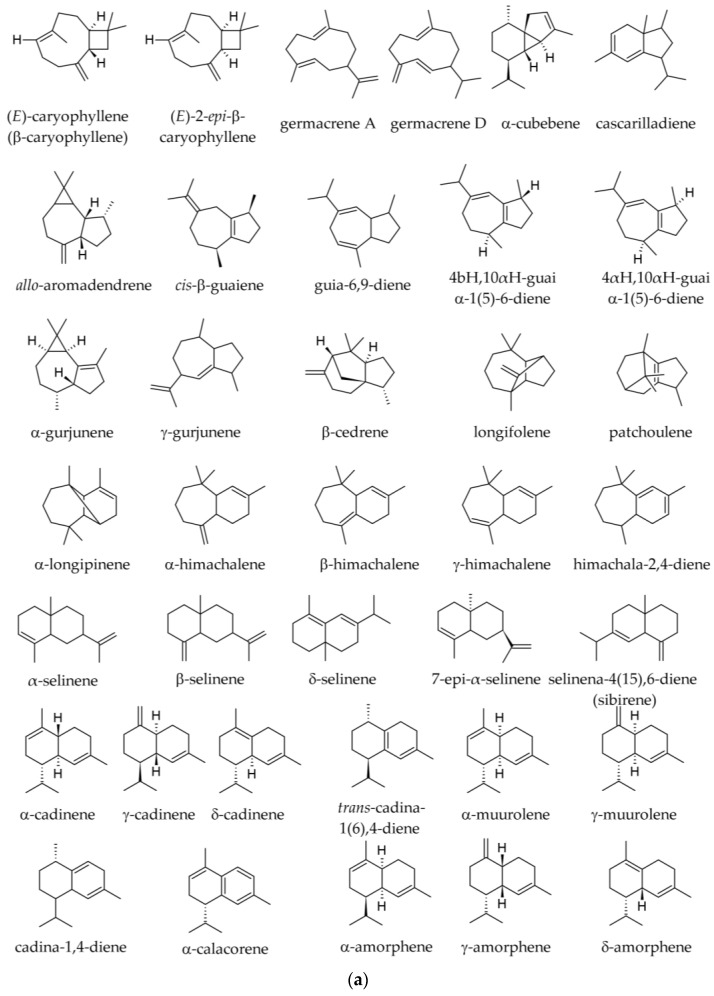
V tabuľke 3 je znázornená variácia seskviterpénových uhľovodíkov ( obrázok 5 ) podľa sezóny vo vzorkách získaných z Albánska . V týchto vzorkách boli E-karyofylén a α-humulén prítomné vo všetkých populáciách a pozitívne korelovali. 10- epi -γ-eudesmol sa medzi populáciami značne líšil a mal tendenciu zvyšovať sa od severu na juh [ 19 ]. V kórejskej vzorke boli hlásené nasledujúce seskviterpénové uhľovodíky: karyofylén (2,18 %); santén (bicyklo[2.2.1]hept-2-én,2,3-dimetyl) (1,64 %); β-elemén (0,72 %); humulén (0,20 %); (E)-β-farnesén (0,0–0,2 %); valenén (0,13 %); α-bisabolén (0,12 %); a aromadendrén (0,05 %) [ 35 ].
Obrázok 5.
Tabuľka 3.
Zmena obsahu seskviterpénových uhľovodíkov v albánskych vzorkách ihličkového esenciálneho oleja zozbieraného v rôznych ročných obdobiach [ 19 ].
| Seskviterpénový uhľovodík | Podiel v zimných vzorkách (%) | Podiel v letných vzorkách (%) |
|---|---|---|
| E-karyofylén | 0,6 – 1,2 % | 7,2 – 12,8 % |
| Nerylacetát | chýbajúce/stopy | 0,2 – 0,6 % |
| α-himachalén | stopy – 0,2 % | stopy – 0,28 % |
| α-humulén | 0,3 – 0,6 % | 4,7 – 7,2 % |
| 9- epi -E-karyofylén (2- epi- (E)-β-karyofylén) | stopy | stopy – 0,4 % |
| y-gurjunén | stopy | stopy – 0,4 % |
| y-muurolén | stopy | 0,5 – 0,9 % |
| Germakrén D | 0,1 – 0,3 % | 0,1 – 0,3 % |
| β-selinén | stopy – 0,2 % | 0,6 – 1,0 % |
| cis -β-guaién | stopy – 0,4 % | 0,3 – 1,2 % |
| α-selinén | 0,0–0,2 % | 0,5 – 1,0 % |
| β-himachalén | 0,2 – 0,4 % | 0,7 – 1,2 % |
| Germakrén A | stopy – 0,1 % | stopy – 0,4 % |
| y-kadínén | stopy – 0,1 % | 0,1 – 1,2 % |
| δ-kadínén | 0,3 – 0,5 % | 2,0 – 3,5 % |
| Cadina-1,4-dién | 0,1 % | 0,2 – 0,3 % |
| α-kadínén | stopy | 0,2 – 0,3 % |
| α-kalakorén | stopy – 0,3 % | 0,1 – 0,3 % |
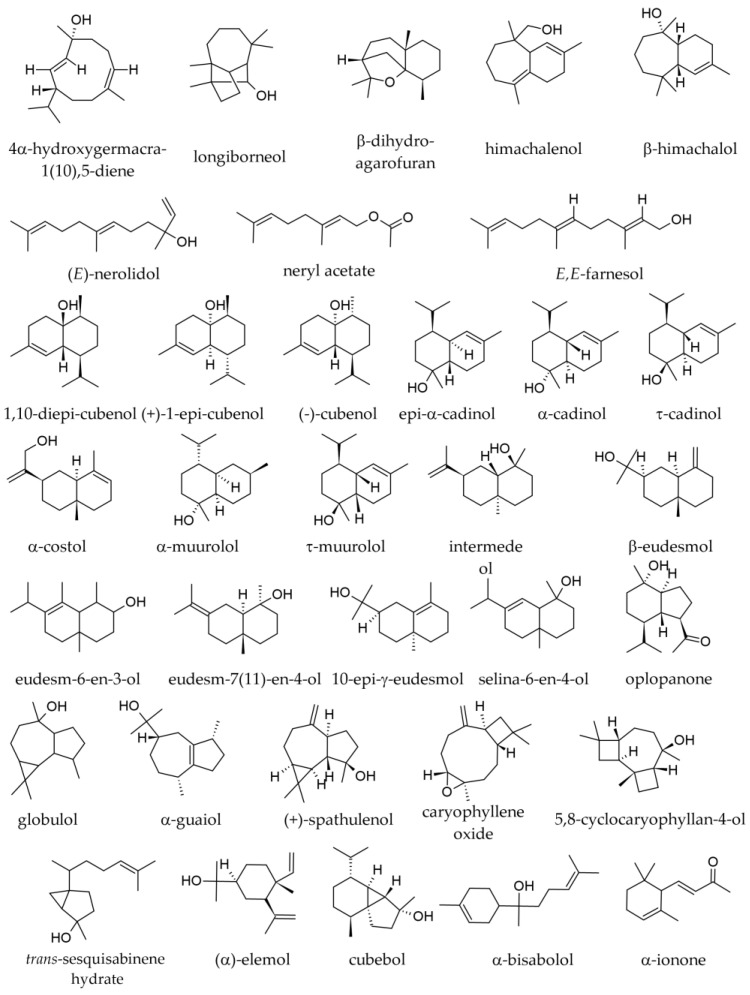
Nasledujúce seskviterpénové deriváty (väčšinou uhľovodíky) boli zaznamenané vo vzorkách z Južných Karpát a Balkánskeho polostrova (letné vzorky): (E)-β-karyofylén (0,9–5,7 %); δ-kadinén (stopy – 1,7 %); globulol (0,0–0,5 %); germakrén D (stopy – 0,9 %); γ-kadinén (stopy – 0,8 %); 10- epi -γ-eudesmol (0,0–0,8 %); α-selinén (stopy – 0,6 %); γ-elemén (0,0–0,5 %); α-ionón (0,0–0,4 %); longifolén (stopy – 0,4 %); β-elemén (0,0–0,3 %); α-himachalén (stopy – 0,3 %); humulén (0,2–2,6 %); aristolén (0,0–0,7 %); δ-amorfén (stopy – 0,3 %); β-eudesmol (0,0 – 0,3 %); γ-gurjunén (0,0 – 0,3 %); β-himachalén (stopy – 0,3 %); β-dihydro-agarofurán (stopy – 0,2 %); α-kopán (stopy – 0,2 %); γ-himachalén (stopy – 0,2 %); α-muurolén (stopy – 0,2 %); γ-muurolén (0,0 – 0,2 %); sibirén (stopy – 0,2 %); α-ylangén (stopy – 0,2 %); himachala-2,4-dién (0,1 – 1,0 %); α-longipinén (0,1 – 0,6 %); β-selinén (0,1 %); trans -kadín-1(6),4-dién (0,0 – 0,1 %); α-kadinén (0,0–0,1 %); oxid karyofylénu (0,0–0,1 %); α-muurolol (0,0–0,1 %), 7- epi -α-selinén (0,0–0,1 %); a v stopách α-amorfén, cyklosativén, 6,9-guaiadién, longicyklén, cis -muurola-3,5-dién, β-selinén, δ-selinén [ 2 , 36 , 39 ]. V stopách bol zaznamenaný diterpén (5,9-1 O)-kaur-15-én [ 36 ]. Vo vzorkách iného pôvodu boli zaznamenané nasledujúce seskviterpénové uhľovodíky: (E)-karyofylén (β-karyofylén, 2,78–7,0 %); β-himachalén (0,0–2,59 %); α-himachalén (0,00–1,10 %); α-longipinén (0,0–0,9 %); longifolén (0,1–0,6 %); γ-humulén (0,0–1,1 %); a-humulén (0,2–2,02 %); 5-kadinén (0,0–0,6 %); a-gurjunén (0,0–0,4 %); y-muurolén (0,0–0,3 %); a-selinén (0,0–0,1 %); a v stopách α-amorfén, β-bisabolén, α-kadinén, α-kopaén a α-muurolén, β-selinén (stopy) [ 34 , 37 , 40 , 41 ].
V albánskych vzorkách odobratých z rôznych ročných období majú okysličené seskviterpény ( obrázok 6 ) tendenciu byť menej zastúpené v zimných vzorkách ako v letných ( tabuľka 4 ). V slovenských, talianskych a francúzskych vzorkách bol ako okysličený seskviterpén uvedený iba karyofylénoxid (0,2 – 1,0 %) [ 34 , 34 , 37 , 38 , 40 ].
Obrázok 6.
Tabuľka 4.
Zmena obsahu okysličených seskviterpénov v albánskych vzorkách ihličkového esenciálneho oleja zozbieraného v rôznych ročných obdobiach [ 19 ].
| Zložené | Zimné vzorky (% zloženie) | Letné vzorky (% zloženie) |
|---|---|---|
| E-nerolidol | stopy – 0,4 % | 0,1 – 0,4 % |
| 10- epi -γ-eudesmol | 1,4 – 5,4 % | 0,7 – 3,9 % |
| epi -α-kadinol | stopy – 0,6 % | 0,2 – 0,3 % |
| kubenol | 0,2 – 0,5 % | stopy – 0,1 % |
| himačalol | 0,3 – 0,8 % | stopy – 0,2 % |
| α-kadinol | 0,3 – 0,42 % | 2,7 – 4,2 % |
| E,E-farnezol | stopy – 0,3 % | 0,3 – 1,0 % |
V analýze 16 vzoriek esenciálnych olejov z ihličia komerčného pôvodu malo najvyššie koncentrácie nasledujúcich desať zlúčenín: limonén (6,1 – 54,7 %); α-pinén (0,5 – 2,8 %); β-pinén (7,4 – 31,7 %); kamfén (5,8 – 17,3 %); bornylacetát (0,4 – 14,2 %); β-felandrén (0,01 – 4,9 %); β-karyofylén (0,1 – 4,2 %); tricyklén (0,5 – 2,6 %); myrcén (0,7 – 2,5 %); a α-terpineol (0,07 – 2,3 %) [ 42 ]. Porovnanie s vyššie uvedenými údajmi naznačuje, že týchto 16 vzoriek nereprezentuje široké rozdiely, s ktorými sa možno stretnúť v porovnaní s inými komerčnými alebo nekomerčnými vzorkami. Preto špecifikácia iba názvu a zdroja esenciálneho oleja bez minimálnych informácií o hlavných zložkách nemá veľký význam pre pochopenie povahy esenciálneho oleja.
Chemické analýzy esenciálnych olejov zvyčajne uvádzajú stopové množstvá zlúčenín, o ktorých sa predpokladá, že sú spôsobené niekoľkými faktormi. Patria sem neúplné potlačenie recesívnych génov, nízka aktivita enzýmov, ktoré nie sú špecifické, a chemické artefakty, ktoré sa môžu vyskytnúť počas extrakčných a izolačných procesov. Z týchto dôvodov niektorí autori pri zisťovaní chemických profilov ignorujú zlúčeniny prítomné iba v stopových množstvách [ 19 ].
Okrem mono- a seskviterpénov, ktoré tvoria takmer všetky esenciálne oleje, bolo v esenciálnom oleji získanom z listov a vetvičiek zaznamenaných niekoľko neterpenických zlúčenín, 4-hydroxy-4-metyl-2-pentanón (0,06 %) a androstan-17-1,3-etyl-3-hydroxy-,(5a) (0,12 %) (identifikácia však bola založená iba na hmotnostných spektrách) [ 35 ].
3.1.2. Esenciálny olej z vetvičiek a konárov
E. Duquesnoy a kol. (2007) analyzovali 53 rôznych vzoriek esenciálneho oleja získaného hydrodestiláciou z vetvičiek zozbieraných zo šiestich korzických lesov. Výťažok esenciálneho oleja, odhadnutý na čerstvom základe ( w / w ), sa pohyboval medzi 0,10 a 0,26 % v závislosti od miesta zberu. Najnižšie výťažky boli zaznamenané pri vzorkách z Carbini (0,10 – 0,13 %), zatiaľ čo najvyššie výťažky boli pri vzorkách z Rospigliani (0,13 – 0,26 %). Spomedzi nich autori vybrali dve vzorky s veľmi odlišnými chromatografickými profilmi a identifikovali 65 chemických zlúčenín, ktoré pokrývali veľkú väčšinu zloženia olejov (98,1 % a 95,4 %, respektíve 44 a 52 chemických zlúčenín) [ 1 ]. Oba oleje obsahovali prevažne monoterpénové uhľovodíky (90,8 % a 85,0 %) s výrazne menším obsahom okysličených monoterpénov (5,1 % a 6,3 %); Seskviterpény predstavovali iba 1,8 % a 3,2 %, pričom prevažnú väčšinu tvorili uhľovodíky a malú časť tvorili oxygenované zlúčeniny (1,6 % + 0,2 % a 2 % + 0,7 % pre obe vzorky). Na základe analýzy hlavných komponentov aplikovanej na 53 vzoriek autori identifikovali dva klastre, ktoré pokrývali 64 % a 36 % všetkých vzoriek. Prvý klaster sa vyznačoval vysokou hladinou limonénu (priemer 46,1 % ± 8,1), ako aj kamfénu (16,9 % ± 4,6) a α-pinénu (12,2 % ± 4,3). Druhý klaster sa vyznačoval vysokými hladinami kamfénu (priemer 23,7 % ± 5,0), α-pinénu (18,5 % ± 9,8), limonénu (15,6 % ± 7,9), β-felandrénu (23 %) a β-pinénu (12 %). Výskumníci nezistili žiadny vzťah medzi príslušnosťou ku klastru a geografickým pôvodom vzoriek. Esenciálne oleje s prevahou limonénu boli zaznamenané aj vo vzorkách z Francúzska, Rakúska a Grécka, zatiaľ čo oleje patriace do klastra II zrejme neboli predtým zaznamenané [ 1 ].
V dvoch vzorkách, ktoré Duquesnoy a kol. (2007) vybrali spomedzi 53 vzoriek korzického pôvodu, boli na základe ich odlišných chromatografických profilov zaznamenané nasledujúce monoterpénové zlúčeniny: limonén (9,3 – 68,3 %); kamfén (9,1 – 20,6 %); α-pinén (6,4 – 19 %); β-felandrén (0,4 – 15,1 %); β-pinén (0,8 – 11,6 %); santén (1,3 – 4,3 %); bornylacetát (2,3 – 2,7 %); tricyklén (1,1 – 3,0 %); myrcén (1,0 – 2,2 %); citronelylacetát (0,5 – 1,5 %); α-terpineol (0,3 – 0,8 %); citronellol (0,2 – 0,5 %); terpinolén (0,0 – 0,8 %); geranylacetát (0,0–0,5 %); linalool (0,2–0,3 %); dekanal (kaprinový aldehyd, 0,1 %); 2-exo-kamfénhydrát (0,0–0,2 %); karvón (0,0–0,2 %); citronellal (0,0–0,2 %); α-felandrén (0,0–0,2 %); borneol (0,0–0,1 %); α-kamfolenal (0,1 %); terpinén-4-ol (0,1 %), trans -karveol (0,0–0,1 %); α-fenchol (0,0–0,1 %); geraniol (0,0–0,1 %); metylgeraniát (0,0–0,1 %); linalylacetát (0,0–0,1 %); myrtanylacetát (0,0–0,1 %); α-terpinén (0,0–0,1 %); α-terpinylacetát (0,0–0,1 %); p -cymén (stopy – 0,1 %); γ-terpinén (stopy – 0,1 %). Sabinén, 1,8-cineol, (E)-β-ocimén a p -cymenén boli v niektorých vzorkách detegované iba v stopách alebo úplne chýbali [ 1 ].
V esenciálnych olejoch z vetvičiek boli zaznamenané nasledujúce seskviterpény: (E)-β-karyofylén (0,4–0,7 %); (E)-β-farnezén (stopy – 0,4 %); α-longipinén (stopy – 0,3 %); β-himachalén (0,2 %); junipinén (0,2 %); δ-kadinén (0,1–0,3 %); longiborneol (0,1–0,3 %); longifolén (0,0–0,3 %); α-humulén (0,1–0,2 %); cembrén (stopy – 0,2 %); γ-humulén (0,0–0,2 %); β-bisabolén (0,0–0,1 %); α-kadinol (0,0–0,1 %); τ-kadinol (0,0–0,1 %); (E)-2- epi -β-karyofylén (0,0–0,1 %); β-cedrén (0,0–0,1 %); izocembrén (0,00–0,1 %); kubebol (0,0–0,1 %); (Z,E)-α-farnesén (0,0–0,1 %); himachalenol (0,0–0,1 %); τ-muurolol (0,0–0,1 %). Longicyklén, β-elemén, trans- kalamenén, karyofylénoxid a manoyloxid boli uvedené iba v stopách alebo úplne chýbali v niektorých vzorkách [ 1 ]. Nepodarilo sa nám nájsť žiadne chemické znázornenie pre „junipinén“ ani žiadne synonymá.
Dodekanal bol hlásený v množstvách 0,2 – 0,4 %. Izopimaradién bol jediným diterpénom zisteným v kvantifikovateľných množstvách (0,0 – 0,1 %); diterpény boli zistené v stopách iba v jednej vzorke a v druhej vzorke v podiele približne 0,4 % [ 1 ].
3.1.3. Extrakty superkritickej tekutiny z vetvičiek
Superkritické fluidné extrakty (SFE) získané z vetvičiek sa značne líšia v porovnaní s esenciálnymi olejmi získanými z rovnakých častí rastlín, ako dokazuje analýza dvoch vzoriek patriacich do dvoch vyššie uvedených korzických klastrov. V oboch vzorkách SFE je podiel monoterpénových uhľovodíkov nižší ako v esenciálnom oleji a v niektorých prípadoch úplne chýbajú. Napríklad limonén tvoril 43,5 % esenciálneho oleja v prvej vzorke, ale v zodpovedajúcej vzorke SFE iba 17,5 %; v druhej vzorke to bolo 15,6 % a v zodpovedajúcej vzorke SFE iba 5,6 %. α-Pinén predstavoval 18,0 % a 11,4 % vzoriek esenciálnych olejov, ale iba 3,4 % a 2,6 % vzoriek SFE. Podobne sa koncentrácie kamfénu znížili z 13,7 % a 15,7 % v esenciálnych olejoch na iba 1,9 % a 3,9 % v SFE. Bez ohľadu na jeho koncentráciu v esenciálnom oleji, v SFE bola koncentrácia β-felandrénu približne polovičná v porovnaní s esenciálnym olejom (14,4 % v esenciálnom oleji, 7,0 % v SFE, 0,2 % v esenciálnom oleji a 0,1 % v SFE). Santén, ktorý sa nachádza v dvoch esenciálnych olejoch v koncentráciách 3,6 % a 3,0 %, sa v SFE našiel v 0,1 % alebo len v stopách [ 43 ]. α-Terpineol, ktorý sa v esenciálnych olejoch zistil v nízkych množstvách (0,7 %, 1,2 %), je v SFE úplne nezistený [ 43 ].
Naopak, seskviterpénové zlúčeniny sa extrahujú oveľa efektívnejšie v SFE, takže v esenciálnych olejoch predstavovali 4,1 % a 3,0 %, ale v SFE 27,3 % a 30,0 %. Okrem toho bolo v SFE detegovaných iba 11 seskviterpénových uhľovodíkov (v pomeroch pohybujúcich sa medzi 0,2 % a 5,2 %), zatiaľ čo v esenciálnom oleji chýbali, čo naznačuje, že nie všetky seskviterpénové uhľovodíky sa mohli extrahovať v esenciálnych olejoch; týchto 11 molekúl boli prevažne deriváty selinanu, kadinénu a himachalánu [ 43 ].
V SFE boli zistené nasledujúce monoterpénové uhľovodíky: limonén (5,6 – 17,7 %); β-felandrén (0,1 – 7,0 %); kamfén (1,9 – 3,9 %); α-pinén (2,6 – 3,4 %); β-pinén (0,4 – 2,7 %); tricyklén (0,3 – 0,5 %); myrcén (0,3 – 0,4 %); santén (stopy – 0,1 %) [ 43 ]. V SFE boli zaznamenané nasledujúce monoterpénové kyslíkaté deriváty: bornylacetát (1,0 – 8,1 %); geranylacetát (0,0 – 1,7 %); citronelylacetát (0,7 – 1,1 %); borneol (0,0 – 0,9 %); linalylacetát (0,0–0,4 %), geraniol (0,0–0,3 %), terpinolén (0,1 %), citronellol (0,0–0,1 %) a dekanal (0,0–0,1 %). V SFE boli zaznamenané nasledujúce seskviterpénové uhľovodíky: (E)-β-karyofylén (5,6–6,3 %); β-selinén (3,8–5,2 %); himachala-2,4-dién (2,4–2,6 %); α-longipinén (2,3 %); α-humulén (2,1–2,2 %); γ-humulén (1,6–2,0 %); δ-kadinén (0,7–1,8 %); longifolén (1,3–1,7 %); β-himachalén (0,9–1,3 %); α-selinén (0,7–1,1 %). γ-kurkumén (0,4–1,0 %); α-himachalén (0,7–0,9 %); γ-himachalén (0,2–0,8 %); ar -himachalén (0,4–0,7 %). Zdá sa, že longiborneol (0,0–2,6 %) bol jediným okysličeným seskviterpénom v SFE. Diterpén cis -abienol bol tiež detegovaný iba v SFE, a to vo významných množstvách (17,3 % a 7,5 % oboch SFE), ale nie v oboch esenciálnych olejoch, pravdepodobne kvôli jeho nízkej prchavosti [ 43 ].
3.1.4. Oleoresin z kôry a triterpenoidy z kôry
Mnohé ihličnany si vyvinuli živicové kanáliky a sú schopné ukladať významné množstvo oleoresínu, keď je rastlina zranená alebo poškodená [ 44 ] a A. alba z tohto pravidla nerobí výnimku. Chemické zloženie oleoresínu z kôry sa líši od zloženia oleoresínu z ihličia. V albánskych vzorkách (pozri vyššie, časť 3.1.4 ) bolo identifikovaných 33 zlúčenín, čo zodpovedá 95 – 97 % esenciálneho oleja. Podobne ako esenciálny olej z ihličia, aj zimné vzorky mali bohatšie zloženie (väčší počet zlúčenín) ako letné vzorky [ 19 ].
Esenciálny olej pozostáva prevažne z monoterpénových uhľovodíkov (64,2 – 85,8 %), zatiaľ čo okysličené monoterpény predstavujú (v priemere) menej ako 2 % oleja. Identifikované monoterpénové uhľovodíky s ich podielom v zimných a letných vzorkách sú uvedené v tabuľke 5. V albánskych vzorkách bol zaznamenaný rastúci trend obsahu limonénu zo severu na juh, zatiaľ čo u kamfénu bol zaznamenaný opačný trend. Medzi α-pinénom a β-pinénom (pravdepodobne spoločný biosyntetický pôvod) boli zaznamenané významné negatívne korelácie, zatiaľ čo medzi α-pinénom a limonénom, ako aj u β-pinénu a limonénu boli zaznamenané významné negatívne korelácie [ 19 ].
Tabuľka 5.
Zmena obsahu monoterpénových uhľovodíkov v albánskych vzorkách esenciálneho oleja z kôry zozbieraného v rôznych ročných obdobiach [ 19 ].
| Monoterpénový uhľovodík | Podiel v zimných vzorkách (%) | Podiel v letných vzorkách (%) |
|---|---|---|
| α-pinén | 12,2 – 37,2 | 23,1 – 47,1 |
| kamfén | 0,3 – 0,9 | 0,4–0,9 |
| β-pinén | 14,9 – 36,6 | 18,3 – 30,0 |
| myrcén | 1,4–1,6 | 1,4 – 2,6 |
| limonén | 6,9 – 35,3 | 5,5 – 41,4 |
| α-terpinolén | stopy – 0,1 | stopy |
Seskviterpénové uhľovodíky predstavovali 14,8 – 30,8 % esenciálnych olejov pripravených zo zimných vzoriek a 13,5 – 18,0 % esenciálnych olejov pripravených z letných vzoriek. Identifikované seskviterpénové uhľovodíky s ich podielom v zimných a letných vzorkách sú uvedené v tabuľke 6. Robustná pozitívna korelácia bola zaznamenaná pre E-karyofylén a α-humulén, dve zlúčeniny, o ktorých je známe, že majú spoločný biosyntetický pôvod, a takáto korelácia bola zaznamenaná aj u iných nahosemenných rastlín [ 19 ].
Tabuľka 6.
Zmena obsahu seskviterpénových uhľovodíkov v albánskych vzorkách esenciálneho oleja z kôry zozbieraného v rôznych ročných obdobiach [ 19 ].
| Zložené | Podiel v zimných vzorkách (%) | Podiel v letných vzorkách (%) |
|---|---|---|
| α-longipinén | stopy – 0,3 % | stopy – 0,1 % |
| nerylacetát | stopy – 0,2 % | stopy – 0,1 % |
| E-karyofylén | 3,4 – 8,9 % | 3,2 – 3,9 % |
| α-himachalén | stopy – 0,3 % | stopy |
| α-humulén | 1,6 – 3,9 | 1,6 – 1,9 |
| y-muurolén | 0,3 – 0,6 % | stopy – 0,1 % |
| germakrén D | 5,9 – 15,2 % | 6,9 – 12,1 % |
| β- cis -guaién | stopy – 0,7 % | stopy – 0,1 % |
| α-selinén | stopy – 0,3 % | stopy – 0,2 % |
| β-himachalén | stopy – 0,2 % | stopy – 0,1 % |
| γ-kadinén | 0,2 – 0,6 % | 0,1 – 0,3 % |
| δ-kadínén | 0,6 – 1,1 % | stopy – 0,3 % |
| α-kadínén | 0,3 – 0,6 % | 0,2 – 0,4 % |
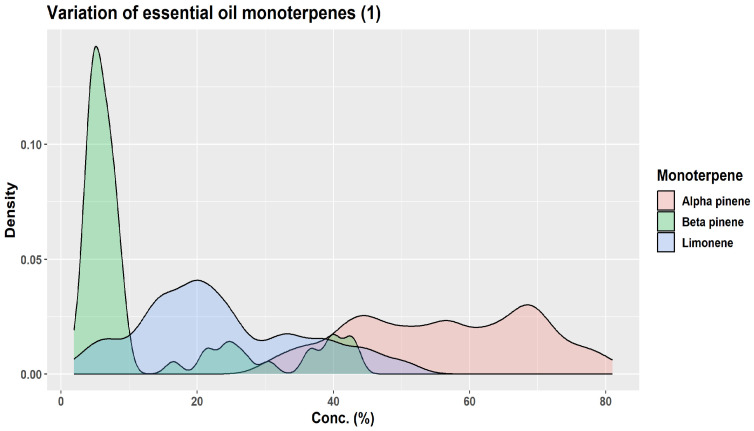
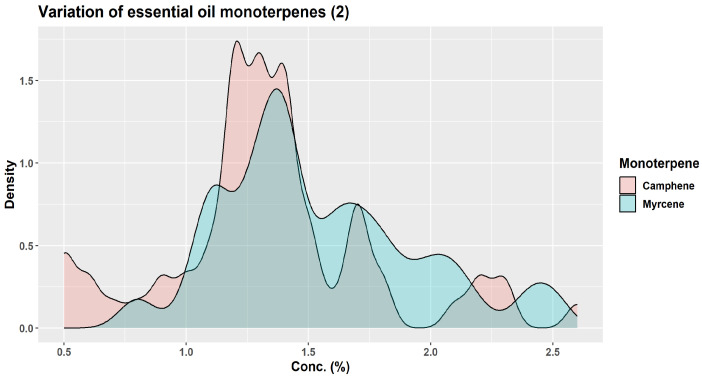
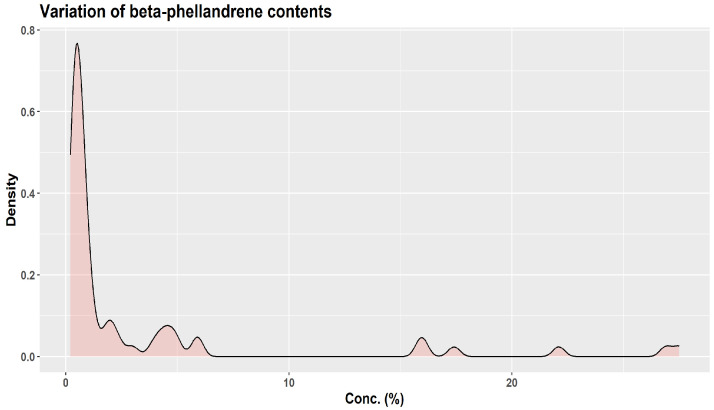
Približne pred tromi desaťročiami KJ Lang študoval chemickú variabilitu veľkého počtu (viac ako 1500) vzoriek oleoresínu získaných z dvojročnej kôry vetvičiek A. alba pochádzajúcich zo 63 rôznych zdrojov v Európe [ 1 , 45 ]. Pomocou nekontrolovanej klastrovej analýzy KJ Lang rozlíšil tri „skupiny pôvodu“: skupinu I (Bavorský les, východné predhorie Álp a určité oblasti Álp); skupinu II (západné predhorie Álp, Alpy, Čierny les, Francúzsko, severné Taliansko a zóny východnej Európy); a skupinu III (stredné a južné Taliansko plus balkánske krajiny) [ 45 ]. Na základe kvantitatívnej variability iba šiestich monoterpénov (α-pinén, β-pinén, limonén, kamfén, myrcén, β-felandrén) autori naznačili prítomnosť 13 chemotypov a štyroch hlavných skupín v závislosti od európskeho regiónu pôvodu: západo-stredná, východo-stredná, juho-východná a stredojužná [ 1 ]. Ich výsledky sú obzvlášť zaujímavé, pretože ukazujú, aké široké môžu byť variácie v šiestich monoterpénoch ( obrázok 7 , obrázok 8 a obrázok 9 ) [ 45 ].
Obrázok 7.
Obrázok 8.
Obrázok 9.
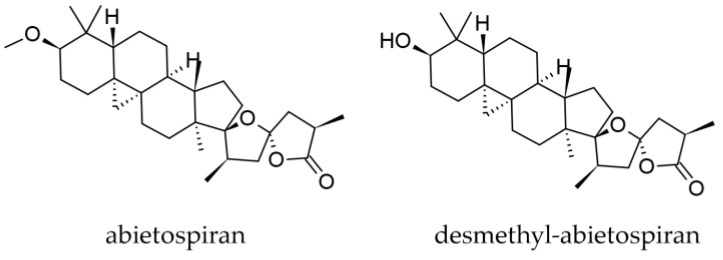
Okrem bohatého mono- a seskviterpénového profilu v oleoresíne boli z kôry izolované a doteraz identifikované dva triterpenoidy, abietospirán a desmetylabietospirán ((23S,-25R)-3α-hydroxy-17,23-epoxy-9,19-cyklo-9β-lanostan-26,23-olid) ( obrázok 10 ) [ 46 , 47 ].
Obrázok 10.
3.1.5. Esenciálne oleje zo šišiek
Šišky (šupiny šišiek) sú chudobnejšie na esenciálny olej ako semená, s výťažnosťou oleja okolo 0,5 – 0,75 % pre A. alba a 0,5 % pre A. koreana EH Wilson [ 33 , 48 ]. Esenciálny olej pripravený hydrodestiláciou zo šišiek A. alba obsahuje podobný podiel celkových monoterpénov (94,4 %) ako semená (93,6 %), ale v šiškách je podiel okysličených monoterpénov v porovnaní so semenami zvýšený (8,0 % oproti 0,2) [ 33 ].
Hlavnými zložkami éterického oleja zo šišky sú, ako už bolo spomenuté, monoterpény: α-pinén (50 – 57,1 %), limonén (10,1 – 27,2 %), β-pinén (6,5 – 9,4 %) a verbenón (2,5 – 6,4 %) [ 33 ]. Ďalšie monoterpény zaznamenané v menších množstvách v éterických olejoch zo šišiek sú β-myrcén (0,3–0,7 %), trans- pinokarveol (0,7–3,2 %), trans -verbenol (0,7 %), α-kamfolenal (0,6 %), kamfén (0,3–0,5 %), trans -karveol (0,5 %), tuja-2,4(10)-dién (dehydrosabinén, 0,5 %), α-fenchén (0,0–0,4 %), borneol (0,3–1,4 %), α-kamfolenal (0,3 %), limonénoxid (0,3 %), p -menta-1,5-dién-8-ol (0,3 %), myrtenol (0,3–1,0 %), α-terpineol (0,3 %), cis -karveol (0,2 %), p- cymén (0,2–0,4 %), karvón (0,0–0,3 %), α-felandrén. (stopy – 0,2 %), pinokarvón (0,2 %), sabinén (stopy – 0,2 %), cis- verbenol (0,2 – 0,8 %), bornylacetát (stopy – 0,1 %), trans- dihydrokarvón (karvomentón, 0,1 %), m-cymén (0,1 %), p -cymén-8-ol (0,1 %), globulol (0,0 – 0,1 %), cis – p- menta-1(7),8-dién-2-ol (0,1 %), terpinolén (0,1 %) a tricyklén (stopy – 0,1 %) [ 33 , 48 ]. Nasledujúce látky boli hlásené iba v stopových množstvách (alebo v niektorých vzorkách chýbali): gáfor; δ-kar-3-én; p -cymenén; linalool; p -menta-1,3,8-trién; cis – p- menta-2,8-dién-1-ol; trans – p- menta-2,8-dién-1-ol; trans – p -ment-2-én-1-ol; (E)-β-ocimén; β-felandrén; pinokamfón; santén; γ-terpinén; terpinén-4-ol; a α-tujén [ 33 , 48 ]. Analýza esenciálnych olejov uvoľňovaných šiškami zozbieranými vo Francúzsku ukázala podobné zloženie, pokiaľ ide o hlavné zložky, a to α-pinén (57,2 %), limonén + β-felandrín (27,7 %) (tieto dva monoterpény neboli pri GC analýze oddelené), β-pinén (8,5 %), myrcén (3,3 %), kamfén (1,3 %) a v stopách tricyklén a sabinén [ 32 ].
Seskviterpénové uhľovodíky sú menej zastúpené v šiškách ako v semenách (2,0 oproti 5,20), ale kyslíkaté seskviterpény sú tiež o niečo vyššie v éterickom oleji zo šišiek ako v oleji získanom zo semien (1,5 % oproti 1,0 %) [ 33 ]. Popredné seskviterpény sú selin-6-en-4-ol (0,6 %), longifolén (stopy – 0,4 %), δ-kadinén (0,1–0,3 %), γ-kadinén (0,2 %), α-kadinol (stopy – 0,2 %), (E)-β-karyo,2-himaléndie (E)-karyofyléndie (0,2-40. (0,2 %), α-humulén (stopy – 0,2 %), α-amorfén (0,1 %), α-kadinén (0,1 %), τ-kadinol (0,0–0,1 %), β-karyofylénoxid (0,0–0,1 %) α-kopaén (stopy – 0,1 kubických percent α-bene), – 0,1-0,1 kubických percent 1-epikubenol (cubenol, 0,1 %), β-elemén (stopy – 0,1 %), elemol (stopy – 0,1 %), α-guaiol (0,0–0,1 %), β-himachalol (stopy – 0,1 %), intermedeol (0,1 %), α-longipinén (stopy – 0,1 %), τ-muurolol (0,0–0,1 %), α-muurolén (0,1 %), 0–0,10,1% pačulén (0,1 %) a ô-selinén (0,1 %) [ 33 , 48 ]. Agarospirol, γ-amorfén, δ-amorfén, allo -aromadendrén, bicykloelemén, β-bisabolén, 7αH,10βH-kadina-1(6),4-dién, kadina-1,4-dién, α-calacorén, transkórén , β – calaracén 2- epi -(E)-β-karyofylén, karyofylénoxid, kascarilladién, α-cedrén, 1,10-diepicubenol, epizonarén, α-fenchol, germacrén D, 4α-hydroxygermakra-1(10),5-dién, guadién,6,9 4αH,10αH-guaia-1(5)-6-dién, β-himachalén, γ-himachalén, humulénoxid, longiborneol, β-longipinén, 13- epi -manoyloxid, γ-muurolén, sativén, selina-4(15),6-dién (sibirén), spathulenol a α-ylangén boli v niektorých vzorkách zaznamenané v stopových množstvách alebo úplne chýbali [ 33 , 48 ].
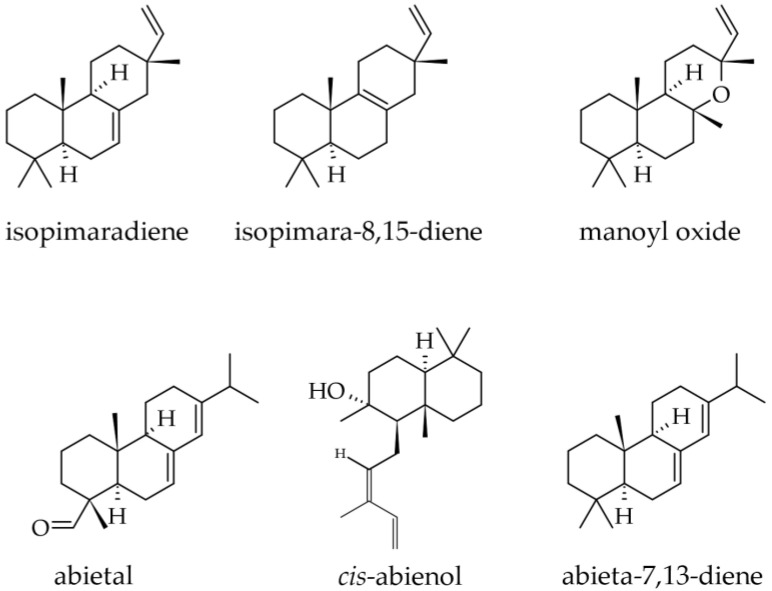
Esenciálny olej zo šišky bol jediný, ktorý obsahoval malé, ale kvantifikovateľné množstvá diterpénov, a to uhľovodíkov (0,2 %) aj oxygenovaných (0,2 %). Pozostávajú z abietalu (0,0 – 0,2 %), manoyloxidu (0,0 – 0,2 %), abieta-7,13-diénu (0,1 %), izopimara-8,15-diénu (0,1 %) ( obrázok 11 ), zatiaľ čo abieta-8(14),13(15)-dién sa našiel iba v stopách [ 33 ].
Obrázok 11.
Zloženie esenciálnych olejov zo šišiek je podobné u A. alba a A. koreana , s rozdielmi, ktoré sa zdajú byť malé, v hlavných zlúčeninách (50 % α-pinénu v A. alba oproti 56,8 % v A. koreana ; 5,6 % β-pinénu v A. alba oproti 11,2 % v A. koreana ; 27,2 % limonénu v A. alba oproti 13,0 % v A. koreana ) [ 33 ]. Rôzne analýzy vykonané na tých istých dvoch druhoch z rovnakej geografickej oblasti v rôznych rokoch ukázali konzistentné výsledky s malými rozdielmi (napr. 57 % α-pinénu v teste vykonanom o päť rokov skôr pre A. alba ) [ 48 ].
3.1.6. Esenciálne oleje zo semien
Semená boli hlásené ako veľmi bohaté na esenciálne oleje (7,4 %, 12,4 %, 14,3 % – v závislosti od pôvodu a času zberu), pričom ich obsah bol v jednej publikácii z Poľska približne trikrát vyšší ako obsah v esenciálnych olejoch semien A. koreana EHWilson (približne 3,8 %) [ 33 , 48 ]. Zdá sa, že množstvo esenciálneho oleja je tiež o niečo vyššie v semenách A. alba ako v semenách A. pinsapo subsp. marocana (Trab.) Emb. a Maire (syn. A. marocana Trab.) (5,3 % uvedené v jednej práci) [ 48 , 49 ] alebo A. nordmanniana (Steven) Spach (6,0 %) [ 48 ]. Esenciálny olej má živicovú, drevitú, príjemnú vôňu s decentným nádychom citrónovo-pomarančovej vône, ktorá môže súvisieť s prítomnosťou limonénu [ 33 ]. Esenciálny olej zo semien obsahuje predovšetkým monoterpénové uhľovodíky (88 % v jednej vzorke a viac ako 93 % v inej, obe z rôznych regiónov Poľska a zozbierané v rôznych rokoch) a seskviterpény (približne 6 %), na rozdiel od A. koreana , kde druhú najväčšiu skupinu zložiek tvoria okysličené deriváty (v éterickom oleji zo semien A. alba predstavovali okysličené monoterpény iba 0,2 % a okysličené seskviterpény 1,1 %) [ 33 , 48 ].
Hlavnou zlúčeninou je (−)-limonén (70,1 – 82,9 %); prevažne jeho ľavotočivý izomér (viac ako 96 % celkového limonénu) (v absolútnom vyjadrení bol (+) limonén zaznamenaný ako 2,1 – 2,6 %). Ďalšie monoterpénové zložky esenciálneho oleja zo semien sú α-pinén (6,3–11,5 % v rôznych vzorkách), β-pinén (1–2,1 %), β-myrcén (2,8–3,1 %), bornylacetát (0,1 %), kamfén (0,1 % v jednej vzorke, iba stopy v dvoch vzorkách), gáfor (0,1 % alebo iba stopy), α-fenchén (0,1 % v dvoch vzorkách, chýba v jednej), terpinolén (0,1 %), α-terpinylacetát (0,1 %), tricyklén (0,1 % v jednej vzorke, iba stopy v dvoch rôznych vzorkách), verbenón (0,1 %, stopy alebo chýba) a v stopách (alebo chýba v niektorých vzorkách) cis -anetol, trans -anetol, apiol, borneol, bornylacetát, karvakrol, trans -karveol, cis -karveol , karvón, trans -karvón epoxid, citronellol, citronelylacetát, p -cymén, eugenol, fenchone, geranial, geranyl acetát, linalool, mentol, cis – p -ment-2,8-dien-1-ol, trans – p- ment-2-en-1-ol, myrtenol, neral, (E)-β-ocimen, α-felanderverén, trans -bineopinol, trans-bineopinol y-terpinén, a-terpineol, a-terpinylacetát, tymol a cis -verbenol [ 33 , 48 ].
Medzi seskviterpénmi boli hlásené nasledujúce: δ-kadinén (0,9 – 1,5 %); guaiol (0,0 % až 1,5 %); spathulenol (0,0 % až 1,1 %); selín-6-én-4-ol (0,6 %); γ-kadinén (0,5 – 1,0 %); (E)-β-karyofylén (0,5–0,8 %); pačulén (stopy – 0,7 %); alo -aromadendrén (0,0 % až 0,5 %); α-kubebén (zo stôp – 0,4 – 0,5 %); δ-selinén (0,5 %); α-amorfén (stopy – 0,3 %); β-selinén (0,3 %); β-elemén (0,2 – 0,3 %); β-himachalol (stopy – 0,3 %); 1-epikubenol (stopy – 0,2 %); globulol (0,0 % až 0,2 %); himachala-2,4-dién (stopy – 0,2 %); α-humulén (0,2 – 0,7 %); izogermakrén D (neprítomnosť do 0,3 %); longifolén (0,2 %); α-muurolén (stopy – 0,2 %); γ-amorfén (0,1 %); δ-amorfén (0,1 %); α-kadinén (stopy – 0,1 %); α-kadinol (stopy – 0,4 %); 2- epi- (E)-p-karyofylén (0,1 %); β-karyofylénoxid (0,0 % až 0,1 %); kaskarilladién (0,1 %); guaja-6,9-dién (0,1 %); 4αH,10αH-guaia-1(5)-6-dién (0,1 %); 4βH,10αH-guaia-1(5)-6-dién (0,1 %); 4α-hydroxygermakra-1(10),5-dién (0,1 %); β-himachalén (0,1 %); γ-himachalén (0,1 %); a-longipinén (stopy – 0,1 %); γ-muurolén (stopy – 0,1 %); selina-4(15),6-dién (0,1 %); a α-ylangén (stopy – 0,1 %) [ 33 , 48 ]. Nasledujúce seskviterpény boli hlásené iba v stopových množstvách alebo v niektorých vzorkách chýbali: agarospirol; aromadendrén; ( E ) -trans -bergamotol; bicykloelemén; kadína-1,4-dién; kadína-3,5-dién; 7αH,10βH-kadín-1(6),4-dién; τ-kadinol; kalkorén; α-kopán; β-kubebén; kocková guľa; kubenol; 1,10-diepikubenol; cis -β-elemén; elemol; epizonarén; eudesma-5,7(11)-dién; farnezol; ( E,E )-farnezylacetát; germakrén D; humulénový epoxid II; intermedeol; longiborneol; cis -muurola-4(15),5-dién; T-muurolol; (E)-nerolidol; sedatívum; β-selinén; selina-4(15),7-dién; a selina-3,7-dién. Väčšinu seskviterpénov tvorili uhľovodíky (celkovo 5,2 %), zatiaľ čo okysličené boli zastúpené menej (celkovo 1,1 %). Zatiaľ čo v esenciálnom oleji pripravenom zo semien A. alba predstavoval limonén 82,9 %, v esenciálnom oleji pripravenom zo semien A. koreana predstavoval limonén iba 53,7 %, pričom ten druhý obsahoval vyššie množstvo α-pinénu, kamfénu a bornylacetátu [ 33 ]. Analýzy vykonané s odstupom približne piatich rokov v rovnakých geografických oblastiach ukázali konzistentnosť v zložení s určitými kvantitatívnymi odchýlkami (hlavná zlúčenina, (−)-limonén, bola v prvom teste zastúpená v pomere približne 70 % a v druhom 82,9 % [ 33 , 48 ].
Manoyloxid, 13-epi-manoyloxid, abieta-7,13-dién a abietal boli jediné diterpenoidy zistené v esenciálnom oleji zo semien, a to iba v stopových množstvách [ 48 ].
3.1.7. Hydroláty zo semien
Hydrolát (kvetinová voda, hydrosol) získaný z odpadovej kvapaliny vznikajúcej hydrodestiláciou rastlinných semien má údajne sviežu, príjemnú živicovú vôňu. Jeho obsah éterického oleja bol odhadnutý na 10,7 mg/l (hydrolát zo semien pripravený z príbuzného druhu A. koreana má 37,3 mg/l éterických olejov). Hydrolát zo semien obsahoval selín-6-én-4-ol (51,7 %), β-himachalol (14,5 %), τ-kadinol (10,7 %), intermedeol (9,8 %), 1-epikubenol (2,1 %), elemol (1,7 %), 1,10-diepikubenol (1,5 %), longiborneol (1,0 %), eudesm-7(11)-én-4-ol (0,6 %), oplopanón (0,5 %), 5,8-cyklokaryofylán-4-ol (0,3 %), kubebol (0,2 %), eudesm-6-én-3-ol (0,2 %), α-bisabolol (0,1 %), borneol (0,1 %), α-kostol (0,1 %), (E)-nerolidol (0,1 %), trans -sesquisabinénhydrát (0,1 %), izomér p -ment-8-én-1,2-diolu. (0,1 %), α-terpineol (0,1 %), verbenón (0,1 %) a v stopách bornylacetát, 8-hydroxylinalool, terpinén-4-ol a α-terpinylacetát. Zatiaľ čo v éterickom oleji zo semien bola teda dominantná frakcia zastúpená monoterpénovými uhľovodíkmi, v hydroláte semien dominovali oxygenované seskviterpény (viac ako 95 %). Mnohé zlúčeniny prítomné v hydroláte chýbali v éterických olejoch a naopak [ 33 ].
3.1.8. Drevené terpenoidy
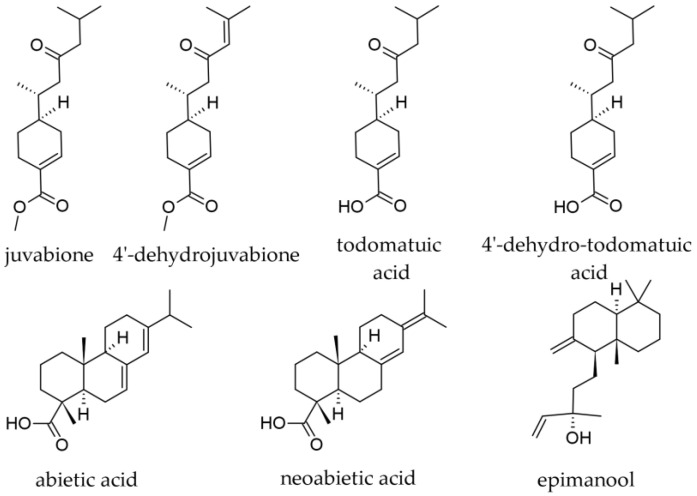
Hoci drevo ako časť rastliny jedle striebornej nie je primárne zaujímavé pre svoj obsah terpenoidov, boli v ňom tiež zaznamenané malé množstvá terpenoidných látok, hoci ich obsah v terpenoidoch nie je zanedbateľný (extrakt pripravený s etanolom obsahoval 15,65 % terpénov [ 23 ]. V metanolickom extrakte z dreva konárov boli okrem väčšiny zlúčenín patriacich do skupiny lignanov identifikované nasledujúce terpenoidy pomocou LC-DAD–ESI-MS/MS: dehydrojuvabión; kyselina neoabietová; a kyselina abietová ( obrázok 12 ) [ 50 ]. V extraktoch pripravených so 100 % etanolom z uzla bol zaznamenaný aj diterpenoid epimanool [ 23 ].
Obrázok 12.
Juvabióny sú zlúčeniny so silným hormonálnym pôsobením na mladý hmyz a antimykotickou aktivitou; chemicky sú to seskviterpénové kyseliny alebo nefenolické deriváty seskviterpénu. V dreve A. alba boli hlásené juvabión, 4′-dehydrojivabión, kyselina todomatuová a kyselina 4′-dehydrotodomatuová, ktoré boli o niečo hojnejšie v mŕtvych hrčkách ako v živých hrčkách a dva až trikrát rozpustnejšie v hydrofilných rozpúšťadlách (acetón, voda) ako v lipofilných (hexán) [ 21 ]. V drevených extraktoch pripravených so 100 % etanolom bol dehydrojivabión hlásený ako hojnejší ako juvabión [ 23 ].
3.2. Lignany
Kôra a drevo A. alba , podobne ako u iných ihličnanov, patria medzi najbohatšie zdroje lignanov v rastlinnom svete.
3.2.1. Lignany z kôry
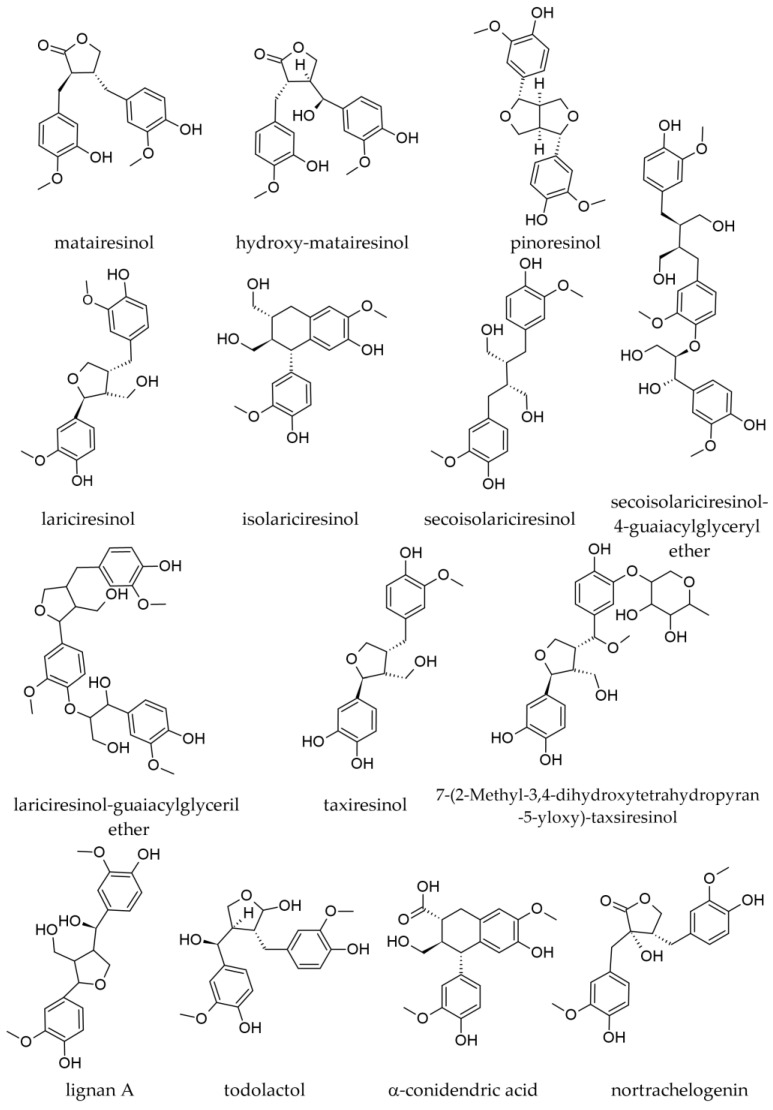
V extraktoch pripravených s vodou z kôry zozbieranej zo stoniek a konárov boli zaznamenané nasledujúce lignany ( obrázok 13 ): matairesinol; 7-hydroxymatairesinol (tiež známy ako hydroxymatairesinol); lariciresinol; izolaricirezinol (cyklolaricirezinol); sekoizolaricirezinol; pinoresinol; lignan A; a oligolignany [ 18 ]. Zdá sa, že matairesinol bol hojnejší v kôre stonky ako v kôre konárov (0,20 mg/g oproti 0,10–0,14 mg/g, suchej hmotnosti). Kôra kmeňa bola niekoľkonásobne bohatšia na izolaricirezinol ako kôra konárov (0,09 mg/g oproti 0,02 mg/g suchej hmotnosti), zatiaľ čo lariciresinol bol prítomný iba v kôre kmeňa (0,035 mg/g, suchej hmotnosti) a chýbal v kôre konárov. Sekoizolaricirezinol bol tiež hojnejší v kôre kmeňa ako v kôre konárov (0,04 mg/g oproti 0,02–0,03 mg/g, suchá hmotnosť) [ 18 ].
Obrázok 13.
V extrakte Abigenol® boli identifikované štyri lignany pomocou hmotnostnej spektrometrie: 7-(2-metyl-3,4-dihydroxytetrahydropyrán-5-yloxy)-taxirezinol; taxirezinol; sekoisolaricirezinol; a laricirezinol [ 4 ].
3.2.2. Drevené lignany
Ukázalo sa, že extrakty pripravené z dreva konárov sú bohaté na lignany, okrem obsahu fenolických derivátov a sacharidov [ 26 ]. V metanolickom extrakte z dreva konárov boli pomocou LC-DAD–ESI-MS/MS identifikované nasledujúce lignany: 7-hydroxylariciresinol; todolaktol; izolariciresinol; kyselina α-konidendrová; 7-hydroxymatairesinol; sekoizolariciresinol; sekoizolariciresinol guaiacylglyceryléter; lariciresinol; lariciresinol guaiacylglyceryléter; nortrachelogenín. Najhojnejšie sa javili sekoizolariciresinol a lariciresinol ( obrázok 13 ). V prípade nortrachelogenínu ten istý článok uviedol jeho prítomnosť v tabuľke, ale v diskusnej časti ju vyvrátil („nepozorovali sme žiadny signál pri očakávaných retenčných časoch“; preto jeho prítomnosť v A. alba nie je s istotou preukázaná) [ 50 ].
Vek a kol. (2021) uviedli izolaricirezinol v množstvách až do 46,9 mg/g v rôznych vzorkách dreva, pričom najbohatšie boli odumreté hrče; laricirezinol sa vo vzorkách dreva našiel v množstvách až do 32,3 mg/g, pričom najvyššie množstvo sa našlo v dreve konárov. V rôznych vzorkách dreva bol sekoizolaricirezinol lepšie zastúpený s hladinami 37,6 mg/g v dreve konárov [ 22 ]. Ďalšia práca uviedla, že sekoizolaricirezinol predstavoval 26,6 % všetkých zlúčenín v acetónovom extrakte z uzlov [ 51 ]. Pinoresinol bol v dreve menej zastúpený, pričom najvyššie hladiny boli zaznamenané v odumretých hrčoch (2,5 mg/g). Spomedzi vzoriek dreva mal matairesinol najvyššie zastúpenie v dreve konárov (10 mg/g), pričom mierne nižšie hladiny sa našli aj v živých a odumretých hrčoch [ 22 ].
V konároch (ktoré sú väčšinou z dreva, hoci zrejme boli frézované spolu s kôrou) bol zaznamenaný pokles obsahu rôznych lignanov so zvyšujúcou sa vzdialenosťou konára od kmeňa (takýto pokles bol výraznejší ako pokles zaznamenaný pre fenoly v konároch toho istého druhu) [ 13 ]. Najhojnejším lignanom bol sekoisolaricirezinol s hladinami 5,95 ± 1,41 mg/g v blízkosti kmeňa a iba 0,29 ± 1,03 mg/g vo vzdialenosti 80 cm od kmeňa. Koncentrácia izolaricirezinolu bola 1,34 mg/g v blízkosti kmeňa, ale iba 0,14 ± 0,15 mg/kg vo vzdialenosti 80 cm. Koncentrácia niekoľkých lignanov, vrátane laricirezinolu, 7-hydroxymatairezinolu, pinorezinolu a matairezinolu, sa významne znížila po celej dĺžke konára. Koncentrácia laricirezinolu sa znížila z 1,34 ± 0,19 na 0,15 ± 0,06 mg/kg po celej dĺžke vetvy, hladina 7-hydroxymatairezinolu z 0,54 ± 0,11 na 0,24 ± 0,30 mg/kg, hladina pinorezinolu z 0,49 ± 0,12 na 0,06 ± 0,04 mg/kg a obsah matairezinolu klesol z 0,32 ± 0,08 na 0,05 ± 0,06 mg/kg. Vzorka mletých konárov používaných na priemyselnú výrobu extraktu z jedle striebornej (obchodná značka Belinal® ) analyzovaná na porovnanie obsahovala 0,50 mg/kg sekoizolaricirezinolu, 0,26 mg/kg izolaricirezinolu, 0,21 mg/kg 7-hydroxymatairezinolu, 0,17 mg/kg laricirezinolu, 0,09 mg/kg pinorezinolu a 0,04 mg/kg matairezinolu [ 13 ].
V komerčne dostupnom extrakte z vetvičky (Belinal® ) boli identifikované a kvantifikované nasledujúce lignany: sekoisolaricirezinol (5,51 %); izolaricirezinol (1,78 %); 7-hydroxymatairezinol (0,89 %); laricirezinol (0,79 %); matairezinol (0,50 %); a pinoresinol (0,24 %) [ 52 ].
Vodné extrakty pripravené z uzlového dreva daného druhu obsahujú výrazne vyššie množstvo extrahovaných látok ako extrakty pripravené z kmeňového alebo jadrového dreva [ 21 , 22 ]. Bolo teda hlásené, že v rôznych druhoch Abies môže uzlové drevo obsahovať 20 – 50-krát viac lignánov ako kmeňové drevo, ale sú možné veľké rozdiely nielen medzi druhmi, ale aj vnútrodruhovo, medzi stromami. V beľovom dreve a jadrovom dreve A. alba sú lignány prítomné v množstvách rádovo μg/g, zatiaľ čo v živých alebo mŕtvych uzloch sú v množstvách rádovo mg/g [ 21 ].
Extrakty pripravené so 100 % etanolom z uzla sú tiež veľmi bohaté na lignany (približne 55 % plochy chromatogramu). Chromatograficky bolo pozorovaných najmenej 81 píkov, medzi ktorými bolo identifikovaných 21 zlúčenín. Najdôležitejší bol sekoizolaricirezinol (dominantný lignan), nasledovaný laricirezinolom, 7-hydroxymatairezinol, ako aj významným množstvom D-pinitolu. Sekoizolaricirezinol, hlavný lignan dreva A. alba (33,40 % celkovej plochy chromatogramu), má maximálne koncentrácie v uzloch nachádzajúcich sa okolo bázy koruny, pričom jeho hladiny klesajú v uzloch umiestnených smerom k bázám kmeňa alebo smerom k vrcholu stromu. Laricirezinol (9,87 % celkovej plochy chromatogramu) nemal podobnú závislosť od polohy uzla na strome. Výťažok hydroxymatairezinolu (mg/g) má tendenciu klesať so zvyšujúcou sa výškou uzla. Izolaricirezinol bol v etanolovom extrakte zaznamenaný v menších množstvách [ 23 ].
Zdá sa, že výťažok extrakcie je vyšší v prípade mŕtvych hrčí ako v prípade živých hrčí vzhľadom na celkové množstvo lignanov (53 – 55 mg/g oproti 67 – 70 mg/g) a medzi lignánmi v týchto dvoch kategóriách hrčí existujú určité kvalitatívne rozdiely [ 21 , 22 ]. Celkový obsah sekoizolaricirezinolu sa zdá byť podobný v prípade živých aj mŕtvych hrčí, ale v prvom produkte je malá časť tohto lignanu vo forme dimetyl- alebo monometyléteru (29 – 30 mg/g sekoizolaricirezinolu + 0,56 – 0,57 mg/g dimetyléteru + 2,3 mg/g monometyléteru oproti 32 – 36 mg/g). Laricirezinol je prítomný v takmer dvojnásobnom množstve v mŕtvych hrčkách ako v živých hrčkách (9,9 – 10,0 mg/g oproti 4,6 – 5,2 mg/g). Liovil (až tri izoméry) je hojnejší v živých hrčkách ako v mŕtvych hrčkách (5,5 – 6,0 mg/g oproti 3,8 – 4,0 mg/g). 7-hydroxymatairezinol (4,2 mg/g oproti 4,8 – 5,2 mg/g), 7- allo- hydroxymatairezinol (2,8 mg/g oproti 2,4 mg/g) a matairezinol (2,5 – 2,6 mg/g oproti 2,6 mg/kg) sú prítomné v viac-menej podobných množstvách v oboch typoch hrčiek. Mŕtve hrčky sú bohatšie na izolaricirezinol (cyklolaricirezinol, 5,7 – 7,4 mg/g oproti 0,88 – 0,89 mg/g) a pinorezinol (0,36 – 0,40 mg/g oproti 0,98 – 1,0 mg/g) ako živé hrčky. Nortrachelogenín bol zaznamenaný vo veľmi vysokých množstvách v odumretých hrčkách (270 mg/g), zatiaľ čo v živých hrčkách chýbal. Seskvineolignány (13 – 16 mg/g), dilignany (12 – 14 mg/g) a vyššie oligolignany (2,5 – 3,1 mg/g) sú tiež prítomné v dreve uzlov jedle striebornej, pričom dominantné sú dineolignány, s mierne vyšším množstvom v odumretých hrčkách ako v živých hrčkách. Lignany sa v A. alba nachádzajú v prevažnej miere ako voľné aglykóny [ 21 ].
Hoci sa všeobecne uvádza, že laktobacily môžu ovplyvniť metabolizmus určitých lignanov a viesť k zvýšeniu produkcie lignanov, Stojanov a kol. (2021) nezistili žiadny vplyv laktobacilov (10 rôznych druhov, z ktorých niekoľko bolo odvodených z ľudských izolátov) na produkciu enteriodiolu alebo enterolaktónu z lignanov prítomných v extrakte z dreva A. alba . Mikrobiálne druhy testované týmito autormi sa však líšili od druhov v predtým publikovanom výskume a hladiny lignanov boli nižšie ako tie, ktoré sa používali predtým [ 26 ].
3.3. Fenoly
3.3.1. Fenolové zlúčeniny z kôry (vrátane flavonoidov)
V kôre stonky a konárov A. alba zo Slovinska bol zaznamenaný obsah približne 2,67 % ( hmotn./hmotn . , suchá hmotnosť ) celkových fenolov [ 18 ]. Hydrofilné extrakty získané z kôry obsahujú približne 15 % celkových fenolov [ 18 ]. Namiesto toho sa na vzorkách švajčiarskej kôry extrahovaných vodou pri teplote 60 °C uvádzal celkový extrakčný výťažok 10,1 – 12,0 % ( hmotn./hmotn . , suchá hmotnosť ) a celkové fenolové zlúčeniny predstavovali 27,9 % tohto extraktu [ 6 , 53 ].
Zdá sa, že podiel fenolických zlúčenín je vyšší v kôre zo spodných častí kmeňa [ 20 ]. Hoci vnútorná a vonkajšia vrstva kôry majú podobný celkový priemer hydrofilných extrahovateľných látok, obsah fenolov sa medzi týmito dvoma vrstvami líši: vnútorná vrstva kôry bola chudobnejšia na celkové fenoly ako vonkajšia vrstva (vonkajšia obsahovala 14,87 mg/g, teda viac fenolov ako vonkajšia). Rozdiel by mohol byť aspoň čiastočne spôsobený fenolmi z buniek peridermu korku [ 18 ].
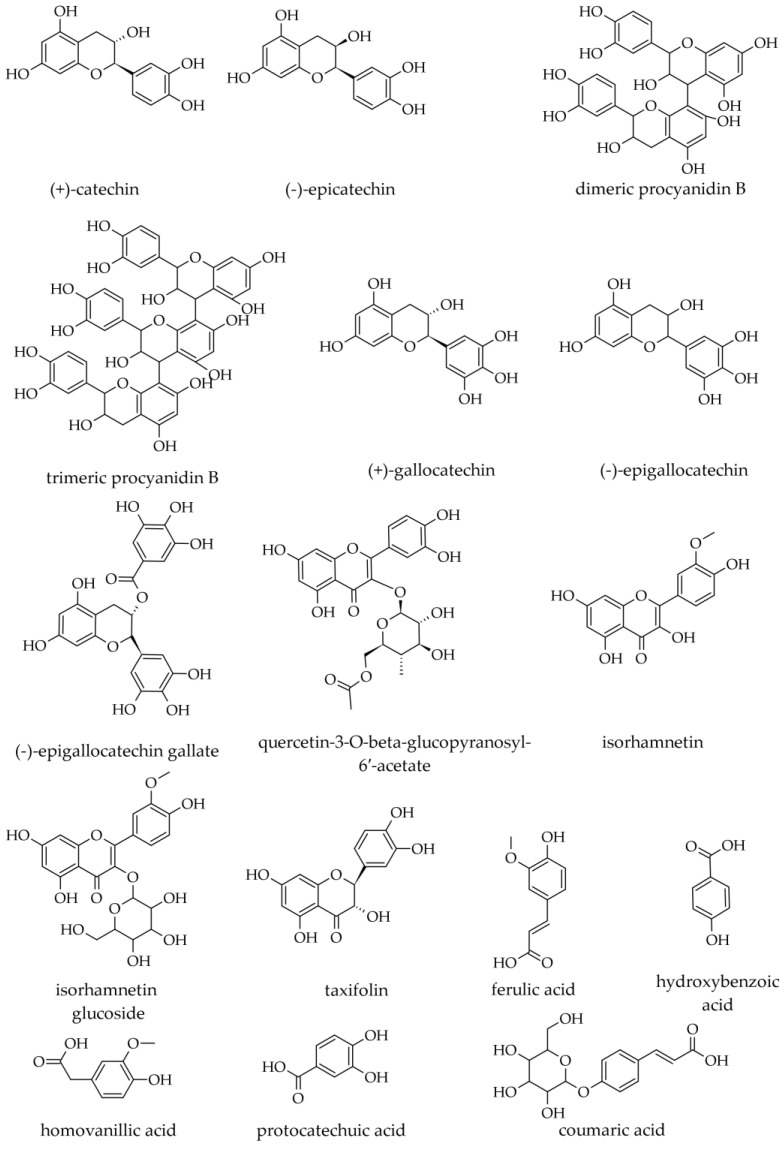
V extraktoch pripravených zmesou voda-etanol 50:50 ( v / v ) boli identifikované nasledujúce polyfenolické zlúčeniny: galokatechín; epigalokatechín; dimér galokatechínu; galokatechín galát; (+)-katechín; kvercetín glykozid (SiC), kvercetín-3-O-beta-glukopyranosyl-6′-acetát, izoramnetín a izoramnetín glukozid ( obrázok 14 ). Hoci deriváty stilbénu boli hlásené u druhu Picea spp., žiadny z nich nebol identifikovaný u druhu A. alba [ 54 ].
Obrázok 14.
Vo vodných extraktoch pripravených z kôry kmeňa (stonky) alebo konárov boli najhojnejšími fenolikmi katechín, epikatechín, taxifolín, kyselina ferulová a v menšej miere kyselina homovanilová a kumarová [ 18 ]. Katechín a epikatechín sa zdajú byť najhojnejšie a nachádzajú sa v podobných hladinách v hydrofilných extraktoch. V prípade katechínu sa zdá, že kôra z kmeňa je o niečo bohatšia ako kôra z konárov (0,76 mg/g oproti 0,68–0,72 mg/g, suchej hmotnosti), zatiaľ čo v prípade epikatechínu to tak nie je (0,78 mg/g oproti 0,66–0,81 mg/g, suchej hmotnosti). Naopak, taxifolín sa zdá byť o niečo menej hojný v kôre z kmeňa ako v kôre z konárov (0,29 mg/g oproti 0,34–0,38 mg/g, suchej hmotnosti) [ 18 ].
Na rozdiel od iných druhov čeľade Pinaceae sú prodelfinidíny dominantnými jednotkami v kondenzovaných tanínoch (s polymerizačným stupňom ≤ 9; vo všeobecnosti je polymerizačný stupeň nižší pre taníny Gymnosperm ako pre taníny Angiosperm), zatiaľ čo prokyanidíny sú zastúpené menej (ich pomer je približne 4:1). Prokyanidíny sa nachádzajú prevažne v cis-konfigurácii (epikatechín, epigalokatechín), zatiaľ čo prodelfinidíny sú v trans -konfigurácii (katechín, galokatechín) [ 6 , 53 , 54 ].
Kyselina kumarová sa nachádza v mierne vyšších množstvách v kôre stromov ako v kôre konárov (0,10 mg/g oproti 0,08–0,09 mg/g, suchej hmotnosti). Kyselina ferulová je v kôre prítomná v podobných množstvách bez ohľadu na jej pôvod (kmeň alebo konáre – 0,03 mg/g oproti 0,02–0,03 mg/g, suchej hmotnosti). Kyselina hydroxybenzoová sa v kôre kmeňa zrejme nenachádza, zatiaľ čo v kôre konárov sa môže nachádzať v nízkych množstvách (0,01 mg/g, suchej hmotnosti). Kyselina homovanilová sa zrejme nenachádza v kôre kmeňa, ako aj v kôre v zónach konárov blízko kmeňa, zatiaľ čo v kôre z častí ďalej od kmeňa je prítomná v nízkych množstvách (0,025 mg/g, suchej hmotnosti) [ 18 ].
Uvádza sa, že Abigenol ® (komerčný extrakt pripravený z kôry) obsahuje nasledujúce fenolové kyseliny: kyselinu galovú (0,25 %); kyselinu homovanilovú; kyselinu protokatechuovú (0,77 %); kyselinu p -hydroxybenzoovú (0,10 %); kyselinu vanilovú (0,11 %); a kyselinu p -kumarovú (0,37 %) [ 4 ]. V Abigenole ® boli detegované tri flavonoidné zlúčeniny: katechín; epikatechín; a tetrametyléter katechínu [ 4 ]. Jedna dávka Abigenolu ® /AlbiPhenol ® (150 mg) obsahuje 9,2 ± 0,1 mg katechínov. Simulačné štúdie in vitro založené na trávení naznačujú, že približne 50 % katechínov z extraktu sa uvoľňuje z matrice počas procesu trávenia, zatiaľ čo približne 43 % by bolo biologicky neprístupných a vylučovalo by sa stolicou. Experimenty s údajmi in vitro s použitím buniek Caco-2 ukázali, že napriek dobrej biodostupnosti katechínov bola biologicky dostupná frakcia pod detekčným limitom metódy HPLC (2,7 µg/ml) [ 55 ].
3.3.2. Fenolové zlúčeniny dreva (vrátane flavonoidov)
V metanolovom extrakte z dreva konárov boli pomocou LC-DAD–ESI-MS/MS identifikované nasledujúce fenolové zlúčeniny: galokatechín; dimérny prokyanidín B (najmenej štyri rôzne diméry); trimérny prokyanidín B; katechín; a epikatechín [ 18 , 50 ]. V rôznych vzorkách dreva (belové drevo, jadrové drevo, drevo konárov, živé alebo mŕtve hrče) Vek a kol. (2021) uviedli, že epikatechín buď nebol zistený, alebo bol v koncentráciách 0,1 mg/g. Tí istí autori uviedli, že kyselina homovanilová nebola v beľovom dreve prítomná a jej koncentrácia sa pohybovala medzi 0,3 a 2,3 mg/g v rôznych vzorkách dreva vrátane hrčov. Kyselina kumarová nebola v beľovom dreve zistená, ale spomedzi rôznych vzoriek dreva mala najvyššie koncentrácie v živých alebo mŕtvych hrčoch (0,5 mg/g) [ 22 ]. V dreve bola kyselina ferulová zaznamenaná v množstvách pohybujúcich sa (v závislosti od druhu dreva) medzi 0,0 a 0,2 mg/g [ 22 ].
Willför a kol. (2004) nenašli taxifolín vo vzorkách kmeňového a uzlového dreva [ 21 ], ale Vek a kol. (2021) uviedli, že bol prítomný v koncentráciách až do 0,9 mg/kg vo vzorkách uzlového a konárového dreva. Malé množstvá kvercetínu uviedli tí istí autori vo vzorkách dreva A. alba v koncentráciách pohybujúcich sa medzi 0,1 a 1,4 mg/kg, pričom najvyššia hladina bola zistená v odumretých uzloch [ 22 ].
Priemerný obsah fenolických zlúčenín 28,7 mg/g (ekvivalenty kyseliny galovej, GAE) bol odhadnutý vo vzorke šiestich konárov (väčšinou dreva, ale aj kôry) zozbieraných v Slovinsku, pričom z každej vetvy bolo odobratých viacero segmentov v rôznych vzdialenostiach od kmeňa (deväť segmentov pre každú vetvu, vo vzdialenosti približne 10 cm od seba). Pre segment nachádzajúci sa vo zvyšujúcich sa vzdialenostiach od kmeňa bol zaznamenaný kontinuálny pokles obsahu fenolov, pričom obsah fenolov bol približne o 61 % nižší vo vzdialenosti 80 cm od kmeňa ako vo vzdialenosti 0 cm od kmeňa [ 13 ].
3.4. Iné zlúčeniny
3.4.1. Lipidy a iné lipofilné zlúčeniny
Spomedzi štyroch druhov ihličnanov ( Pinus sylvestris L., A. alba , Picea abies (L.) H.Karst.) a Larix decidua Mill.) mala kôra A. alba druhý najnižší obsah lipidov (25,73 mg/g vzorky, na suchú bázu) a druhý najvyšší obsah mastných kyselín (155,70 mg/g lipidov). Tieto mastné kyseliny sú zastúpené kyselinami behenovou (41,78 %), lignocerovou (21,09 %), arachidovou (18,02 %), trikozylovou (4,52 %), stearovou (3,49 %), heptadecénovou (3,55 %), undekánovou (2,20 %) a cis -pentadecénovou (2,07 %) [ 7 ]. Extrakcia kôry n-hexánom poskytla výťažok 4,12 ml/100 g čerstvej vzorky. V tomto n-hexánovom extrakte bolo identifikovaných deväť zlúčenín, ktoré predstavovali 99,98 % jeho obsahu (v zostupnom poradí podľa ich zastúpenia): di(2-etylhexyl)-ftalát (59,83 %); metylcyklopentán alebo cyklopentylmetán (16,63 %); 13-epimanool (diterpenoid, 6,31 %); metylcyklohexán alebo cyklohexylmetán (3,73 %); a 3-metylhexán (3,29 %) [ 44 ].
Spomedzi štyroch vyššie uvedených druhov ihličnanov malo jadrové drevo A. alba najnižší obsah lipidov (11,03 mg/g vzorky, v sušine) a druhý najnižší obsah mastných kyselín (17,48 mg/g lipidov). Tieto mastné kyseliny pozostávajú z kyseliny arachidovej (37,42 %), palmitovej (22,02 %), pentadekánovej (15,14 %), margarínovej (12,23 %), stearovej (5,83 %), myristovej (5,10 %) a erukovej (2,14 %) [ 7 ]. Extrakcia dreva n-hexánom poskytla výťažok 1,13 ml/100 g čerstvej vzorky. V tomto extrakte prevláda 4-hydroxy-4-metyl-2-pentanón (diacetónalkohol), čo predstavuje 73,36 %. Ďalšie štyri zlúčeniny, ktoré spolu s diacetónalkoholom predstavujú 97 % jeho zloženia, sú α-cedrol (10,08 %), 2,6-dimetyl-1,3,6-heptatrién (7,35 %), terpinén-4-ol (4-terpinenol, S-origanol) (3,25 %) a α-felandrén (2,96 %) [ 44 ].
Spomedzi semien štyroch druhov jedle (Abies) a troch druhov smreka (Picea ) poskytovali semená druhu A. alba najbohatší extrahovaný lipofilný obsah (41,1 %), druhé v klesajúcom poradí boli semená druhu A. cephalonica (32,0 %). Zatiaľ čo u druhu Picea sp. sa zdá, že kyselina pinolénová je jednou z charakteristických zlúčenín v lipofilnej frakcii semien; spomedzi štyroch skúmaných druhov jedle (Abies ) bola prítomná iba v semenách druhu A. alba . Spomedzi tokoferolov bol v semenách druhu A. alba zaznamenaný α-tokoferol a v menšom množstve γ-tokoferol [ 56 ].
Živicové uhľovodíky sú v semenách prítomné vo veľmi nízkom množstve, ich celkový obsah predstavuje menej ako 0,1 % všetkých zlúčenín. V semenách A. alba boli zaznamenané 18-norabieta-8,11,13-trién, abieta-8,11,13-trién, abieta-7, 13-diente a levopimaradién [ 56 ]. Živicové aldehydy sú hojnejšie (0,47 %): levopimaral a neoabietal sú hlavnými zlúčeninami tejto skupiny, zatiaľ čo v oveľa menších podieloch boli zaznamenané aj dehydroabietal a abietal. Živicové alkoholy sú prítomné v mierne vyšších množstvách ako živicové aldehydy; v klesajúcom kvantitatívnom poradí sú to cis -abienol, neoabietol, abietol, palustrol, levopimarol, dehydroabietol a neoabienol. Živicové kyseliny tvoria približne 1,8 % lipofilnej frakcie. Hlavnou živicovou kyselinou bola kyselina abietová, nasledovaná kyselinami neoabietovou, levopimarovou a dehydroabietovou; v oveľa menších podieloch boli prítomné aj nasledujúce živicové kyseliny: kyselina monohydroxydehydroabietová; kyselina monohydroxyživicová 1; izopimarová; sandaracopimarová; a palustrová. Malé množstvo živicových esterov (0,02 %) pozostávalo z metylneoabietátu a metylabietátu. Mastné alkoholy predstavujú približne 0,05 % lipofilnej frakcie a pozostávajú prevažne z tetrakosanolu s veľmi malým množstvom hexakosanolu a nonakosan-10-olu. Steroly, zistené vo veľmi nízkych množstvách (menej ako 0,002 %), sú zastúpené β-sitosterolom a kampesterolom [ 56 ].
Lipofilná frakcia semien A. alba obsahuje približne 0,26 % voľných mastných kyselín, z ktorých boli identifikované nasledujúce (v zostupnom poradí podľa kvantitatívnej dôležitosti): kyselina linolová; olejová; stearová; behenová; heptadekánová; lignocerová; oktadekadiénová; a palmitová. Veľmi nízke množstvá monoglyceridov mastných kyselín (<0,009 %) pozostávali z monoglyceridu kyseliny tetrakozanovej, monoglyceridu kyseliny dokozánovej a monoglyceridu kyseliny eikozánovej. Sterylestery predstavujú 0,34 % celkovej lipofilnej frakcie, diglyceridy 2,77 % a triglyceridy 19,5 %. Po alkalickej hydrolýze boli identifikované nasledujúce mastné kyseliny: myristová; pentadekánová; palmitová; palmitoolejová; 14-metylhexadekánová; stearová; olejová; cis -vakcenová; linolová; taxolová; α-linolénová; linolénová; arachidová; eikozénová (20:1(9) a 20:1(11)); eikozadiénová; sciadonová; behenová; a lignocerová [ 56 ].
3.4.2. Sacharidy
Z extraktu získaného s vodou pri teplote 60 °C predstavovali sacharidy 29,1 % (16,5 % voľných, 12,6 % viazaných). Monosacharidy v kôre sú zastúpené glukózou (8,97 g/kg) a fruktózou (9,76 g/kg) s malým množstvom galaktózy (1,06 g/kg). Sacharóza bola uvedená ako hlavný oligosacharid v kôre A. alba (8,08 g/kg), zatiaľ čo rafinóza a stachyóza sú dostupné v oveľa nižších množstvách (približne 1 g/kg sušiny). Viazané sacharidy (polysacharidy) obsahovali najmä glukózu (8,84 g/kg), galaktózu (2,06 g/kg), arabinózu (1,56 g/kg), kyselinu galakturónovú (0,69 g/kg) a manózu (0,42 g/kg). S vyšším obsahom glukózy a nižším obsahom arabinózy sa viazané sacharidy z A. alba podstatne líšili od ostatných analyzovaných druhov borovice [ 57 ].
Extrakty pripravené so 100 % etanolom z uzlov obsahujú 8,91 % sacharidov, 15,56 % cyklitolov, ako aj malé množstvo disacharidov a C6 monosacharidov [ 23 ]. Extrakty zo živých uzlov sú bohatšie na sacharidy a glycitoly ako extrakty z mŕtvych uzlov [ 22 ]. Hladiny D-pinitolu boli vyššie v uzloch nachádzajúcich sa v horných častiach stromov, zatiaľ čo v uzloch nachádzajúcich sa v spodných častiach stromu boli nižšie [ 23 ].
3.4.3. Anorganické zlúčeniny
V ihličí jedle striebornej bol vo vzorkách z Českého lesa odhadnutý stredný obsah dusíka na 13,5 g/kg. Pre fosfor bola vo vzorkách z Českého lesa zaznamenaná stredná hodnota 1952 mg/kg, zatiaľ čo v Nemecku, na Slovensku a v Poľsku boli odhadnuté hodnoty 1400 mg/kg. Priemerná hladina horčíka v ihličí je medzi 1971 a 2400 mg/kg v závislosti od zdroja vzoriek, zatiaľ čo priemerné hladiny vápnika sa pohybujú medzi 5432 a 15 500 mg/kg. V prípade železa sa priemerné hladiny pohybovali medzi 53,3 mg a 215 mg/kg; v prípade mangánu 625 mg/kg; a v prípade zinku 30 – 63 mg/kg [ 58 ]. V ihličí majú hladiny dusíka, fosforu, K a Mg tendenciu s vekom exponenciálne klesať, zatiaľ čo hladiny Zn, Ca a Mn sa naopak s vekom exponenciálne zvyšujú. Hladiny železa mali tendenciu lineárne sa zvyšovať s vekom, zatiaľ čo hladiny Ni, Cd a Pb mali nepravidelný dynamický vzorec [ 59 ]. Extrakt z kôry pripravený s vodou pri teplote 60 °C obsahuje približne 3,8 % anorganických zlúčenín [ 57 ].
4. Etnofarmakológia
V 18. storočí sa z ihličia ihličnanov pripravovali rôzne nápoje (čaje, zápary a pivá), ktoré sa pod názvom „sapinette“ používali na liečbu skorbutu. Zatiaľ čo vo Francúzsku sa pojem „sapinette“ mal používať ako odvar z „sapin du Nord“ (t. j. Picea abies ); v Kanade sa pripravoval z púčikov „pruskej jedle“, čo označovalo ktorúkoľvek z druhov A. alba , A. balsamea alebo P. abies [ 60 ]. Je zaujímavé, že Radulescu a kol. (2013) uviedli, že bez ohľadu na obdobie zberu (máj, júl alebo október) výhonky A. alba obsahujú nižšie množstvo kyseliny askorbovej ako výhonky P. abies , čo potvrdzuje správnosť francúzskeho chápania pojmu „sapinette“. Jedľa strieborná bola v tejto štúdii druhým najlepším zdrojom kyseliny askorbovej, pretože obsah vitamínu C vo výhonkoch mal tendenciu byť vyšší ako v Pinus nigra JFArnold, Pseudotsuga menziesii (Mirb.) Franco alebo Larix decidua (iba výhonky zozbierané v októbri mali vyššiu hladinu kyseliny askorbovej ako A. alba ) [ 61 ]. To naznačuje, že ani kanadská verzia nebola až taká nedostatočná.
V minulosti sa esenciálne oleje pripravené z ihličia striebornej používali na hojenie modrín a liečbu bežného prechladnutia a kašľa [ 8 ]. Vo Francúzsku sa olej z ihličia striebornej používa proti prechladnutiu a iným infekciám dýchacích ciest a aplikuje sa ako balzam, pleťové mlieko alebo do kúpeľa, často spolu s inými olejmi (napríklad eukalyptovým) [ 30 ].
V bylinkárni Matthiolus z roku 1590 sa spomína použitie miazgy (živice) z jedle striebornej na liečbu dny v nohách a bolesti bedrového kĺbu [ 62 ]. Živica sa používala v Transylvánii (západná časť Rumunska) na liečbu furunklov a kožných problémov [ 63 ]. V Albánsku, Bosne a Hercegovine a Macedónsku sa živica (pravdepodobne zo stoniek a konárov) používa ako balzam a lokálne sa aplikuje na rany alebo bradavice. Na rany sa živica niekedy aplikuje spolu s tabakom, ktorý sa používa ako hemostatikum [ 64 ]. V talianskom ľudovom liečiteľstve sa živica používa na liečbu bolestí hlavy natieraním spánkov [ 65 ]. Živica sa tiež tradične používa na liečbu artrózy vo forme obkladu aplikovaného lokálne [ 66 ].
V etnomedicíne sa jeho výhonky, pripravené ako sirup, používali v Transylvánii na liečbu kašľa a ako obklady na zubný kaz; žuvali sa aj na čistenie zubov. V tom istom regióne sa výhonky používali ako odvary alebo nálevy na liečbu respiračných ochorení, zatiaľ čo ako kúpele sa používali na liečbu reumatizmu [ 63 ].
V Transylvánii sa púčiky používali ako odvar proti opuchnutým krčným uzlinám, zatiaľ čo ihličie sa aplikovalo ako obklad proti „bolesti pečene“ [ 63 ]. V Rumunsku sa púčiky a konáre používali na vonkajšie ošetrenie rán pre ich sťahujúce vlastnosti [ 67 ].
Kôra sa v Transylvánii používala ako odvar proti bolestiam hrdla [ 63 ].
V Katalánsku (Španielsko) sa sirup pripravuje z nezrelých šišiek ich krájaním a maceráciou s cukrom. Sirup sa môže získať s varom alebo bez varu, pričom varenie má výhodu v tom, že sa vyhýba fermentácii. Používa sa pre svoje balzamikové, antitusické, protinádchové a bronchopulmonálne dekongestívne vlastnosti [ 68 ].
5. Biologické a farmakologické účinky
5.1. Antioxidačné účinky
5.1.1. Antioxidačné účinky esenciálnych olejov
V teste DPPH mal esenciálny olej pripravený z listov a vetvičiek v 10 % koncentrácii antioxidačné účinky podobné účinkom kyseliny askorbovej. Jeho účinky boli nižšie na ABTS ako na voľné radikály DPPH [ 35 ]. S. Garzoli a kol. odhadli hodnotu IC50 v teste DPPH na 7,84 ± 1,70 µg/ml pre esenciálny olej z ihličia z A. alba , čím sa tento esenciálny olej umiestnil na druhom mieste z hľadiska jeho antioxidačnej účinnosti za olej z Pinus mugo Turra, ale pred oleje z Pinus cembra L. a Picea abies . Mal hodnotu TEAC 3,01 ± 0,48 µM (ekvivalent troloxu/mg oleja). Pri hodnotení oproti radikálu ABTS sa štyri hodnotené esenciálne oleje medzi sebou len málo líšili; olej z A. alba mal hodnotu IC50 44,23 ± 1,10 µg/ml a ekvivalent TEAC [ 37 ]. Pokiaľ ide o jeho zložky, limonén preukázateľne má silný vplyv na DPPH a mierny vplyv na ABTS; β-pinén má „mierny“ vplyv na DPPH (21,4 % pri koncentrácii, ktorá nebola v pôvodnej správe jasne identifikovaná) a nízky vplyv na ABTS, zatiaľ čo α-pinén má zanedbateľný vplyv na voľné radikály [ 35 , 69 , 70 ]. Spomedzi 15 esenciálnych olejov z rôznych rastlinných druhov testovaných pri koncentrácii 50 μL/ml na ich účinky proti DPPH, olej z ihličia A. alba (časť rastliny nie je v tejto práci spomenutá, ale potvrdil nám to autor korešpondencie) patril medzi najmenej účinné vo svojich účinkoch na zachytávanie, pričom poskytoval iba 56,17 % antioxidačnú aktivitu (v porovnaní napríklad s najsilnejším olejom z Origanum vulgare , ktorý poskytoval 93,00 % antioxidačnú aktivitu pri rovnakej koncentrácii 50 μL/ml) [ 71 ].
Pri vyhodnotení metódou DPPH sa zistilo, že esenciálny olej zo šišiek získaný z A. alba vykazuje silnejšie antioxidačné účinky v porovnaní s olejom extrahovaným zo semien. Antioxidačné účinky olejov zo šišiek a semien A. koreana boli strednej sily, spadajúce medzi účinky šišiek a semien A. alba . [ 33 ]
5.1.2. Antioxidačné účinky rôznych extraktov
V extraktoch získaných z čerstvých a sušených ihličia hydrodynamickou kavitáciou s vodou ako rozpúšťadlom sa antioxidačná aktivita DPPH ukázala byť veľmi citlivá na teplotu extrakcie s náhlym poklesom nad 47 °C. Antioxidačné účinky DPPH vykazovali malú koreláciu s celkovým obsahom polyfenolov alebo celkových flavonoidov. Antioxidačné účinky ORAC rovnakých extraktov boli tiež citlivé na teplotu, ale iným spôsobom, pričom náhle poklesy boli zaznamenané, keď teplota prekročila prahovú hodnotu okolo 60 °C. Antioxidačné účinky ORAC lepšie korelovali s celkovou koncentráciou polyfenolov a flavonoidov [ 16 ].
Antioxidačné účinky extraktov pripravených z konárov sa znižovali so zvyšujúcou sa vzdialenosťou od kmeňa. Pri extraktoch získaných zo segmentov vzdialených 80 cm od kmeňa došlo k 52 % zníženiu radikálu DPPH (12,1 ± 1,1 mg/g GAE oproti 5,8 mg GAE) a 51 % zníženiu katiónu radikálu ABTS (11,7 mg/g oproti 5,7 mg/g) v porovnaní s extraktmi získanými zo segmentov v bezprostrednej blízkosti kmeňa. Extrakty z konárov zo segmentov vzdialených 0 cm od kmeňa mali antioxidačný účinok 12,2 (± 1,1) mg/g proti DPPH a segmenty z 80 cm mali antioxidačný účinok 5,8 mg/g (± 2,8); rovnaké extrakty mali antioxidačný účinok proti katiónu radikálu ABTS 11,7 (± 0,8) mg/g GAE vo vzdialenosti 0 cm a 5,7 mg/g GAE vo vzdialenosti 80 cm [ 13 ].
Spomedzi hydrofilných extraktov pripravených z rôznych vzoriek dreva mal extrakt získaný z beľového dreva najnižší účinok zachytávania, zatiaľ čo extrakty pripravené z konárového dreva, živých alebo mŕtvych hrčí, mali podobné účinky zachytávania, odhadované v porovnaní s DPPH, pri koncentrácii 100 mg/ml ako približne o 60 % nižšie ako kyselina galová a o 30 % nižšie ako kyselina askorbová, zatiaľ čo pri koncentrácii 500 mg/ml bola aktivita približne o 20 % nižšia ako u dvoch referenčných látok (hodnoty IC50 neboli vypočítané) [ 22 ].
Hydrofilné extrakty z kôry stonky a konárov, bohaté na lignany a fenolové deriváty, vykazovali horšie antioxidačné účinky ako kyselina gallová a kyselina askorbová, najmä pri koncentráciách nižších ako približne 500 mg/l. Pri koncentrácii 1000 mg/l majú extrakty z kôry stonky aj konárov účinok prakticky rovnaký ako u dvoch referenčných látok (približne 90 % inhibícia DPPH); obe referenčné látky však spôsobujú rovnaký účinok (90 % inhibícia DPPH) od 300 mg/l vyššie. Pri koncentrácii 100 mg/l nemal ani jeden z dvoch extraktov badateľný účinok na DPPH, zatiaľ čo kyselina askorbová inhibovala približne 50 % DPPH a kyselina gallová inhibovala približne 90 % DPPH [ 18 ]. Etylacetátová frakcia extraktu z kôry mala hodnotu IC50 7,9 ± 0,1 μg/ml proti DPPH a 1,56 ± 0,05 μg/ml proti železnatým iónom, pričom tieto hodnoty sa blížili hodnotám katechínu (7,1 ± 0,05 μg/ml) a sodnej soli EDTA (1,27 ± 0,1 μg/ml) [ 72 ]. Na základe hodnôt IC50 sa aktivita zachytávania superoxidu (53,30 ± 5,91 μg/ml) a hydroxylových radikálov (63,12 ± 1,78 μg/ml) zdala slabšia [ 72 ].
Pre extrakt SFTE (získaný z kmeňa) bola odhadnutá hodnota IC50 2,9 μg/ml pre aktivitu zachytávania hydroxylového radikálu. Tento účinok bol silnejší proti rovnakému radikálu ako účinok zaznamenaný pre resveratrol (IC50 = 5,8 μg/ml), butylovaný hydroxytoluén (BHT, IC50 = 9,2 μg/ml), tokoferol (IC50 = 10,1 μg/ml) a epigalokatechín galát (EGCG, IC50 = 18,3 μg/ml) [ 27 ].
V bunkovom teste sa tvrdilo, že Abigenol® ( extrakt z kôry) má výrazne vyššie antioxidačné účinky v porovnaní s komerčným suchým extraktom z kôry Pinus maritima ((F0400/Pycnogenol® ) ), čo je takmer dvojnásobný účinok v porovnaní s extraktom z kôry Pinus maritima . Extrakt pripravený tými istými autormi priamou extrakciou etylacetátom, po ktorej nasledovalo vyzrážanie polyfenolov pomocou heptánu („d-AABE“), mal ešte silnejšiu antioxidačnú aktivitu [ 4 ]. V tejto práci nebola stanovená žiadna hodnota IC50 pre antioxidačný účinok týchto dvoch extraktov.
Abigenol ® /AlbiPhenol ® významne znížil oxidačnú záťaž spôsobenú dietylmaleátom v endoteli (bunky HUVEC) znížením tvorby ROS aj oxidácie glutatiónu. Napriek obmedzenej dostupnosti extraktu v koncentrácii 2,7 µg/ml stále účinne znížil produkciu ROS spôsobenú dietylmaleátom. Relevantný pokles oxidácie glutatiónu sa však dal dosiahnuť iba pri použití 1000 µg/ml (t. j. najvyššej netoxickej koncentrácie extraktu). Extrakt nemal významný vplyv na expresiu superoxiddismutázy (SOD) pri interakcii s endotelom. Extrakt tiež znížil oxidačný stres spôsobený dietylmaleátom v bunkách H9c2, čím znížil tvorbu ROS (pri 700 µg/ml) aj aktivitu SOD (pri 700 µg/ml aj pri 2,7 µg/ml) a nemal žiadny vplyv na oxidáciu glutatiónu. Pri koncentrácii 1200 µg/ml extrakt významne znížil produkciu ROS a oxidáciu glutatiónu v bunkách HepG2. In vitro sa preukázalo, že Abigenol ® /AlbiPhenol ® pri svojej biologicky dostupnej koncentrácii významne spomaľuje oxidáciu HDL a LDL o 51,8 %, respektíve 43,9 %, zatiaľ čo pri vyšších koncentráciách mohol antioxidačný účinok na obe lipoproteínové frakcie dosiahnuť 98,5 %, respektíve 85,8 %. V teste ORAC (Oxygen Radical Absorbance Capacity) extrakt vykazoval vysoké hodnoty (vyjadrené ako ekvivalenty Troloxu), čo mu umožnilo umiestniť sa medzi prvými štyrmi miestami v databáze USDAORAC (tlačené vydanie z roku 2010) [ 55 ]. Význam tohto zistenia by sa však nemal preceňovať. Je známe, že databáza ORAC bola odstránená z webovej stránky USDA z dvoch hlavných dôvodov: rozsiahle zneužívanie zo strany potravinárskeho a výživového priemyslu a obavy týkajúce sa vedeckej platnosti a relevantnosti hodnôt ORAC in vivo, pretože údaje in vitro nebolo možné spoľahlivo preložiť do klinických prínosov preukázateľných vo vhodne navrhnutých klinických štúdiách [ 73 ].
Belinal ® (extrakt získaný z konárov jedle striebornej) mal antioxidačnú aktivitu proti radikálom ABTS, DPPH a NO, ktorá bola nižšia ako u EGCG, resveratrolu, BHT a kyseliny askorbovej; jeho redukčná sila bola tiež nižšia ako u týchto referenčných látok. V teste lipidovej peroxidácie bol extrakt tiež horší ako BHT a resveratrol. Proti superoxidovému radikálu bol Belinal ® podstatne horší ako EGCG, ale jeho účinky boli lepšie ako účinky resveratrolu. Namiesto toho bol Belinal ® účinnejší proti hydroxylovému radikálu ako resveratrol, BHT a EGCG (kyselina askorbová sa v tomto teste nepoužila ako referencia), čo naznačuje jeho schopnosť prechádzať bunkovými membránami vo vnútri buniek. In vivo, s použitím intracelulárneho testu v Saccharomyces cerevisiae , Belinal ® preukázal antioxidačný účinok porovnateľný s účinkom EGCG a lepší ako u kyseliny askorbovej, resveratrolu, BHT a tokoferylsukcinátu. Antioxidačný účinok sa v podmienkach in vivo so zvyšujúcimi sa koncentráciami zvyšoval nevýznamne, zatiaľ čo pri použitých referenčných látkach sa so zvyšujúcimi sa koncentráciami pozoroval pokles alebo dokonca prooxidačný účinok [ 52 ].
Intracelulárna produkcia ROS bunkami C2C12 v prítomnosti extraktu Belinal® bola v prostredí s vysokým obsahom glukózy výrazne nižšia v porovnaní s extraktom z dreva Castanea sativa Mill. a antioxidačný účinok bol silnejší ako účinok Pycnogenolu. Pokles produkcie ROS sa pozoroval aj v prostredí s nízkym obsahom glukózy, ale v tomto prípade bol účinok silnejší pri nižšej koncentrácii extraktu [ 74 ].
V štúdii simulovaného trávenia (bez prítomnosti črevnej mikrobioty) preukázal Belinal® relatívne dobrú stabilitu v žalúdku počas prvých dvoch hodín a dobrú stabilitu v črevách počas ďalších dvoch hodín. Účinnosť extraktu sa však počas trávenia v žalúdku a črevách znížila približne o 30 % a 20 %, čo bolo stanovené metódou založenou na DPPH [ 52 ].
5.2. Antimikrobiálna aktivita
5.2.1. Antimikrobiálna aktivita esenciálnych olejov
Esenciálne oleje z rôznych rastlinných druhov boli skúmané z hľadiska ich potenciálnych antimikrobiálnych účinkov už v roku 1924 [ 75 ]. Pri interpretácii výsledkov uvedených nižšie treba mať na pamäti, že v literatúre sa odhaduje, že surový extrakt, aby sa mohol považovať za sľubne účinný, musí mať MIC menej ako 100 μg/ml a čistá zlúčenina musí mať MIC menej ako 16 μg/ml [ 76 ].
Uvádza sa, že esenciálne oleje majú vo všeobecnosti tendenciu byť účinnejšie na kvasinky ako na baktérie, ale v štúdii hodnotiacej antimikrobiálne účinky esenciálnych olejov z deviatich druhov a poddruhových taxónov patriacich do rodu Abies (vetvičky s listami) esenciálny olej z A. alba nemal žiadnu aktivitu proti kvasinkám; ten istý esenciálny olej patril aj medzi najmenej účinné proti baktériám [ 75 ]. V in vitro diskovom difúznom teste mali esenciálne oleje z listov A. alba , listov Melaleuca armillaris subsp. armillaris Sm. a M. quinquenervia (Cav.) STBlake pomerne miernu aktivitu proti trom druhom Penicillium ; aktivita esenciálneho oleja z listov A. alba sa však zdala byť najnižšia. In situ, na niekoľkých potravinách, pri najvyššej testovanej koncentrácii (500 µL/l), mali tri esenciálne oleje podobné účinky proti Penicillium citrinum ; esenciálny olej z listov A. alba mal strednú aktivitu (medzi tromi olejmi) proti P. expansum ; a najnižšiu aktivitu proti P. crustosum . V každom prípade je 500 µL/l dosť vysoká hodnota [ 40 ].
Proti Penicillium verrucosum bol esenciálny olej pripravený zo šišiek účinnejší ako esenciálny olej pripravený z ihličia (MIC 6,25 μL/ml oproti 9,38 μL/ml). Obe aktivity však boli mierne aj v porovnaní s esenciálnym olejom z oregana ( Origanum vulgare L., 1,17 μL/ml) alebo čistým tymolom (125 μg/ml) [ 77 ].
Salamon a kol. (2019) testovali jedenásť esenciálnych olejov z rôznych druhov rastlín vrátane A. alba (časť rastliny neuvedená) pomocou diskovo-difúznej metódy. Zistili, že esenciálny olej mal slabú alebo žiadnu aktivitu proti baktériám, ale mal druhú najsilnejšiu aktivitu proti Candida albicans (ATCC 885-653); tento účinok bol však menší ako polovica účinku zaznamenaného pre esenciálny olej z Thymus vulgaris L. Podobné výsledky sa pozorovali aj pri testovaní rovnakých esenciálnych olejov na klinických izolátoch, s tým rozdielom, že v tomto prípade mal olej získaný z A. alba tretiu najsilnejšiu aktivitu proti Candida albicans , ktorá bola len mierne nižšia ako účinok pozorovaný u esenciálneho oleja získaného z Pinus sylvestris L. Hoci časti rastliny neboli v tejto práci uvedené, autori uviedli v zložení esenciálneho oleja nasledujúce zlúčeniny: limonén (24,0 ± 2,0 %); bornylacetát (18,0 ± 1,0 %); α-pinén (15,0 ± 1,0 %) a borneol (2,2 ± 0,2 %) [ 78 ].
Bağci a Diğrak [ 75 ] použili metódu diskovej difúzie; pre mnohé bakteriálne druhy bol olej z A. alba (vetvičky a listy) úplne neaktívny alebo spôsoboval inhibičné plochy s veľkosťou 9 mm alebo menej (iba pri koncentráciách 6,0 – 9,0 μg/disk; pri nižších koncentráciách nevykazoval žiadnu aktivitu) [ 75 ]. Výsledky sú vo všeobecnosti v súlade so štúdiou diskovej difúzie vykonanou na esenciálnom oleji získanom z vetvičiek a listov z kórejských vzoriek. U piatich bakteriálnych druhov sa nezistili žiadne antibakteriálne účinky, zatiaľ čo u S. aures 25 μl esenciálneho oleja preukázalo približne 70 % inhibičných účinkov gentamicínu (25 μg) [ 35 ]. Treba však vziať do úvahy, že 25 μl esenciálneho oleja zodpovedá hmotnosti približne 20 mg, nie 25 μg, t. j. znamená koncentráciu približne 800-krát vyššiu (za predpokladu hustoty esenciálneho oleja okolo 0,8 g/ml), ale aj zmes s najmenej 30 – 40 zlúčeninami – mnohé len v stopách alebo malých množstvách. Mitić a kol. (2022) [ 39 ] hodnotili esenciálny olej pripravený z listov troch rodov Abies proti 17 mikrobiálnym druhom a vo všetkých z nich olej z A. alba nepreukázal žiadny antimikrobiálny účinok až do veľmi vysokých koncentrácií (20 mg/ml).
Garzoli a kol. (2021) odhadli hodnoty MIC a MBC pre esenciálny olej získaný z ihličia proti Escherichia coli , Pseudomonas fluorescens a Kocuria marina na 51,28 mg/ml, čo je obrovská hodnota v porovnaní s hraničnou hodnotou 100 μg/ml. Pre Acinetobacter bohemicus a Bacillus cereus boli odhadované hodnoty MIC mierne nižšie, 12,82 mg/ml a 25,64 mg/ml, ale stále sú veľmi vysoké v porovnaní s prahovou hodnotou. Tí istí autori tiež hodnotili antibakteriálne účinky esenciálneho oleja v plynnej fáze metódou diskovej difúzie a nezistili žiadny účinok proti E. coli a P. fluorescens , zatiaľ čo jeho aktivita proti A. bohemicus , K. marina a B. cereus bola hodnotená ako silnejšia ako v kvapalnej fáze [ 37 ]. Okrem toho, ak je cieľom napríklad zabezpečiť príjemnú vôňu v miestnosti a zároveň znížiť mikrobiálnu záťaž, aplikácia oleja v plynnej fáze môže byť uskutočniteľnejšia.
V štúdii hodnotiacej antimikrobiálne účinky 15 esenciálnych olejov z rôznych druhov rastlín sa zistilo, že esenciálny olej z ihličia A. alba je najúčinnejší proti Clostridium butyricum , Clostridium intestinale a Clostridium ramosum . Hodnoty MIC pre tento esenciálny olej proti týmto druhom však boli 0,25, 1,70 a 0,25 μL/ml [ 71 ]. To zodpovedá približne 20 μg/ml, 1360 μg/ml a 20 μg/ml, čo je stále nad hraničnou hodnotou 16 μg/ml, ktorá ich považuje za sľubne účinné. V porovnaní s účinkami hlásenými pre esenciálne oleje z A. alba proti iným bakteriálnym druhom sa tieto účinky proti Clostridium zdajú byť podstatne silnejšie. Je zaujímavé, že chemické zloženie tohto esenciálneho oleja sa dosť líšilo od zloženia hláseného pre väčšinu olejov získaných z tohto druhu: bornylacetát (30 %); kamfén (18 %); α-pinén (3 %); borneol (1,5 %). a α-terpinén (1,2 %) (zvyšok zlúčenín nie je uvedený v referenčnom zdroji) [ 71 ].
Șandru (2015) hodnotil 12 esenciálnych olejov z rôznych rastlinných druhov z hľadiska ich účinku na E. coli pomocou diskovej difúznej metódy [ 79 ]. Esenciálny olej z A. alba (časti rastliny neboli špecifikované, chemické zloženie nebolo uvedené) patril medzi najaktívnejšie s inhibičnými zónami 17,3 – 18,1 mm (v závislosti od času merania). Autor však použil vysoké množstvo esenciálneho oleja, 100 μl/disk, čo zodpovedá približne 80 mg/disk.
Limonén, ktorý je jednou z hlavných zlúčenín esenciálnych olejov z A. alba , bol opísaný v článku, ktorý hodnotil viacero prírodných terpénových zložiek s MBC 6000 μg/g (6 mg/g) alebo vyššou proti niekoľkým bakteriálnym druhom [ 80 ], a to aj napriek skutočnosti, že experimentálne dôkazy ukázali, že limonén je schopný narušiť lipidový profil mikrobiálnych cytoplazmatických membrán [ 81 ]. V inej štúdii boli pre limonén zaznamenané hodnoty MIC 2 – 27 mg/ml, čo potvrdzuje pomerne nízky antimikrobiálny účinok [ 82 ].
V štúdii in vitro sa hodnoty MIC pre (+)-α-pinén pohybovali medzi 117 a 3125 μg/ml pre tri druhy húb, zatiaľ čo MIC pre rovnaký izomér proti MRSA bola 4,1 mg/ml; enantiomér (−)-α-pinénu bol údajne úplne bez antimikrobiálnej aktivity. Hodnoty MIC pre (+)-β-pinén boli medzi 187 a 780 μg/ml pre rovnaký druh húb a MIC pre rovnaký izomér proti MRSA bola 6,2 mg/ml; enantiomér (−)-β-pinénu bol tiež úplne bez antimikrobiálnej aktivity [ 83 ]. V inom hodnotení sa hodnoty MIC pre gram(+) baktérie α-pinénu (enantiomér neuvedený/zaškrtnutý) pohybovali medzi 0,75 a 1,29 % ( v / v ), zatiaľ čo pre β-pinén (enantiomér neuvedený/zaškrtnutý) sa pohybovali medzi 1,16 a > 2,0 % ( v / v ); V prípade gram(−) baktérií sa hodnoty MIC pre α-pinén pohybovali medzi 1,05 a 1,59 % ( v / v ), zatiaľ čo v prípade β-pinénu sa pohybovali medzi 1,80 a > 2,0 % ( v / v ) [ 84 ].
Kamfén má tiež pomerne miernu antibakteriálnu aktivitu, pričom rôzne štúdie uvádzajú MIC pre reprezentatívne Gram (+) a Gram (−) patogény väčšie ako 120 µg/ml [ 85 ]. Pokiaľ ide o bornylacetát, hodnoty MIC vyššie ako 1 mg/ml boli hlásené proti S. aureus , S. epidermidis a súboru gramnegatívnych bacilov [ 86 ]. α-Terpineol a terpinen-4-ol majú MIC nižšie ako α-pinén proti Staphylococcus aureus , S. epidermidis a Propionobacterium acnes , ale v tomto esenciálnom oleji sú prítomné iba v malých množstvách. V tej istej práci [ 87 ] autori zistili silnejší účinok α-pinénu ako α-terpineolu a terpinen-4-olu v TLC-bioautografii; to je však v rozpore nielen s hodnotami MIC z tej istej štúdie, ale aj s minimálnou baktericídnou koncentráciou (MBC) stanovenou Cosentinom a kol. (1999) pre α-pinén, ktorý bol viac ako 900 μg/ml [ 88 ]. Uvádza sa tiež, že borneol má určité antibakteriálne účinky (horšie ako chloramfenikol) [ 89 ] a je tiež prítomný v nízkych množstvách v esenciálnych olejoch z A. alba . p -cymén, γ-terpinén a linalool sú nielen prítomné v nízkych množstvách v esenciálnych olejoch produktov z A. alba , ale ich hodnoty MBC boli tiež odhadnuté na viac ako 900 μg/ml pre všetky bakteriálne druhy, na ktorých boli testované [ 88 ].
Esenciálne oleje pripravené zo semien a šupín šišiek majú tiež relatívne nízke antimikrobiálne účinky v porovnaní s tymolom ako pozitívnou kontrolou. Esenciálne oleje zo semien a šupín šišiek A. alba mali menšie inhibičné účinky ako oleje z A. koreana . Preto je nepravdepodobné, že by antimikrobiálne účinky esenciálnych olejov zo semien alebo šišiek boli skutočne klinicky zaujímavé. Podobne esenciálne oleje pripravené z listov alebo vetvičiek majú len miernu antimikrobiálnu aktivitu, zatiaľ čo oleje z A. koreana boli opísané ako silnejšie. Minimálne inhibičné koncentrácie (MIC) proti rôznym gram(+) a gram(-) baktériám sa pohybovali medzi 10,0 a 28,5 μL/ml pre esenciálne oleje získané zo semien alebo šišiek A. koreana a medzi 16,5 a 33,0 μL/ml pre oleje pripravené z produktov A. alba [ 33 ].
Lanzerstorfer a kol. (2019) uviedli, že po aplikácii zmesi esenciálnych olejov z Citrus limon (L.) Osbeck (časť rastliny neuvedená, ale z dostupných obchodných informácií o produkte pochádza z oplodia) a A. alba (časť neuvedená, ale z dostupných obchodných informácií o produkte pochádza z ihličia a konárov) pomocou ultrazvukových odparovačov (typ VASE) (2 – 3 mg m –3 ) sa pozoroval priemerný pokles koncentrácie baktérií približne o 40 % počas dvoch hodín po rozptýlení vo vzduchu. V prípade druhov húb sa zaznamenal priemerný pokles o 30 – 60 % v závislosti od oddelenia, kde sa oleje aplikovali [ 41 ].
Záverom možno konštatovať, že pôsobivé množstvo výskumov konzistentne uvádza vysoké hodnoty MIC pre esenciálne oleje z A. alba (v porovnaní s vyššie uvedenými orientačnými hraničnými hodnotami) a vysoké hodnoty MIC hlásené pre hlavné zlúčeniny týchto esenciálnych olejov. Nízka antimikrobiálna aktivita hlásená doteraz pre esenciálne oleje z A. alba je teda v súlade s ich chemickým zložením a so všeobecnými poznatkami o antimikrobiálnej aktivite ich hlavných zložiek.
5.2.2. Antimikrobiálna aktivita rôznych extraktov z A. alba
80 % metanolový extrakt z ihličia bol testovaný proti trom fytopatogénnym hubám a buď úplne nevykazoval žiadnu aktivitu ( Fusarium oxysporum , Phytophthora cambivora ), alebo mal nízku úroveň aktivity ( Alternaria alternata ) [ 90 ].
Hydrofilné extrakty bohaté na lignany a rôzne fenolové zlúčeniny tiež nemali alebo mali minimálnu antifungálnu aktivitu na Trametes versicolor , Schizophyllum commune , Gloeophyllum trabeum a Penicillium expansum [ 18 ]. Extrakty z dreva hrčov a konárov z A. alba mali veľmi slabý inhibičný účinok na Trametes versicolor, Schizophyllum commune a Gloeophyllum trabeum , pričom 5 % roztoky spôsobili priemernú inhibíciu plesní približne 20 % a 1 % roztoky nespôsobili žiadnu inhibíciu. Situácia bola podobná pre dva testované druhy plesní, Penicillium expansum a Fusarium solani , pričom pri 5 % roztokoch sa pozorovala približne 25 % inhibícia a pri 1 % roztokoch približne 10 % inhibícia [ 22 ]. Tieto zistenia boli v silnom súlade so zisteniami, ktoré uviedli Välimaa a kol. (2007), ktorí skúmali veľké množstvo hydrofilných extraktov z uzlov alebo kôry získaných z 30 druhov stromov, a to ako z mäkkých (t. j. nahosemenných) alebo tvrdých (krytosemenných) stromov. V predbežnom skríningu zistili, že extrakt z uzlov jedle striebornej bol úplne neúčinný proti väčšine testovaných druhov baktérií a kvasiniek; jediný pozitívny účinok bol zaznamenaný proti B. cereus , ale bol veľmi slabý (11 % inhibícia). Tento nedostatok účinku bol potvrdený aj v podrobnejších hodnoteniach, keď sa ukázalo, že ten istý extrakt takmer nemá žiadny účinok (pre väčšinu testovaných druhov bola priemerná inhibícia 0 % alebo blízka 0 %; pre Candida albicans bola hlásená 15 % inhibícia, ale táto hodnota bola v porovnaní s extraktmi z druhov Pinus , u ktorých bola inhibícia viac ako 80 %) menšia [ 91 ].
5.3. Cytotoxicita a toxicita
5.3.1. Cytotoxická aktivita esenciálnych olejov z A. alba
Esenciálny olej získaný z listov a vetvičiek A. alba nemal žiadny vplyv na prežitie ľudských fibroblastových buniek (línia CCD-986 SK) počas 24 hodín pri koncentráciách 1 % alebo nižších, ale pri koncentrácii 5 % rýchlo a významne znížil schopnosť buniek prežiť, pričom po 6 hodinách klesla na 34 % a po 24 hodinách na 6,3 % [ 35 ].
Esenciálne oleje pripravené z listov troch druhov jedle ( A. alba , A. cephalonica a A. borisii-regis ) boli hodnotené z hľadiska ich toxicity voči naupliám Artemia salina a všetky vykazovali relatívne silnú toxicitu (LC50 menej ako 100 mg/l), ale spomedzi týchto troch bol esenciálny olej z A. alba odhadnutý ako olej s najnižšou toxicitou. Autori špekulovali, že nižšia toxicita tohto esenciálneho oleja v porovnaní s ostatnými dvoma by súvisela s jeho vysokým obsahom kamfénu a limonénu, ktoré sa považujú za menej toxické spomedzi mono- a seskviterpénov troch esenciálnych olejov. Tie isté tri esenciálne oleje vykazujú aj určitú toxicitu voči larvám Drosophila melanogaster , pričom olej z A. alba má tiež najnižšiu toxicitu [ 39 ].
Esenciálne oleje zo semien a šišiek z A. alba (rovnako ako tie z A. koreana ) boli slabo aktívne proti bunkovým líniám MCF-7 (rakovina prsníka u ľudí) a MDA-MB-231 (veľmi agresívna, invazívna a slabo diferencovaná rakovina prsníka). Hodnoty IC50 , okolo 100 μg/ml, boli veľmi blízke hodnotám IC50 odhadovaným v normálnych ľudských fibroblastoch. To naznačuje veľmi obmedzenú selektivitu a nedostatok potenciálu pre použitie týchto esenciálnych olejov proti rakovine. Autori predpokladajú, že tento nízky účinok súvisí so skutočnosťou, že v oboch bunkách bola dominantnou zlúčeninou (-) izomér limonénu, zatiaľ čo na základe údajov z literatúry by mal (+) limonén zaujímavé protinádorové účinky bez toho, aby spôsoboval dysfunkciu orgánov. Autori však dospeli k záveru, že pri koncentráciách v rozmedzí 1 – 50 μg/ml boli oleje „pomerne bezpečné“. Tieto dva esenciálne oleje boli pre normálne ľudské bunky menej toxické ako tymol [ 33 ].
5.3.2. Cytotoxická aktivita rôznych extraktov z A. alba
Zdá sa, že Abigenol ® /AlbiPhenol ® nemá významný vplyv na zdravie alebo priepustnosť črevného epitelu. Maximálna koncentrácia, pri ktorej bol Abigenol ® /AlbiPhenol ® netoxický, bola 1000 µg/ml pre bunky HUVEC, 700 µg/ml pre bunky H9c2 a 1200 µg/ml pre bunky HepG2 [ 55 ].
Belinal® spustil významný pokles prežívajúcich mezenchymálnych kmeňových/stromálnych buniek (MSC ) (približne 20 % buniek zostalo životaschopných); mierne výraznejší účinok (v rovnakom zmysle) bol pozorovaný u pyknogenolu, resveratrolu a kvercetínu. Avšak v tomto experimente, aj v kontrolnej skupine, bola pozorovaná životaschopnosť 50 – 60 %; preto autori pre ďalšie experimenty zvolili koncentráciu 375 µg/ml (čo bola najnižšia testovaná koncentrácia) [ 25 ]. Nízke koncentrácie (5 alebo 10 μg/ml) Belinalu® nemajú žiadny vplyv na životaschopnosť myšej myoblastovej bunkovej línie C2C12 [ 74 ].
Extrakty z hrčového dreva získané z A. alba boli prakticky neškodné pre bunky Hepa-1 [ 91 ].
5.4. Vplyv na chondrogenézu
In vitro, v porovnaní s kontrolnou skupinou a pyknogenolom, resveratrolom a kvercetínom, Belinal® podporoval chondrogenézu v ľudských mezenchymálnych kmeňových/stromálnych bunkách (hMSC) odvodených z kostí od pacientov s osteoartrózou. Takýto účinok sa však nepozoroval u MSC získaných od zdravých darcov (po smrti), pričom autori špekulujú, že tento rozdiel by mohol byť spôsobený nižším chondrogénnym potenciálom hMSC získaných od pacientov s osteoartrózou v porovnaní so zdravými darcami [ 25 ].
5.5. Prebiotické účinky
Stojanov a kol. (2021) informovali o účinkoch komerčného dreveného extraktu (Belinal® ) , ktorý údajne obsahuje rôzne molekuly lignanov, ako aj fenoly a sacharidy, na desať rôznych druhov Lactobacillus , z ktorých niekoľko bolo izolovaných u ľudí. Zistili, že extrakt pôsobí ako prebiotikum pre niekoľko z týchto druhov: L. paracasei, L. rhamnosus a L. acidophilus (črevného pôvodu), L. gasseri a L. crispatus (vaginálneho pôvodu) a L. bulgaricus (druh používaný v potravinárskom priemysle). Zložky extraktu, ktoré pôsobia ako prebiotiká, neboli identifikované, hoci autori špekulovali, že by to mohli byť oligosacharidy alebo iné sacharidy [ 26 ].
5.6. Antidiabetické účinky
Vychádzajúc z antidiabetických účinkov hlásených pre Pycnogenol, ktoré sa pripisujú inhibícii α-amylázy a α-glukozidázy, Lunder a kol. testovali Belinal® , ako aj extrakt pripravený z kôry A. alba , aby posúdili ich účinky na tieto isté enzýmy, ako aj na dipeptidylpeptidázu 4 (DPP4). V tejto štúdii sa použili vysoké koncentrácie extraktov na základe rozumného predpokladu, že po perorálnom podaní sú takéto vysoké koncentrácie dosiahnuteľné. Dva extrakty z A. alba vykazovali to, čo autori opísali ako „veľký in vitro inhibičný potenciál“ pre všetky tri enzýmy. V prípade α-glukozidázy mal Belinal® najnižšiu odhadovanú hodnotu IC50 ( 1,4 mg/ml), zatiaľ čo extrakt z kôry mal IC50 2,1 mg/ml, čo je presne rovnaký odhad (2,1 mg/ml) hlásený pre Pycnogenol. Tieto hodnoty IC50 sú nižšie ako hodnoty odhadované pre Farmatan® , priemyselný extrakt získaný z dreva Castanea sativa [ 74 ].
V prípade α-amylázy bol najsilnejší inhibičný účinok pozorovaný pri Pygnogenole (IC50 1,5 mg/ml), nasledovanom extraktom z kôry A. alba (IC50 3,3 mg/ml). Účinok Belinalu® bol slabší (11,8 mg/ml); iba extrakt z dreva C. sativa mal vyššiu hodnotu IC50 ( 38,2 mg/ml) [ 74 ].
Extrakt z kôry A. alba mal najsilnejší inhibičný účinok na DPP4 (IC50 3,4 mg/ml) spomedzi hodnotených extraktov, nasledovaný Pycnogenolom (IC50 4,8 mg/ml), Belinalom® ( IC50 5,2 mg/ml) a Farmatanom (IC50 9,1 mg/ml) [ 74 ].
Hoci enzymatické inhibičné účinky týchto extraktov boli opísané ako „účinné“, ich hodnota je stále relatívne vysoká, vzhľadom na to, že napríklad pre fukoidán extrahovaný z rias druhu Ascophyllum nodosum bola IC50 nižšia ako 0,05 mg/ml [ 92 ], ale keďže v čreve sa dajú dosiahnuť relatívne vysoké koncentrácie, tieto zistenia by mohli mať klinický význam.
Autori hodnotili deväť lignanov (lariciresinol, matairesinol, nortrachelogenín, pinoresinol, sekoisolariciresinol diglukozid, 7-hydroxymatairesinol, izolariciresinol, pinoresinol diglukozid a sekolariciresinol) nachádzajúcich sa v extraktoch z A. alba . Zistili, že pinoresinol diglukozid a izolariciresinol pri koncentrácii 1 mg/ml spôsobujú výraznú inhibíciu DPP4 (takmer 50 % inhibícia); všetky ostatné boli menej aktívne na DPP4 a úplne neaktívne alebo len slabo aktívne na α-glukozidázu a α-amylázu. Pri rovnakej koncentrácii (1 mg/ml) spôsobil Belinal ® približne 40 % inhibíciu α-glukozidázy, 15 % inhibíciu α-amylázy a 32 % inhibíciu DPP4. Zdá sa však, že lignany nie sú jedinými zlúčeninami zodpovednými za antidiabetické účinky, keďže tí istí autori preukázali, že najmenej tri prírodné fenolové kyseliny (gallová, protokatechová a p- hydroxybenzoová) sú stredne silnými inhibítormi α-amylázy, zatiaľ čo kyselina p -kumarová je inhibítorom α-glukozidázy [ 74 ].
Účinnosť Belinalu® pri kontrole glykémie bola hodnotená v malej klinickej štúdii ( n = 31) na zdravých dobrovoľníkoch s normálnym BMI a normálnou odpoveďou na perorálny glukózový tolerančný test [ 93 ]. Táto štúdia bola dvojito zaslepená, randomizovaná a používala skrížený dizajn zahŕňajúci vstupnú návštevu plus štyri testovacie návštevy s vymývacím obdobím jeden týždeň. Pri každom zo štyroch prípadov subjekty skonzumovali 100 g bieleho chleba a dostali jeden zo skúšaných produktov: placebo; 200 mg Belinalu® ; 200 mg gaštanového extraktu; alebo 50 mg akarbózy. Po 90 minútach boli hodnoty glykémie významne vysoké pre placebo a gaštanový extrakt, ale nie pre akarbózu alebo Belinal® . Po 120 minútach sa koncentrácie v štyroch skupinách významne nelíšili od počiatočných hodnôt nalačno. Autori dospeli k záveru, že Belinal® bol len mierne horší ako akarbóza, ale lepší ako placebo a extrakt z gaštanového dreva. Priemerná postprandiálna koncentrácia inzulínu bola v skupine s akarbózou približne o 30 % nižšia ( p = 0,048), o 25 % nižšia v skupine s Belinalom® ( p = 0,010) a iba o 4 % nižšia v skupine s gaštanovým drevom ( p > 0,05; hodnota nie je uvedená v zdrojovej publikácii). Glykemický index štandardného jedla konzumovaného s Belinalom® bol 65 % a jedla konzumovaného s akarbózou 57 %; obe sa štatisticky významne líšili od štandardného jedla konzumovaného s placebom (100 %), ale medzi sebou sa štatisticky nelíšili ( p = 0,27). Glykemický index štandardného jedla konzumovaného s extraktom z gaštanového dreva bol 87 % a významne sa nelíšil od štandardného jedla konzumovaného s placebom [ 93 ]. Výsledky sú povzbudivé, ale vzhľadom na obmedzenia tejto štúdie (skreslenie malej veľkosti vzorky, nedostatok transparentnosti pri prideľovaní liečby a populácia pozostávajúca zo zdravých dobrovoľníkov a nie diabetických pacientov) je potrebné potvrdenie v klinických štúdiách, ktoré sú správne navrhnuté a vykonané.
5.7. Steatóza pečene
V in vitro modeli steatózy pečene s použitím pečeňovej bunkovej línie HepG2 a kyseliny olejovej ako spúšťača akumulácie tuku extrakt Abigenol® / AlbiPhenol® výrazne znížil hromadenie lipidov v pečeňových bunkách indukované kyselinou olejovou pri koncentrácii 0,5 mM, ale nie pri použití kyseliny olejovej v koncentrácii 1 mM. Extrakt spustil 68,8 % zníženie cholesterolu v hepatocytoch HepG2 pri použití v koncentrácii 1200 µg/ml, ale nie pri nízkej biologicky dostupnej koncentrácii 2,7 µg/ml. Obmedzené dôkazy naznačujú, že tento účinok možno čiastočne vysvetliť miernym zvýšením biosyntézy žlčových kyselín v dôsledku zníženia cholesterolu [ 55 ].
5.8. Kardiovaskulárne účinky
Ex vivo, v modeli ischemicko-reperfúzneho poškodenia, sa uvádza, že extrakt SFTE bohatý na fenol mal významný kardioprotektívny účinok na izolované srdcia potkanov. Kyselina p -kumarová a protokatechuová, o ktorých autori predpokladali, že sú účinnými zložkami extraktu, mali nižší účinok ako extrakt. Rýchlosti uvoľňovania LDH (súvisiace so závažnosťou ischémie a poškodením myokardu) boli zmiernené SFTE koncentračne závislým spôsobom (účinok bol výraznejší pri 100 µg/l ako pri 10 µg/l), zatiaľ čo kyselina p -kumarová a protokatechuová takéto účinky nemali. SFTE tiež spôsobil koncentračne závislý nárast koronárneho prietoku porovnateľný s nárastom pozorovaným pri kyseline p -kumarovej (ale nie pri kyseline protokatechuovej); to naznačuje vazodilatačný účinok, o ktorom autori špekulujú, že čiastočne súvisí s interferenciou so signálnou dráhou NO syntázy a čiastočne s antioxidačnými účinkami extraktu. Skutočnosť, že L-NNA, inhibítor eNOS, tento účinok potlačil, potvrdzuje mechanizmus dráhy NO syntázy. Hoci SFTE nemalo významný vplyv na srdcovú frekvenciu, autori uviedli, že „zdá sa, že obnovuje hodnoty srdcovej frekvencie pred ischemickou chorobou“. V tej istej ex vivo štúdii pre SFTE sa uvádza významné zníženie celkového trvania arytmií v období reperfúzie o 80 %. Táto veľkosť účinku bola väčšia ako tá, ktorá sa pozorovala u dvoch prírodných kyselín (40 % zníženie kyselinou p -kumarovou a 45 % zníženie kyselinou protokatechuovou) [ 94 ]. Celkovo táto sada experimentov naznačuje kardioprotektívny účinok extraktu SFTE, ale je potrebné ešte neklinické a klinické potvrdenie.
Extrakt SFTE (extrakt z kmeňa jedle striebornej), bohatý na polyfenoly, tiež preukázal ochranné účinky proti negatívnym účinkom na arteriálnu funkciu a zmenám v morfológii tepien vyvolaným aterogénnou diétou u morčiat [ 27 , 94 ]. Hrudné aortálne prstence zvierat, ktoré boli vopred stiahnuté fenylefrínom, sa uvoľnili pod vplyvom acetylcholínu. Avšak v prípade zvierat vystavených aterogénnej diéte sa rozsah tejto relaxácie drasticky znížil, zatiaľ čo SFTE relaxačný účinok výrazne zlepšil. Predpokladá sa, že tento vazorelaxačný účinok je aspoň čiastočne spojený s mechanizmom súvisiacim s NO, ale určite nie s priamym pôsobením na bunky hladkého svalstva. Vnútro brušných aort morčiat vykazovalo významný nárast aterosklerotických plakov v porovnaní s negatívnymi kontrolami. Zaradenie SFTE do diéty zodpovednej za aterosklerózu však významne znížilo výskyt aterosklerózy (približne o 80 %) [ 27 ].
Pri koncentrácii 700 µg/ml extrakt Abigenol® / AlbiPhenol® významne inhiboval aktivitu angiotenzín konvertujúceho enzýmu (ACE) v bunkách H9c2, ale nie v bunkách HUVEC pri koncentrácii 1000 µg/ml. Keďže veľkosť účinku inhibície ACE v bunkách H9c2 bola mierna (inhibícia približne 10 – 15 %) [ 55 ], praktický význam tohto zistenia sa javí prinajlepšom nejasný bez ďalších údajov.
5.9. Antipsoriatické účinky
Masť na báze extraktu z kôry jedle striebornej (ABI) 2 %, bohatá na polyfenoly, bola hodnotená v malej ( n = 61, z ktorých 56 dokončilo štúdiu), randomizovanej, dvojito zaslepenej, placebom kontrolovanej, pravo-ľavej klinickej štúdii u pacientov s psoriázou. Masť sa aplikovala 12 týždňov alebo kým nebola ošetrovaná oblasť čistá. Extrakt významne a podstatne inhiboval IL-1β, ale inak nemal žiadny významný vplyv na hladiny IL-6, IL-8, IL-10, IL-12p70 a TNF-α. Pokles hladín IL-1β sa pripisuje polyfenolovej frakcii, keďže podobný účinok bol pozorovaný aj pri podobnom extrakte z kôry borovice borovej (Pinus pinaster) . Autori uviedli 15 % rozdiel v zlepšení symptómov v prospech extraktu oproti placebu, ale nebol štatisticky významný (a to by mohlo súvisieť s malou veľkosťou vzorky použitej v štúdii, ale aj za predpokladu, že účinok bol významný, jeho veľkosť je relatívne malá) [ 95 ].
5.10. Protinádorové účinky
Karkabounas a kol. (2000) uviedli účinky vodného extraktu získaného zo zmesi A. alba a Viscum album se abies , t. j. imelo parazitujúce na jedli striebornej. Na bunkách L-1210 (myšia lymfocytová leukémia) bola odhadnutá hodnota IC50 49,6 ± 1,4 mg/l. V modeli karcinómu indukovaného benzo(α)pyrénom (BaP) u (samcov) potkanov Wistar autori tvrdili, že extrakt u zvierat liečených BaP v porovnaní s kontrolnou skupinou predĺžil život a znížil rýchlosť rastu nádoru, mierny účinok inhibície indukcie nádoru (o 16,6 %) a predĺžil život a vyvolal nekrotické účinky na malígne bunky, keď bol extrakt podávaný zvieratám s už vytvorenými nádormi indukovanými BaP [ 96 ].
5.11. Farmakokinetika
Údaje in vitro naznačujú, že gastrointestinálne trávenie Belinalu® nemá významný vplyv na molekuly lignanov [ 25 ] v tom zmysle, že nie sú podstatne degradované. Nie sú k dispozícii žiadne farmakokinetické údaje in vivo pre extrakty z A. alba , a to ani u zvierat, ani u ľudí.
6. Závery
V posledných troch desaťročiach sa druhu A. alba venovalo pôsobivé množstvo výskumu . Ide prevažne o fytochemické štúdie; uskutočnilo sa však aj množstvo štúdií o biologických alebo farmakologických účinkoch prchavých olejov alebo extraktov získaných z rôznych častí rastliny. Variabilita esenciálnych olejov (či už pochádzajú z listov, oleorezínu z konárov alebo iných častí rastliny) je pôsobivá, a to aj medzi vzorkami zozbieranými z rovnakej geografickej oblasti. Zdá sa, že aj obdobie zberu podstatne ovplyvňuje chemické zloženie esenciálnych olejov. V prípade esenciálnych olejov pripravených z ihličia alebo vetvičiek a konárov sú hlavnými zlúčeninami limonén, β-pinén, α-pinén, kamfén, β-felandrén a bornylacetát, hoci ich široké variácie zrejme zodpovedajú viacerým chemotypom. Extrakcia superkritickou kvapalinou z rovnakých častí rastliny vedie k tomu, že esenciálne oleje sú chudobnejšie na monoterpény a oveľa bohatšie na seskviterpény (27,3 – 30,0 %) ako pri destilácii parou (kde seskviterpény predstavujú najviac 3 – 4 %). Esenciálne oleje získané z kortikálneho oleorezínu sú tiež bohatšie na seskviterpény ako esenciálne oleje z ihličia (13,5 – 30,8 % v závislosti od niekoľkých premenných vrátane ročného obdobia zberu), hoci hlavné monoterpény sú približne rovnaké (limonén, β-pinén, α-pinén, kamfén, bornylacetát). Doterajšie výskumy ukázali, že α-pinén je prevládajúcou zlúčeninou v esenciálnom oleji zo šišiek spolu s ďalšími monoterpénmi, ako sú limonén, β-pinén a verbenón. Z doteraz dostupného obmedzeného výskumu vyplýva, že v esenciálnom oleji zo semien dominuje limonén (70,1 – 82,9 %) a α-pinén (6,3 – 11,5 %). Kôra aj drevo sú bohaté na lignany a fenolové zlúčeniny. Matairesinol je zrejme dominantným lignanom v kôre a sekoisolariciresinol a lariciresinol sú dominantné vo vzorkách dreva.
Zdá sa, že esenciálne oleje a rôzne extrakty (z rôznych častí rastliny) majú nezanedbateľné antioxidačné účinky. Namiesto toho sa zdá, že rôzne esenciálne oleje aj extrakty z rôznych častí A. alba buď nemajú antibakteriálne účinky, alebo majú len veľmi mierne takéto účinky. Esenciálne oleje aj rôzne extrakty sú relatívne bezpečné, čo sa týka ich účinkov na viacero bunkových línií, s malou alebo žiadnou cytotoxicitou. V niekoľkých in vitro alebo neklinických experimentoch vykonaných s rôznymi extraktmi boli zaznamenané povzbudivé výsledky, pokiaľ ide o ich prebiotické účinky, ich pozitívne účinky na chondrogenézu a steatózu pečene, ako aj ich antidiabetické, kardiovaskulárne a protinádorové účinky. Ich antipsoriatické účinky sa zdajú byť príliš obmedzené na to, aby boli skutočne klinicky zaujímavé.
Očakáva sa, že budúcnosť prinesie nové údaje týkajúce sa fytochémie, ako aj biologickej a farmakologickej aktivity druhu. Korelácia fytochémie s genetickým zložením analyzovaných vzoriek by zlepšila naše pochopenie pozorovanej širokej variability, najmä pokiaľ ide o esenciálne oleje; zistenie, že epigenetické aspekty sú rovnako dôležité, by však nemalo vedeckú komunitu prekvapiť. Väčšina farmakologického výskumu sa doteraz zameriavala na viac či menej charakterizované extrakty, ale identifikácia kľúčových účinných látok a ich mechanizmov účinku v prípade pozitívnych výsledkov by mala zostať prioritou budúceho výskumu. Okrem toho sa očakáva, že v budúcnosti sa preskúmajú nové terapeutické oblasti s použitím rôznych extraktov a čistých zlúčenín odvodených z A. alba .
Príspevky autorov
Konceptualizácia, R.A. a M.D.; metodika, R.A.; vyšetrovanie, R.A., M.V.H., A.M., A.I.A. a M.D.; kurátorstvo údajov, R.A., M.V.H., A.I.A. a M.D.; písanie – príprava pôvodného návrhu, R.A.; písanie – recenzia a úprava, R.A., M.V.H., A.M., A.I.A. a M.D.; vizualizácia, R.A.; dohľad, MUDr. Všetci autori si prečítali a súhlasili s publikovanou verziou rukopisu.
Vyhlásenie o dostupnosti údajov
Zdieľanie údajov sa neuplatňuje.
Konflikty záujmov
R.A. v minulosti dostával poplatky za poradenstvo alebo rečníkov od UCB, Sandoz, Abbvie, Zentiva, Teva, Laropharm, CEGEDIM, Angelini, Biessen Pharma, Hofigal, AstraZeneca a Stada. Všetci ostatní autori neuvádzajú žiadny konflikt záujmov.
Vyhlásenie o financovaní
Publikáciu tohto článku podporila Univerzita medicíny a farmácie Carol Davila prostredníctvom inštitucionálneho programu Publish not Perish.
Poznámky pod čiarou
Zrieknutie sa zodpovednosti/poznámka vydavateľa: Vyhlásenia, názory a údaje obsiahnuté vo všetkých publikáciách sú výlučne vyhláseniami jednotlivých autorov a prispievateľov a nie MDPI a/alebo redaktora. MDPI a/alebo redaktor (redaktori) sa zriekajú zodpovednosti za akúkoľvek ujmu na zdraví ľudí alebo majetku vyplývajúcu z akýchkoľvek nápadov, metód, pokynov alebo produktov uvedených v obsahu.
Referencie
- 1.Duquesnoy E., Castola V., Casanova J. Zloženie a chemická variabilita vetvičkového oleja Abies alba Miller z Korziky. Príchuť Fragr. J. 2007; 22:293–299. DOI: 10.1002/FFJ.1796. [DOI] [Google Scholar]
- 2.Nikolić J.S., Zlatković B.K., Jovanović S.Č., Stojanović G.S., Marin P.D., Mitić Z.S. Ihličkové prchavé látky ako chemofenetické markery v diferenciácii prirodzených populácií Abies alba, A. x borisii-regis a A. cephalonica. Fytochémia. 2021;183:112612. DOI: 10.1016/j.phytochem.2020.112612. [DOI] [PubMed] [Google Scholar]
- 3.Svetová flóra WFO online. 2023. [(stránka navštívená 12. júla 2023)]. Dostupné online: http://www.worldfloraonline.org.
- 4.Benković E.T., Grohar T., Žigon D., Švajger U., Janeš D., Kreft S., Štrukelj B. Chemické zloženie extraktu z kôry jedle striebornej (Abies alba) Abigenol® a jeho antioxidačná aktivita. Ind. Crop. Prod. 2014; 52:23–28. doi: 10.1016/j.indcrop.2013.10.005. [DOI] [Google Scholar]
- 5.Kersten B., Rellstab C., Schroeder H., Brodbeck S., Fladung M., Krutovsky K.V., Gugerli F. Sekvencia mitochondriálneho genómu Abies alba Mill. Odhaľuje vysokú štrukturálnu a kombinatorickú variabilitu. BMC Genomika. 2022;23:776. DOI: 10.1186/s12864-022-08993-9. [DOI] [PMC bezplatný článok] [PubMed] [Google Scholar]
- 6.Bianchi S., Gloess A.N., Kroslakova I., Mayer I., Pichelin F. Analýza štruktúry kondenzovaných trieslovín vo vodných extraktoch z kôrových tkanív smreka obyčajného (Picea abies [krasová]) a jedle striebornej (Abies alba [Mill.]) Použitie hmotnostnej spektrometrie MALDI-TOF. Ind. Plodina. Prod. 2014; 61:430–437. DOI: 10.1016/j.indcrop.2014.07.038. [DOI] [Google Scholar]
- 7.Salem M.Z.M., Nasser R.A., Zeidler A., Elansary H.O., Aref I.M., Böhm M., Ali H.M., Ahmed A.I. Metylované mastné kyseliny zo jadrového dreva a kôry Pinus sylvestris, Abies alba, Picea abies a Larix decidua: Účinok ošetrenia silnou kyselinou. Biologické zdroje. 2015; 10:7715–7724. DOI: 10.15376/biores.10.4.7715-7724. [DOI] [Google Scholar]
- 8.Európska komisia. Spoločné výskumné centrum. Európsky atlas lesných drevín. Úrad pre vydávanie publikácií; Luxembursko: 2016. [Google Scholar]
- 9.Farjon A. Príručka svetových ihličnanov. Koninklijke Brill NV; Leiden, Holandsko: Boston, MA, USA: 2010. [Google Scholar]
- 10.CAB International, redaktor. Encyklopédia lesných stromov CABI. CABI; Oxfordshire, Spojené kráľovstvo: Boston, MA, USA: 2013. [Google Scholar]
- 11.Idzojtic M. Dendrológia: šišky, kvety, plody a semená Európy. Elsevier; Wlatham, MA, USA: 2019. [Google Scholar]
- 12.Petelka J., Plagg B., Säumel I., Zerbe S. Tradičné liečivé rastliny v Južnom Tirolsku (severné Taliansko, južné Alpy): biodiverzita a využitie. J. Ethnobiol. Etnoméd. 2020;16:74. DOI: 10.1186/s13002-020-00419-8. [DOI] [PMC bezplatný článok] [PubMed] [Google Scholar]
- 13.Schoss K., Benedetič R., Kreft S. Obsah fenolov, antioxidačné vlastnosti a extrahovateľné látky v jedli striebornej (Abies alba Mill.) Vetvy sa zmenšujú so vzdialenosťou od kmeňa. Rastliny. 2022;11:333. DOI: 10.3390/plants11030333. [DOI] [PMC bezplatný článok] [PubMed] [Google Scholar]
- 14.Parenti O., Albanese L., Guerrini L., Zanoni B., Zabini F., Meneguzzo F. Celozrnný chlieb obohatený o jedľu striebornú (Abies alba Mill.) Extrakt z ihličia: technologické a antioxidačné vlastnosti. J. Sci. Potravinárske poľnohospodárstvo. 2022; 102:3581–3589. DOI: 10.1002/jsfa.11704. [DOI] [PubMed] [Google Scholar]
- 15.Tofan L., Paduraru C., Amalinei R.L.M., Bunia I., Miron A. Zhodnotenie kôry rumunskej jedle striebornej (Abies alba Mill.) Odpady ako lacný sorbent Cu(II) iónov zo znečistených vôd. Water Sci. Technol. 2016; 74:2314–2324. DOI: 10.2166/wst.2016.415. [DOI] [PubMed] [Google Scholar]
- 16.Albanese L., Bonetti A., D’Acqui L.P., Meneguzzo F., Zabini F. Cenovo dostupná výroba antioxidačných vodných roztokov hydrodynamickým kavitačným spracovaním jedle striebornej (Abies alba Mill.) Ihličie. Potraviny. 2019;8:65. DOI: 10.3390/foods8020065. [DOI] [PMC bezplatný článok] [PubMed] [Google Scholar]
- 17.Butnaru E., Pamfil D., Stoleru E., Brebu M. Charakterizácia kôry, ihličia a šišiek z jedle striebornej (Abies alba Mill.) smerom k zhodnocovaniu lesných zvyškov z biomasy. Bioenergia z biomasy. 2022;159:106413. DOI: 10.1016/j.biombioe.2022.106413. [DOI] [Google Scholar]
- 18.Vek V., Šmidovnik T., Humar M., Poljanšek I., Pec P. Porovnanie obsahu extraktívov v kôre kmeňa a kôre konárov jedle striebornej (Abies alba Mill.) Molekuly. 2022;28:225. DOI: 10.3390/molekuly28010225. [DOI] [PMC bezplatný článok] [PubMed] [Google Scholar]
- 19.Zeneli G., Tsitsimpikou C., Petrakis P.V., Naxakis G., Habili D., Roussis V. Variabilita listovej a kôrovej oleoživice jedle striebornej (Abies alba Mill.) v Albánsku. Z. Naturforschung C. 2001; 56:531–539. DOI: 10.1515/ZNC-2001-7-810. [DOI] [PubMed] [Google Scholar]
- 20.Brennan M., Fritsch C., Cosgun S., Dumarcay S., Colin F., Gérardin P. Výťažok a zloženie fenolových extraktívov kôry z troch komerčne významných mäkkých drevín vykazujú vnútrodruhové a medzidruhové variácie. Fyziológia rastlín. Biochémia. PPB. 2020; 155:346–356. DOI: 10.1016/j.plaphy.2020.07.033. [DOI] [PubMed] [Google Scholar]
- 21.Willför S., Nisula L., Hemming J., Reunanen M., Holmbom B. Bioactive Phenolic Substances in Industrially Important Tree Species. Part 2: Knots and Stemwood of Fir Species. Holzforschung. 2004;58:650–659. doi: 10.1515/HF.2004.119. [DOI] [Google Scholar]
- 22.Vek V., Keržič E., Poljanšek I., Eklund P., Humar M., Oven P. Wood Extractives of Silver Fir and Their Antioxidant and Antifungal Properties. Molecules. 2021;26:6412. doi: 10.3390/molecules26216412. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 23.Brennan M., Hentges D., Cosgun S., Dumarcay S., Colin F., Gérardin C., Gérardin P. Intraspecific Variability of Quantity and Chemical Composition of Ethanolic Knotwood Extracts along the Stems of Three Industrially Important Softwood Species: Abies alba, Picea abies and Pseudotsuga menziesii. Holzforschung. 2021;75:168–179. doi: 10.1515/hf-2020-0108. [DOI] [Google Scholar]
- 24.Kebbi-Benkeder Z., Manso R., Gérardin P., Dumarçay S., Chopard B., Colin F. Knot Extractives: A Model for Analysing the Eco-Physiological Factors That Control the within and between-Tree Variability. Trees. 2017;31:1619–1633. doi: 10.1007/s00468-017-1573-z. [DOI] [Google Scholar]
- 25.Sirše M., Fokter S.K., Štrukelj B., Zupan J. Silver Fir (Abies alba L.) Polyphenolic Extract Shows Beneficial Influence on Chondrogenesis In Vitro under Normal and Inflammatory Conditions. Molecules. 2020;25:4616. doi: 10.3390/molecules25204616. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Stojanov S., Ravnikar M., Berlec A., Kreft S. Interaction between Silver Fir (Abies alba) Wood Water Extract and Lactobacilli. Pharm. 2021;76:614–617. doi: 10.1691/ph.2021.1794. [DOI] [PubMed] [Google Scholar]
- 27.Drevenšek G., Lunder M., Benković E.T., Mikelj A., Štrukelj B., Kreft S. Silver Fir (Abies alba) Trunk Extract Protects Guinea Pig Arteries from Impaired Functional Responses and Morphology Due to an Atherogenic Diet. Phytomedicine. 2015;22:856–861. doi: 10.1016/j.phymed.2015.06.004. [DOI] [PubMed] [Google Scholar]
- 28.Jończyk J. Study of volatile oil from Abies alba Miller. I. Study of raw material. Acta Pol. Pharm. 1970;27:71–77. [PubMed] [Google Scholar]
- 29.Jończyk J. Study of volatile oil from sprigs of Abies alba Miller. II. Study of monoterpene fractions of oil. Acta Pol. Pharm. 1970;27:155–162. [PubMed] [Google Scholar]
- 30.van Wyk B.-E., Wink M. Medicinal Plants of the World: An Illustrated Scientific Guide to Important Medicina Plants and Their Uses. 2nd ed. Timber Press; Portland, OR, USA: 2017. First Impression. [Google Scholar]
- 31.Moukhtar S., Couret C., Rouil L., Simon V. Biogenic Volatile Organic Compounds (BVOCs) Emissions from Abies alba in a French Forest. Sci. Total Environ. 2006;354:232–245. doi: 10.1016/j.scitotenv.2005.01.044. [DOI] [PubMed] [Google Scholar]
- 32.Dormont L., Roques A., Malosse C. Cone and Foliage Volatiles Emitted by Pinus Cembra and Some Related Conifer Species. Phytochemistry. 1998;49:1269–1277. doi: 10.1016/S0031-9422(98)00105-8. [DOI] [Google Scholar]
- 33.Wajs-Bonikowska A., Sienkiewicz M., Stobiecka A., Maciąg A., Szoka Ł., Karna E. Chemical Composition and Biological Activity of Abies alba and A. koreana Seed and Cone Essential Oils and Characterization of Their Seed Hydrolates. Chem. Biodivers. 2015;12:407–418. doi: 10.1002/cbdv.201400167. [DOI] [PubMed] [Google Scholar]
- 34.Chalchat J.-C., Sidibé L., Maksimovic Z., Petrovic S., Gorunovic M. Essential Oil of Abies alba Mill., Pinaceae, from the Pilot Production in Montenegro. J. Essent. Oil Res. 2001;13:288–289. doi: 10.1080/10412905.2001.9699696. [DOI] [Google Scholar]
- 35.Yang S.-A., Jeon S.-K., Lee E.-J., Im N.-K., Jhee K.-H., Lee S.-P., Lee I.-S. Radical Scavenging Activity of the Essential Oil of Silver Fir (Abies alba) J. Clin. Biochem. Nutr. 2009;44:253–259. doi: 10.3164/jcbn.08-240. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 36.Roussis V., Couladis M., Tzakou O., Loukis A., Petrakis P.V., Dukic N.M., Jancic R. A Comparative Study on the Needle Volatile Constituents of Three Abies Species Grown in South Balkans. J. Essent. Oil Res. 2000;12:41–46. doi: 10.1080/10412905.2000.9712038. [DOI] [Google Scholar]
- 37.Garzoli S., Masci V.L., Caradonna V., Tiezzi A., Giacomello P., Ovidi E. Liquid and Vapor Phase of Four Conifer-Derived Essential Oils: Comparison of Chemical Compositions and Antimicrobial and Antioxidant Properties. Pharmaceuticals. 2021;14:134. doi: 10.3390/ph14020134. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 38.Kubeczka K.-H., Schultze W. Biology and Chemistry of Conifer Oils. Flavour Fragr. J. 1987;2:137–148. doi: 10.1002/ffj.2730020402. [DOI] [Google Scholar]
- 39.Mitić Z.S., Stojanović-Radić Z.Z., Jovanović S.Č., Cvetković V.J., Nikolić J.S., Ickovski J.D., Mitrović T.L., Nikolić B.M., Zlatković B.K., Stojanović G.S. Essential Oils of Three Balkan Abies Species: Chemical Profiles, Antimicrobial Activity and Toxicity toward Artemia salina and Drosophila melanogaster. Chem. Biodivers. 2022;19:e202200235. doi: 10.1002/cbdv.202200235. [DOI] [PubMed] [Google Scholar]
- 40.Valková V., Ďúranová H., Vukovic N.L., Vukic M., Kluz M., Kačániová M. Assessment of Chemical Composition and Anti-Penicillium Activity of Vapours of Essential Oils from Abies alba and Two Melaleuca Species in Food Model Systems. Molecules. 2022;27:3101. doi: 10.3390/molecules27103101. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 41.Lanzerstorfer A., Hackl M., Schlömer M., Rest B., Deutsch-Grasl E., Lanzerstorfer C. The Influence of Air-Dispersed Essential Oils from Lemon (Citrus limon) and Silver Fir (Abies alba) on Airborne Bacteria and Fungi in Hospital Rooms. J. Environ. Sci. Health Part A. 2019;54:256–260. doi: 10.1080/10934529.2018.1546498. [DOI] [PubMed] [Google Scholar]
- 42.De Groot A.C., Schmidt E. Essential Oils Contact Allergy and Chemical Composition. Routledge; London, UK: 2021. [Google Scholar]
- 43.Duquesnoy E., Marongiu B., Castola V., Piras A., Porcedda S., Casanova J. Combined Analysis by GC (RI), GC-MS and 13C NMR of the Supercritical Fluid Extract of Abies alba Twigs. Nat. Prod. Commun. 2010;5:1995–1998. doi: 10.1177/1934578X1000501235. [DOI] [PubMed] [Google Scholar]
- 44.Salem M.Z.M., Zeidler A., Böhm M., Mohamed M.E.A., Ali H.M. GC/MS Analysis of Oil Extractives from Wood and Bark of Pinus Sylvestris, Abies alba, Picea abies, and Larix decidua. BioResources. 2015;10:7725–7737. doi: 10.15376/biores.10.4.7725-7737. [DOI] [Google Scholar]
- 45.Lang K.J. Abies alba Mill.: Differentiation of Provenances and Provenance Groups by the Monoterpene Patterns in the Cortex Resin of Twigs. Biochem. Syst. Ecol. 1994;22:53–63. doi: 10.1016/0305-1978(94)90114-7. [DOI] [Google Scholar]
- 46.O’Neill J.A., Gallagher O.P., Devine K.J., Jones P.W., Maguire A.R. Desmethylabietospiran, a Naturally Occurring Self-Gelation Agent. J. Nat. Prod. 2005;68:125–128. doi: 10.1021/np049816u. [DOI] [PubMed] [Google Scholar]
- 47.Steglich W., Klaar M., Zechlin L., Hecht H.J. Abietospiran, the Triterpene from the Bark of the White Fir (Abies alba) Angew. Chem. Int. Ed. Engl. 1979;18:698. doi: 10.1002/anie.197906981. [DOI] [Google Scholar]
- 48.Wajs A., Urbańska J., Zaleśkiewicz E., Bonikowski R. Composition of Essential Oil from Seeds and Cones of Abies alba. Nat. Prod. Commun. 2010;5:1291–1294. doi: 10.1177/1934578X1000500830. [DOI] [PubMed] [Google Scholar]
- 49.Bazdi B., Oller-López J.L., Cuerva J.M., Oltra J.E., Mansour A.I. Composition of the Essential Oil from the Seeds of Abies Marocana. J. Essent. Oil Res. 2006;18:160–161. doi: 10.1080/10412905.2006.9699053. [DOI] [Google Scholar]
- 50.Patyra A., Dudek M.K., Kiss A.K. LC-DAD-ESI-MS/MS and NMR Analysis of Conifer Wood Specialized Metabolites. Cells. 2022;11:3332. doi: 10.3390/cells11203332. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 51.Kebbi-Benkeder Z., Colin F., Dumarçay S., Gérardin P. Quantification and Characterization of Knotwood Extractives of 12 European Softwood and Hardwood Species. Ann. For. Sci. 2015;72:277–284. doi: 10.1007/s13595-014-0428-7. [DOI] [Google Scholar]
- 52.Tavčar Benković E., Žigon D., Mihailović V., Petelinc T., Jamnik P., Kreft S. Identification, in Vitro and in Vivo Antioxidant Activity, and Gastrointestinal Stability of Lignans from Silver Fir (Abies alba) Wood Extract. J. Wood Chem. Technol. 2017;37:467–477. doi: 10.1080/02773813.2017.1340958. [DOI] [Google Scholar]
- 53.Bianchi S., Kroslakova I., Janzon R., Mayer I., Saake B., Pichelin F. Characterization of Condensed Tannins and Carbohydrates in Hot Water Bark Extracts of European Softwood Species. Phytochemistry. 2015;120:53–61. doi: 10.1016/j.phytochem.2015.10.006. [DOI] [PubMed] [Google Scholar]
- 54.Brennan M., Fritsch C., Cosgun S., Dumarcay S., Colin F., Gérardin P. Quantitative and Qualitative Composition of Bark Polyphenols Changes Longitudinally with Bark Maturity in Abies alba Mill. Ann. For. Sci. 2020;77:9. doi: 10.1007/s13595-019-0916-x. [DOI] [Google Scholar]
- 55.Leone K., Micheletto M., Di Maira G., Tedesco E., Benetti F., Zaloker U. Role of a Novel Silver Fir (Abies alba) Extract, Abigenol®/AlbiPhenol®, in Modulating Cardiovascular Disorders: Key Factors. Antioxidants. 2022;11:618. doi: 10.3390/antiox11040618. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 56.Wajs-Bonikowska A., Smeds A., Willför S. Chemical Composition and Content of Lipophilic Seed Extractives of Some Abies and Picea Species. Chem. Biodivers. 2016;13:1194–1201. doi: 10.1002/cbdv.201600014. [DOI] [PubMed] [Google Scholar]
- 57.Bianchi S., Giovannini L. Inhibition of MTOR/S6K1/4E-BP1 Signaling by Nutraceutical SIRT1 Modulators. Nutr. Cancer. 2018;70:490–501. doi: 10.1080/01635581.2018.1446093. [DOI] [PubMed] [Google Scholar]
- 58.Novotný R., Černý D., Šrámek V. Nutrition of Silver Fir (Abies alba Mill) Growing at the Upper Limit of Its Occurrence in the Šumava National Park and Protected Landscape Area. J. For. Sci. 2010;56:381–388. doi: 10.17221/87/2009-JFS. [DOI] [Google Scholar]
- 59.Szymura T.H. Concentration of Elements in Silver Fir (Abies alba Mill.) Needles as a Function of Needles’ Age. Trees. 2009;23:211–217. doi: 10.1007/s00468-008-0268-x. [DOI] [Google Scholar]
- 60.Durzan D.J. Arginine, Scurvy and Cartier’s “Tree of Life”. J. Ethnobiol. Ethnomedicine. 2009;5:5. doi: 10.1186/1746-4269-5-5. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 61.Radulescu V., Ilies D.-C., Voiculescu I., Iovu-Adrian B., Craciunescu A. Determination of Ascorbic Acid in Shoots from Different Coniferous Species by HPLC. Farmacia. 2013;61:1158–1166. [Google Scholar]
- 62.Adams M., Berset C., Kessler M., Hamburger M. Medicinal Herbs for the Treatment of Rheumatic Disorders—A Survey of European Herbals from the 16th and 17th Century. J. Ethnopharmacol. 2009;121:343–359. doi: 10.1016/j.jep.2008.11.010. [DOI] [PubMed] [Google Scholar]
- 63.Papp N., Purger D., Czigle S., Czégényi D., Stranczinger S., Tóth M., Dénes T., Kocsis M., Takácsi-Nagy A., Filep R. The Importance of Pine Species in the Ethnomedicine of Transylvania (Romania) Plants. 2022;11:2331. doi: 10.3390/plants11182331. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 64.Jarić S., Kostić O., Mataruga Z., Pavlović D., Pavlović M., Mitrović M., Pavlović P. Traditional Wound-Healing Plants Used in the Balkan Region (Southeast Europe) J. Ethnopharmacol. 2018;211:311–328. doi: 10.1016/j.jep.2017.09.018. [DOI] [PubMed] [Google Scholar]
- 65.Mazzei R., De Marco E.V., Gallo O., Tagarelli G. Italian Folk Plant-Based Remedies to Heal Headache (XIX–XX Century) J. Ethnopharmacol. 2018;210:417–433. doi: 10.1016/j.jep.2017.09.005. [DOI] [PubMed] [Google Scholar]
- 66.Monari S., Ferri M., Salinitro M., Tassoni A. Ethnobotanical Review and Dataset Compiling on Wild and Cultivated Plants Traditionally Used as Medicinal Remedies in Italy. Plants. 2022;11:2041. doi: 10.3390/plants11152041. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 67.Gilca M., Tiplica G.S., Salavastru C.M. Traditional and Ethnobotanical Dermatology Practices in Romania and Other Eastern European Countries. Clin. Dermatol. 2018;36:338–352. doi: 10.1016/j.clindermatol.2018.03.008. [DOI] [PubMed] [Google Scholar]
- 68.Bonet M.À., Vallès J. Pharmaceutical Ethnobotany in the Montseny Biosphere Reserve (Catalonia, Iberian Peninsula). General Results and New or Rarely Reported Medicinal Plants. J. Pharm. Pharmacol. 2010;55:259–270. doi: 10.1211/002235702432. [DOI] [PubMed] [Google Scholar]
- 69.Bacanlı M., Başaran A.A., Başaran N. The Antioxidant and Antigenotoxic Properties of Citrus Phenolics Limonene and Naringin. Food Chem. Toxicol. 2015;81:160–170. doi: 10.1016/j.fct.2015.04.015. [DOI] [PubMed] [Google Scholar]
- 70.Wei A., Shibamoto T. Antioxidant Activities and Volatile Constituents of Various Essential Oils. J. Agric. Food Chem. 2007;55:1737–1742. doi: 10.1021/jf062959x. [DOI] [PubMed] [Google Scholar]
- 71.Kačániová M., Vukovič N., Horská E., Salamon I., Bobková A., Hleba L., Fiskelová M., Vatľák A., Petrová J., Bobko M. Antibacterial Activity against Clostridium Genus and Antiradical Activity of the Essential Oils from Different Origin. J. Environ. Sci. Health B. 2014;49:505–512. doi: 10.1080/03601234.2014.896673. [DOI] [PubMed] [Google Scholar]
- 72.Vasincu A., Creţu E., Geangalău I., Amalinei R.L.M., Miron A. Polyphenolic Content and Antioxidant Activity of an Extractive Fraction from Abies alba Bark. Rev. Med. Chir. Soc. Med. Nat. Iasi. 2013;117:545–550. [PubMed] [Google Scholar]
- 73.Cunningham E. What Has Happened to the ORAC Database? J. Acad. Nutr. Diet. 2013;113:740. doi: 10.1016/j.jand.2013.03.007. [DOI] [PubMed] [Google Scholar]
- 74.Lunder M., Roškar I., Hošek J., Štrukelj B. Silver Fir (Abies alba) Extracts Inhibit Enzymes Involved in Blood Glucose Management and Protect against Oxidative Stress in High Glucose Environment. Plant Foods Hum. Nutr. 2019;74:47–53. doi: 10.1007/s11130-018-0698-6. [DOI] [PubMed] [Google Scholar]
- 75.Bağci E., Diğrak M. Antimicrobial Activity of Essential Oils of Some Abies (Fir) Species from Turkey. Flavour Fragr. J. 1996;11:251–256. doi: 10.1002/(SICI)1099-1026(199607)11:4<251::AID-FFJ577>3.0.CO;2-K. [DOI] [Google Scholar]
- 76.Bueno J. In Vitro Antimicrobial Activity of Natural Products Using Minimum Inhibitory Concentrations: Looking for New Chemical Entities or Predicting Clinical Response. Med. Aromat. Plants. 2012;1:1000113. doi: 10.4172/2167-0412.1000113. [DOI] [Google Scholar]
- 77.Jeršek B., Poklar Ulrih N., Skrt M., Gavarić N., Božin B., Smole Možina S. Effects of Selected Essential Oils on the Growth and Production of Ochratoxin A by Penicillium Verrucosum. Arh. Hig. Rada Toksikol. 2014;65:199–208. doi: 10.2478/10004-1254-65-2014-2486. [DOI] [PubMed] [Google Scholar]
- 78.Salamon I., Kryvtsova M., Bucko D., Tarawneh A.H. Chemical Characterization and Antimicrobial Activity of Some Essential Oils after Their Industrial Large-Scale Distillation. J. Microbiol. Biotechnol. Food Sci. 2021;2021:984–988. doi: 10.15414/jmbfs.2019.8.4.984-988. [DOI] [Google Scholar]
- 79.Şandru D.M. Antimicrobial Effect of Escherichia Coli on Essential Oils Derived from Romanian Aromatic Plants. Acta Univ. Cibiniensis Ser. E Food Technol. 2015;19:87–92. doi: 10.1515/aucft-2015-0009. [DOI] [Google Scholar]
- 80.Liu T.-T., Yang T.-S. Antimicrobial Impact of the Components of Essential Oil of Litsea Cubeba from Taiwan and Antimicrobial Activity of the Oil in Food Systems. Int. J. Food Microbiol. 2012;156:68–75. doi: 10.1016/j.ijfoodmicro.2012.03.005. [DOI] [PubMed] [Google Scholar]
- 81.Di Pasqua R., Betts G., Hoskins N., Edwards M., Ercolini D., Mauriello G. Membrane Toxicity of Antimicrobial Compounds from Essential Oils. J. Agric. Food Chem. 2007;55:4863–4870. doi: 10.1021/jf0636465. [DOI] [PubMed] [Google Scholar]
- 82.Van Vuuren S.F., Viljoen A.M. Antimicrobial Activity of Limonene Enantiomers and 1,8-Cineole Alone and in Combination. Flavour Fragr. J. 2007;22:540–544. doi: 10.1002/ffj.1843. [DOI] [Google Scholar]
- 83.da Silva A.C.R., Lopes P.M., de Azevedo M.M.B., Costa D.C.M., Alviano C.S., Alviano D.S. Biological Activities of A-Pinene and β-Pinene Enantiomers. Molecules. 2012;17:6305–6316. doi: 10.3390/molecules17066305. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 84.Nissen L., Zatta A., Stefanini I., Grandi S., Sgorbati B., Biavati B., Monti A. Characterization and Antimicrobial Activity of Essential Oils of Industrial Hemp Varieties (Cannabis sativa L.) Fitoterapia. 2010;81:413–419. doi: 10.1016/j.fitote.2009.11.010. [DOI] [PubMed] [Google Scholar]
- 85.Hachlafi N.E., Aanniz T., Menyiy N.E., Baaboua A.E., Omari N.E., Balahbib A., Shariati M.A., Zengin G., Fikri-Benbrahim K., Bouyahya A. In Vitro and in Vivo Biological Investigations of Camphene and Its Mechanism Insights: A Review. Food Rev. Int. 2021;39:1799–1826. doi: 10.1080/87559129.2021.1936007. [DOI] [Google Scholar]
- 86.Runyoro D., Ngassapa O., Vagionas K., Aligiannis N., Graikou K., Chinou I. Chemical Composition and Antimicrobial Activity of the Essential Oils of Four Ocimum Species Growing in Tanzania. Food Chem. 2010;119:311–316. doi: 10.1016/j.foodchem.2009.06.028. [DOI] [Google Scholar]
- 87.Raman A., Weir U., Bloomfield S.F. Antimicrobial Effects of Tea-Tree Oil and Its Major Components on Staphylococcus aureus, Staph. Epidermidis and Propionibacterium Acnes. Lett. Appl. Microbiol. 1995;21:242–245. doi: 10.1111/j.1472-765X.1995.tb01051.x. [DOI] [PubMed] [Google Scholar]
- 88.Cosentino S., Tuberoso C.I.G., Pisano B., Satta M., Mascia V., Arzedi E., Palmas F. In-Vitro Antimicrobial Activity and Chemical Composition of Sardinian Thymus Essential Oils. Lett. Appl. Microbiol. 1999;29:130–135. doi: 10.1046/j.1472-765X.1999.00605.x. [DOI] [PubMed] [Google Scholar]
- 89.Tabanca N., Kırımer N., Demirci B., Demirci F., Başer K.H.C. Composition and Antimicrobial Activity of the Essential Oils of Micromeria cristata subsp. Phrygia and the Enantiomeric Distribution of Borneol. J. Agric. Food Chem. 2001;49:4300–4303. doi: 10.1021/jf0105034. [DOI] [PubMed] [Google Scholar]
- 90.Nikolova M.T., Yordanov P., Slavov S., Berkov S. Antifungal Activity of Plant Extracts against Phytopathogenic Fungi: Antifungal Activity of Plant Extracts. J. Biosci. Biotechnol. 2017;6:155–161. [Google Scholar]
- 91. Valimaa A., Honkalampihamalainen U., Pietarinen S., Willfor S., Holmbom B., Vonwright A. Antimikrobiálne a cytotoxické extrakty z hrčat a súvisiace čisté zlúčeniny a ich účinky na mikroorganizmy spojené s potravinami. Int. J. Food Microbiol. 2007;115:235–243. doi: 10.1016/j.ijfoodmicro.2006.10.031. [ DOI ] [ PubMed ] [ Google Scholar ]
- 92. Kim K.-T., Rioux L.-E., Turgeon SL Inhibícia alfa-amylázy a alfa-glukozidázy je diferencovane modulovaná fukoidanom získaným z Fucus Vesiculosus a Ascophyllum Nodosum. Fytochemia. 2014;98:27–33. doi: 10.1016/j.phytochem.2013.12.003. [ DOI ] [ PubMed ] [ Google Scholar ]
- 93. Debeljak J., Ferk P., Cokolic M., Zavratnik A., Tavcar Benkovic E., Kreft S., Štrukelj B. Randomizovaná, dvojito zaslepená, skrížená, placebom a účinnou látkou kontrolovaná farmakodynamická štúdia u ľudí o vplyve extraktu z dreva jedle striebornej (Belinal) na postprandiálnu glykemickú odpoveď. Pharmazie. 2016;71:566–569. doi: 10.1691/ph.2016.6658. [ DOI ] [ PubMed ] [ Google Scholar ]
- 94.Drevenšek G., Lunder M., Benković E.T., Štrukelj B., Kreft S. Kardioprotektívne účinky extraktu z jedle striebornej (Abies alba) v izolovaných srdciach potkanov s ischemickou reperfúziou. Potravinový Nutr. Rezolúcia 2016;60:29623. DOI: 10.3402/fnr.v60.29623. [DOI] [PMC bezplatný článok] [PubMed] [Google Scholar]
- 95.Zorko M.S., Štrukelj B., Švajger U., Kreft S., Lunder T. Účinnosť polyfenolického extraktu z kôry jedle striebornej (Abies alba) na psoriázu: randomizovaná, dvojito zaslepená, placebom kontrolovaná štúdia. Pharm. 2018; 73:56–60. DOI: 10.1691/ph.2018.7741. [DOI] [PubMed] [Google Scholar]
- 96.Karkabounas S., Assimakopoulos D., Malamas M., Skaltsounis A.L., Leonce S., Zelovitis J., Stefanou D., Evangelou A. Antiproliferatívne a antikarcinogénne účinky vodného prípravku Abies alba a Viscum Album Se Abies na malígnu bunkovú líniu L-1210 a nádorové potkany Wistar. Protirakovinové uznesenie 2000; 20:4391–4395. [PubMed] [Google Scholar]